Bryan人工颈椎椎间盘假体以重建颈椎运动单位生理活动功能、维持颈椎生物力学特性为设计理念,在治疗颈椎椎间盘突出症、颈椎病的临床研究中受到广泛关注和高度重视。随着临床应用研究的逐步推广和深入,Bryan人工颈椎椎间盘置换术(artificial cervical disc replaement,ACDR)对颈椎病和颈椎椎间盘突出症的治疗取得良好的早期临床疗效[1, 2, 3, 4],但仍缺乏进一步的中长期随访观察。本院自2004年3月开展了Bryan ACDR,其中13例进行了5年以上的中长期临床随访观察,着重了解其临床疗效和假体并发症发生情况。
1 资料与方法
1.1 一般资料资料完整的13例颈椎椎间盘突出症患者,男9例,女4例;年龄为33~53岁,平均44岁。8例以神经根性症状为主,表现为一侧上肢放射性疼痛,相应皮肤区域感觉减退,严重者伴有一侧上肢肌力减退的不全瘫表现;5例以脊髓压迫症状为主,主要表现为四肢麻木、肌力下降、行走不稳、反射亢进等。术前行颈椎正侧位、双斜位、过伸过屈位X线检查,显示病变节段椎体后缘部分存在少量骨质增生,但无明显的动态不稳和小关节突退变表现。颈椎MRI检查显示病变节段椎间盘向后方或症状侧突出或脱出,致使硬膜囊或神经根受压,其中2例脊髓信号发生改变,但无明显脊髓后方压迫或椎管狭窄表现。 1.2 手术方法
患者全麻,仰卧位,保持颈部中立位并行露骨牵引,双上肢对抗牵引。取右侧颈前横切口,经颈血管鞘与食管气管鞘之间隙达椎体前方,在C形臂X线机透视下确定置换间隙,切除目标间隙前方纤维环、髓核组织及上下软骨终板直至两侧钩椎关节并接近椎体后缘。安装Bryan系统支架,用球形磨钻去除置换节段终板前缘骨赘,切除该间隙上位椎体前下缘部分骨质,减小其穹顶前缘弧度。用椎间撑开棒逐级撑开椎间隙至8.5 mm,将矢状位楔形定位器在中点插入椎间隙,放置双轨打磨导向器,调整可调钻套,使之与上位椎体前缘接触,用磨钻测深尺测定椎体深度,依序选取相应尺寸的柱状磨钻和盘状磨钻削磨上位椎体下终板和下位椎体上终板,直至凹床成形。拆除导向器,切除椎体后方残留纤维环、髓核组织及增生骨赘,如果后纵韧带破裂,应当切开后纵韧带并取出游离的椎间盘髓核组织,使脊髓获得完全减压。准备相应规格Bryan人工椎间盘,生理盐水灌注,压缩成型后置入椎间隙。C形臂X线机透视观察假体位置。止血,置负压引流管1根,缝合切口。 1.3 术后处理
术后8~12 h拔除气管插管,24~48 h拔除负压引流,可在颈托保护下逐步离床活动。术后2周后去除颈托,鼓励行颈背肌锻练。术后2周内常规口服塞来昔布胶囊。定期于术后1、3、6、12个月门诊随访,以后每年随访1次,摄颈椎正侧位、过伸过屈位X线片。 1.4 评价方法
Odom评级[5]判断疗效:优,≥80%术前症状和体征有改善;良好,≥70%且<80%术前症状和体征有改善;一般,≥50%且<70%术前症状和体征得到改善;差,<50%的术前症状和体征有改善。
日本骨科学会(Japanese Orthopaedic Association,JOA)(17分)评分法[6]评估患者手术前后的神经功能状态,并计算神经功能改善率(rate of the improved JOA score,RIS),RIS =(术后评分-术前评分)/(17分-术前评分)×100%。
通过颈椎正侧位、过伸过屈位X线片观察和测量假体位移、骨吸收、异位骨化、假体活动度及颈椎生理曲度变化情况,评价假体位置、稳定性及活动度变化。用Cobb角评价置换节段及上下邻近节段活动度(range of motion,ROM)大小。 1.5 统计学分析
所采集数据采用SPSS 11.5软件进行统计分析,通过t检验,当P<0.05时认为差异有统计学意义。 2 结果
本组13例患者均实施了Bryan ACDR,其中单节段置换11例:C3/C4 1例,C4/C5 1例,C5/C6 8例,C6/C7 1例;双节段置换2例:C4/C5/C6 1例,C3/C4合并C5/C61例,共置入Bryan人工椎间盘15个,术中术后无神经、脊髓和血管损伤等并发症发生,术后随访5~7年,平均5.5年。
术后早期,8例根性症状为主的患者,6例症状完全缓解,2例明显改善,仅残留神经支配区域的轻微麻木;5例脊髓症状为主的患者,3例主观症状明显改善,2例残留肌张力较高、反射亢进等体征。Odom评级,优9例,良2例,一般2例,优良率为84.6%。脊髓功能JOA评分由术前平均11.6分,提高到术后平均14.8分,改善率为59.3%,有效率为100%。颈椎X线片示人工椎间盘假体位置准确,符合置入要求,5例颈椎生理曲度异常者术后有改善,8例颈椎生理曲度正常者维持正常状态。置入的人工椎间盘假体都达到确切的稳定,无假体前后位移≥2 mm,无脱落发生。术前置换节段平均ROM为4.6°,在术后早期达到8.5°,术后与术前相比差异有统计学意义(P<0.05);上下邻近节段术前ROM分别为7.2°和6.5°,术后分别为7.0°和6.2°,与术前相比略有减小,但差异无统计学意义(P<0.05,见表 1)。
|
|
表 1 手术前后置换节段与邻近节段平均ROM Tab. 1 Preoperative and postoperative average ROM at implanted and adjacent segments |
末次随访时(≥5年),全部患者术前的根性或脊髓症状持续改善,未出现症状复发加重。Odom评级,优10例,良2例,一般1例,优良率为92.3%。JOA评分达到平均15.6分,改善率为74.1%。颈椎X线片示全部病例颈椎曲度保持稳定(见图 1),1例单节段椎间盘置换患者在置换节段发生自发性融合(见图 2);1例在假体置入间隙的上椎体前下缘有较明显的骨质吸收,约2.5 mm,并伴有假体的轻微前移和沉陷以及椎体后缘的异位骨化(Ⅲ度)。上述2例患者近1年在长时间的伏案工作后出现颈肩部酸胀不适的轴性症状,休息、按摩后可缓解;其余11例人工颈椎椎间盘假体无松动、不稳及沉陷表现,假体与上下椎体终板间无X线透光线出现,仅个别假体前上缘与上位椎体前下缘间有轻微骨质吸收现象。未发生自发性融合的12例假体保持了良好的ROM,平均ROM达9.2°,优于术前且差异有统计学意义(P<0.05);邻近上下节段的ROM分别为7.1°和6.3°,略小于术前,但差异无统计学意义。
|
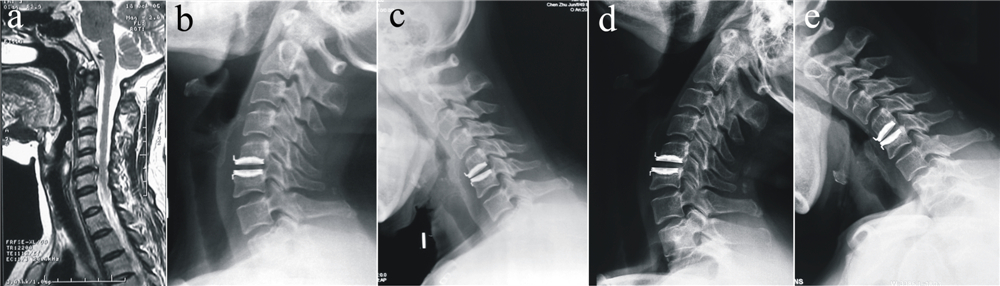
图 1 典型病例影像学资料 Fig. 1 Radiological data of a typical patient a: 术前MRI示C5/C6椎间盘突出 b,c: 术后1周颈椎动力位X线片示Bryan人工颈椎椎间盘稳定,活动度良好 d,e: 术后6年颈椎动力位X线片示Bryan人工颈椎椎间盘稳定,活动度良好 a: Preoperative MRI shows C5/C6 disc herniation b,c: Cervical dynamic reontgenographs 1 week postoperatively shows that the stability and range of motion of Bryan cervical prothesis is normal d,e: Cervical dynamic reontgenographs 6 years postoperatively shows that the stability and range of motion of Bryan cervical prothesis is normal |
|
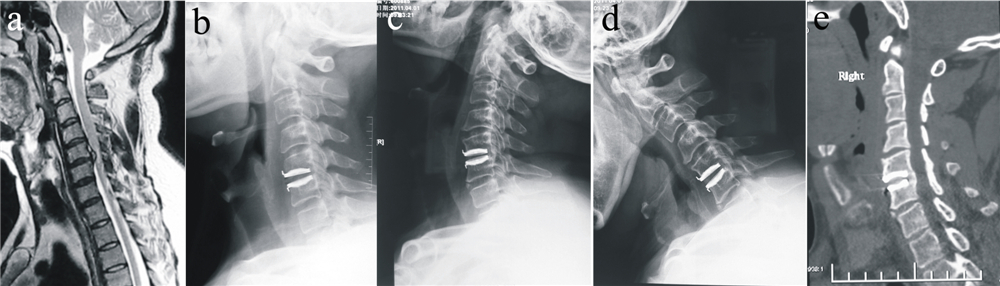
图 2 术后置换节段自发融合患者的影像学资料 Fig. 2 Radiological data of a patient with spontaneous fusion of Bryan cervical prothesis a: 术前MRI示C5/C6椎间盘突出,脊髓信号异常 b: 术后1周侧位X线片示Bryan人工颈椎间盘位置良好,颈椎序列正常 c,d: 术后7年颈椎动力位X线片示Bryan人工颈椎间盘自发融合,活动度消失 e: 术后7年矢状位CT重建示Bryan人工颈椎间盘置换节段自发融合 a: Preoperative MRI shows C5/C6 disc herniation,and the signal of spinal cord is abnormal b: Cervical lateral reontgenograph 1 week postoperatively shows that the location of Bryan cervical prothesis and cervical array are normal c,d: Cervical dynamic reontgenograph 7 years postoperatively shows the spontaneous fusion of Bryan cervical prothesis and the disapearance of range of motion e: Sagittal plane CT 7 years postoperatively shows the spontaneous fusion of Bryan cervical prothesis |
经典的前路减压融合术以其确实可靠的疗效而成为治疗颈椎病及颈椎椎间盘突出症的金标准,但其 牺牲病变节段活动功能所付出的代价却在多年的随 访中逐步显现,给愈来愈多的颈椎融合术后患者带来颈部轴性症状和邻近节段病的困扰。以Bryan 人工颈椎椎间盘为代表的非融合技术是以重建颈椎生理活动功能为设计理念,大量早期临床应用研究显示在充分减压的基础上置入Bryan人工椎间盘治疗颈椎椎间盘突出症可以取得和传统减压融合术相当的临床疗效,同时人工假体在术后确实可以保留或恢复手术节段的运动功能,并维持颈椎生理曲度 [1, 2, 3, 4]。但Bryan ACDR是否可以减少颈部轴性症状、邻近节段病等并发症的发生,假体是否可以与受体长期匹配,以及置入物的可靠性等问题仍缺乏必要认识。
3.1 Bryan ACDR的中长期疗效本组13例接受ACDR治疗的颈椎椎间盘突出症患者经过5年以上的中长期随访,临床疗效的Odom评级优良率达到92.3%,脊髓功能JOA评分达到15.6分,改善率达到74.1%。虽然病例数较少,未与同期前路减压融合术病例进行直接的对照研究,但对照前路减压融合术的相关文献报道[7],这一结果仍令笔者感到满意。
本组Bryan ACDR所取得的临床疗效与多种因素相关。首先,充分减压是手术的关键,彻底去除对脊髓和神经根的压迫是手术成功的根本保证,对于融合与非融合术具有同样重要的意义。其次,Bryan ACDR中对上下终板的打磨更为彻底,避免退变椎间盘残留,降低复发概率,而更为开阔的深部视野为椎体后缘和后纵韧带的处理提供了更为开阔的空间,确保手术减压更彻底。最后,Bryan人工颈椎椎间盘具有良好的稳定性和相应的支撑作用以维持颈椎生理曲度[8]。本组中未出现人工假体失稳现象,避免了颈椎失稳所带来的神经症状;另外,除1例因上位椎体前下缘骨质吸收致使假体略有沉陷外,其余12例均保持了良好的椎间高度和矢状位序列,避免了因椎间高度丢失或序列紊乱所致的后方韧带皱褶而形成新的压迫。由此推测,Bryan ACDR可以取得良好的长期疗效。 3.2 Bryan ACDR与颈部轴性症状和邻近节段病变
颈部轴性症状是颈椎融合术后的常见并发症,其发生与否与患者神经症状的改善情况无关。Kawakami等[9]对60例颈椎前路融合术患者进行观察,发现有23例出现了较为明显的颈部轴性症状,发生率为38.3%。颈部轴性症状可能与多种因素有关,Liu等[10]认为颈椎生理曲度的异常是引发颈部轴性症状的重要原因。在正常颈椎生理前凸状态下,颈椎重力轴线将通过C3~6椎体后方,颈部肌群处于最佳力学状态维持颈椎矢状面力学平衡;当颈椎前凸减少时,颈部肌群需通过持续收缩和缩短的作用力臂维持头颅的正常位置,最终引发疲劳、疼痛并进一步加重力学失衡,引起颈项部疼痛、僵硬等轴性症状。因此,维持颈椎正常的生理曲度对减轻颈部轴性症状具有重要意义。
Fong等[11]认为Bryan人工颈椎椎间盘受其设计限制,其有限的支撑强度可能加重颈椎的局部后凸畸形,但同时也发现Bryan ACDR所致的局部后凸畸形并不一定加重颈部轴性症状,这可能与人工颈椎椎间盘保留了一定的生理运动功能有关。Shim等[8]的研究显示,ACDR可改善颈椎生理性前凸,有效维持颈椎矢状序列。生物力学测试结果显示ACDR保留了置换节段一定的生理ROM,既可避免增加临近节段的应力负荷,防止其过度活动,阻止或降低了邻近节段的退变速度,降低邻近节段病的发生率,同时还可使颈椎的正常生理运动得以保留,并维持肌肉系统的动力平衡,从而减少轴性症状的发生[12]。
本组中2例患者出现了颈部轴性症状,1例发生了置换节段的自发融合,1例则出现假体前缘骨质吸收伴轻微沉陷和异位骨化,其余11例的Bryan人工颈椎椎间盘则活动功能良好,改善或维持了颈椎生理曲度,未出现明显颈部轴性症状。由此推测,功能正常的人工颈椎椎间盘假体对维持颈椎生理曲度及降低颈部轴性症状具有一定意义。本组未发生邻近节段病,测量本组颈椎椎间盘置换和邻近节段的活动度,结果显示置换的Bryan人工颈椎椎间盘提供了该节段比术前更大的ROM,而邻近节段的ROM则与术前保持基本一致。由此推测,置换节段所保留的颈椎ROM避免了邻近节段代偿性的过度活动,可能有助于降低邻近节段病发生率,间接显示出Bryan人工颈椎椎间盘对邻近节段的保护作用[13]。 3.3 Bryan ACDR的异位骨化和自发性融合
Bryan ACDR后的异位骨化与多种因素相关[14],而自发性融合多由异位骨化发展而来。Wang等[15]认为Bryan ACDR中对椎体终板进行打磨的过程会产生骨碎屑和残渣,如果没有彻底冲洗而残留在置换间隙的后方可能是术后发生异位骨化的重要原因。Leung等[16]认为异位骨化与性别和年龄有关,男性和老年患者更易出现异位骨化,同时还发现由于术中需要使用牵拉器拉开双侧颈长肌,可能造成颈长肌的损伤和炎症反应,这也许是术后发生异位骨化的启动因素之一。Goffin等[17]也认为异位骨化的发生是置换节段炎症反应的结果,因此建议术后常规应用非甾体抗炎药(non-steroidal antiinflammatory drugs,NSAIDs)2 周。Mehren等[18]的研究显示NSAIDs可在一定程度上降低ACDR后异位骨化的发生率。
本组1例自发性融合患者,术后即刻颈椎X线片显示Bryan人工颈椎椎间盘矢状径尺寸小于椎体终板矢状径,使上下终板后缘未被假体覆盖,随访2年后在椎体后缘出现异位骨化,随访第5年时该节段已发生自发性融合。由此推测,如果选择与上下终板匹配度最大的假体,尽可能将终板完全覆盖,减少终板间暴露面积,有可能避免异位骨化和自发性融合的发生。另1例由于在假体置入后1年内上位椎体下终板前缘间发生了明显的骨质吸收,使假体发生了相对的前移和沉陷,使该间隙上下终板后缘暴露范围扩大并相互接近,最终在末次随访时出现椎体后缘的异位骨化。由此可见,假体沉陷与移位而导致的椎间高度丢失也是发生异位骨化的可能因素。
目前为止,尚不清楚ACDR后异位骨化的发生机理,因此还没有一种方法能够从根本上预防或减少术后异位骨化的发生,除注意上述可能的相关因素外,在术中减压时应彻底切除椎体后缘增生骨赘,还应完全切除肥厚增生的后纵韧带,因为在异位骨化形成的过程中后纵韧带有可能起到类似支架的效应,切除肥厚增生的后纵韧带可以避免这一可能的负面效应,同时达到更加完善彻底的减压。
通过对本组13例Bryan ACDR患者5年以上的中长期随访,结果显示Bryan ACDR治疗颈椎椎间盘突出症可以取得较长时间的理想疗效。同时Bryan人工颈椎椎间盘假体可靠性较强,在体内可以较长时间保持稳定,并发挥相应的运动功能,对预防颈部轴性症状和邻近节段病的发生起到一定作用。由于本研究病例数量和随访时间有限,尚需要进一步大规模、长时间的研究观察其疗效。
| [1] | Ren X, Wang W, Chu T, et al. The intermediate clinical outcome and its limitations of bryan cervical arthroplasty for treatment of cervical disc herniation[J]. J Spinal Disord Tech, 2011, 24(4): 221-229. |
| [2] | 任先军, 王卫东, 初同伟, 等. 人工颈椎间盘置换术后早中期临床疗效及并发症评价[J]. 中国骨与关节损伤杂志, 2009, 24(10): 865-868. |
| [3] | 孙宇, 潘胜发, 张凤山, 等. Bryan人工椎间盘置换术治疗颈椎病的近期临床效果及出现的问题[J]. 中国脊柱脊髓杂志, 2008, 18(1): 13-17. |
| [4] | 徐荣明, 马维虎, 黄雷, 等. 颈椎人工椎间盘置换早期临床报道[J]. 脊柱外科杂志, 2006, 4(1): 1-4. |
| [5] | Odom GL, Finney W, Woodhall B. Cervical disc lesions[J]. J Am Med Assoc, 1958, 166(1): 23-28. |
| [6] | Yonenobu K, Wada E, Tanaka T, et al. Japanese Orthopaedic Association Cervical Myelopathy Evaluation Questionnaire (JOACMEQ): Part 2. Endorsement of the alternative item[J]. J Orthop Sci, 2007, 12(3):241-248. |
| [7] | Matsumoto M, Okada E, Ichihara D, et al. Anterior cervical decompression and fusion accelerates adjacent segment degeneration: comparison with asymptomatic volunteers in a ten-year magnetic resonance imaging follow-up study[J]. Spine (Phila Pa 1976), 2010, 35(1): 36-43. |
| [8] | Shim CS, Lee SH, Park HJ, et al. Early clinical and radiologic outcomes of cervical arthroplasty with Bryan Cervical Disc prosthesis[J]. J Spinal Disord Tech, 2006, 19(7): 465-470. |
| [9] | Kawakami M, Tamaki T, Yoshida M, et al. Axial symptoms and cervical alignments after cervical anterior spinal fusion for patients with cervical myelopathy[J]. J Spinal Disord, 1999, 12(1): 50-56. |
| [10] | Liu J, Ebraheim NA, Sanford CG Jr, et al. Preservation of the spinous process-ligament-muscle complex to prevent kyphotic deformity following laminoplasty[J]. Spine J, 2007, 7(2): 159-164. |
| [11] | Fong SY, DuPlessis SJ, Casha S, et al. Design limitations of Bryan disc arthroplasty[J]. Spine J, 2006, 6(3): 233-241. |
| [12] | DiAngelo DJ, Roberson JT, Metcalf NH, et al. Biomechanical testing of an artificial cervical joint and an anterior cervical plate[J]. J Spinal Disord Tech, 2003, 16(4): 314-323. |
| [13] | 蒋涛, 任先军, 王卫东, 等. 人工颈椎间盘置换对邻近节段椎间盘的保护作用[J]. 中国矫形外科杂志, 2010, 18(7): 529-533. |
| [14] | 周非非, 赵衍斌, 孙宇, 等. Bryan人工颈椎间盘置换术后异位骨化形成的临床因素分析[J]. 中国脊柱脊髓杂志, 2009, 19(1): 39-43. |
| [15] | Wang MY, Leung CH, Casey AT. Cervical arthroplasty with the Bryan Disc[J]. Neurosurgery, 2005, 56(1 Suppl): 58-65. |
| [16] | Leung C, Casey AT, Goffin J, et al. Clinical significance of heterotopic ossification in cervical disc replacement: a prospective multicenter clinical trial[J]. Neurosurgery, 2005, 57(4): 759-763. |
| [17] | Goffin J, Loon JV, Calenbergh FV. Cervical arthroplasty with the Bryan disc: 4-year results[J].Spine J, 2006, 6(5 suppl): S62-63. |
| [18] | Mehren C, Suchomel P, Grochulla F, et al. Heterotopic ossification in total cervical artificial disc replacement[J].Spine(Phila Pa 1976), 2006, 31(24): 2802-2806. |
 2011, Vol. 9
2011, Vol. 9


