2. 福建医科大学附属第一医院脊柱外科
传统开放式入路行腰椎后路融合术需从后正中线做切口广泛剥离椎旁肌,不少患者伴随腰椎手术失败综合征(failed back surgery syndrome,FBSS) [1],因此能够对椎旁肌结构及功能进行保护的手术入路越来越被人们所重视。本研究回顾分析采用椎旁肌间隙入路[2]患者的疗效,与传统开放式入路进行比较,现报道如下。
1 资料与方法 1.1 一般资料2008~2009年福建医科大学附属第一医院收治具有完整临床资料和随访信息下腰椎疾病的患者中,采用小切口椎旁肌间隙入路方式的有12例,男8 例,女4例;平均48.8岁(32~61岁);腰椎椎间盘突出症6例,腰椎滑脱6例。随机选取同时期由同一组医师采用传统手术入路方式完成的下腰椎手术患者10例,其中男 8例,女2例;平均50.5岁(39~58岁);其中腰椎椎间盘突出症4例,腰椎滑脱6例。术前常规行腰椎正侧位X线片及腰椎MRI检查,术后平均1年复查腰椎MRI。2组患者性别、年龄、诊断、术前疼痛视觉模拟量表(visual analogue scale,VAS)评分[3]、Oswestry功能障碍指数(Oswestry disability index,ODI)[4]差异均无统计学意义(P>0.05),具有可比性(见表 1)。
|
|
表 1 2种不同入路患者一般病例资料 Tab. 1 General clinical data of patients treated by 2 different approaches |
患者全身麻醉,俯卧位。 C形臂X线机透视正位,确定腰椎病变节段,体表分别标出双侧椎间隙平面上关节突外缘位置,并标好中线作为手术切口。沿中线做一个长约4 cm的纵行皮肤切口,切开胸腰筋膜。软组织向两侧牵开,椎旁肌肌间隙手术入路距后正中线约3 cm做单侧或双侧竖脊肌腱膜纵行切口,分离至胸腰筋膜与竖脊肌腱膜后,寻找多裂肌与最长肌的自然间隙,用手指作钝性分离,暴露关节突关节,顺着暴露方向剥离小关节、横突和椎板外侧少许表面软组织,不进行上关节突及横突区以外的操作,即可清楚显露上述结构而无须强力牵拉椎旁肌群等软组织,置入椎弓根螺钉并固定。在上下关节突之间的椎间软组织间隙显露黄韧带,沿上位椎体椎板下沿和下位椎体椎板上沿以及上下关节突内侧沿剥离、切除黄韧带,即可进入上下椎板之间无后壁骨性结构的椎管,必要时于相应椎体水平后方咬除一侧或双侧部分椎板(一侧或双侧有限“开窗”),咬除增生骨赘、摘除椎间盘,松解神经根,探子手感结合C形臂X线机透视下探查椎管情况,然后后斜向置入椎间融合器,术毕缝合肌间隙表面筋膜,肌肉自然紧密贴附对合,封闭死腔。传统手术入路切断多裂肌在棘突的起点,沿棘突单侧或两侧剥离骶棘肌直至关节突关节,咬除棘突、椎板,根据内倾角、头倾角调整置钉方向,并置钉、固定,进行椎间盘摘除、置入椎间融合器等操作,术毕剪除部分因过度牵拉、暴露时间过久而缺血的肌肉,不缝合肌膜,直接缝合腰背肌筋膜,关闭术腔。
术后卧床1周,鼓励患者床上行功能锻炼。1周后鼓励患者在腰围保护下下床活动,术后3个月内穿戴腰围,术后约1年复查腰椎MRI。
1.3 观察指标 1.3.1 术后评价观察指标记录2组手术时间、术中出血量及术后引流量,评估术后1年VAS评分和ODI。
1.3.2 MRI观察指标 1.3.2.1 多裂肌面积测量方法均使用高分辨率美国通用公司生产的1.5T超导MRI成像系统。腰椎矢状面成像T1加权采用自旋回波序列,T2加权采用快速自旋回波序列。采用福建实达软件公司提供的PACS浏览系统对腰椎椎间隙平面多裂肌横断面的面积进行测量。以上结果均由同一个人测量3次取平均值。
1.3.2.2 多裂肌残存率的计算方法多裂肌残存率=术后多裂肌面积/术前同平面多裂肌面积[5]。
1.4 统计学处理所有统计分析均采用SPSS 16.0统计软件完成。计数资料比较采用χ2检验和Fisher确切概率法:计量资料首先行正态性检验,数据以x±s差表示,不符合正态分布的数据行数据转换后分析,2组间比较采用成组t检验。P<0.05认为差异有统计学意义。
2 结果 2.1 术后评价结果2组手术时间、术中出血量、术后引流量、术后VAS评分及术后ODI差异有统计学意义(P<0.05,见表 2)。
|
|
表 2 2种不同入路患者情况比较 Tab. 2 Comparing parameters of patients treated by 2 different approaches |
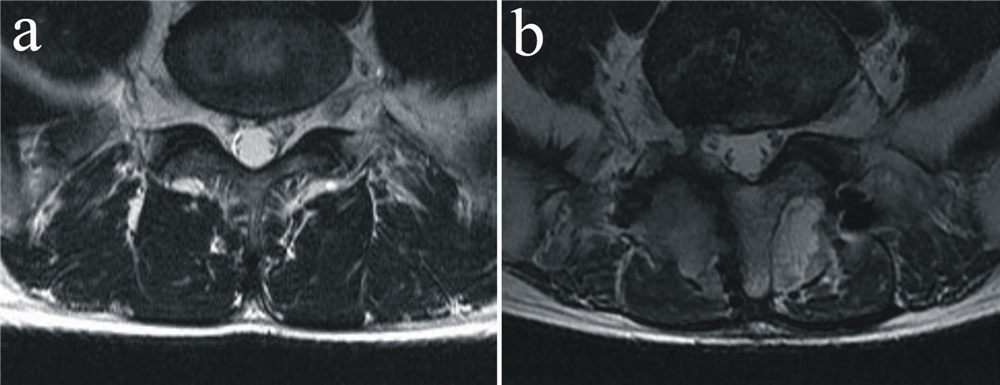
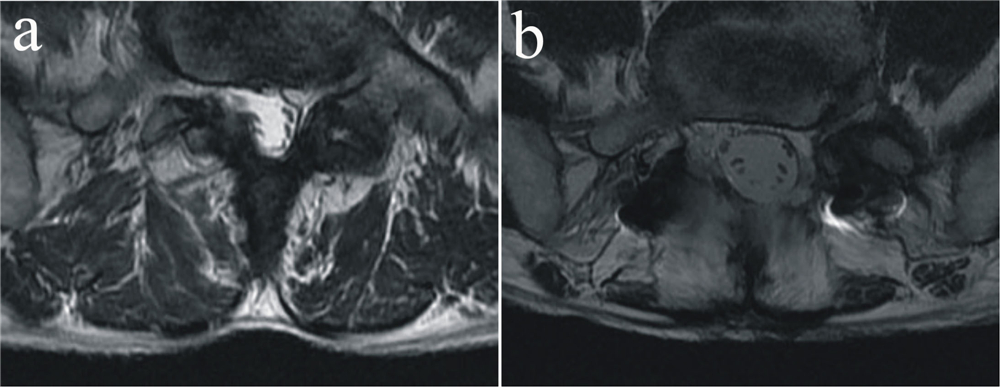
小切口椎旁肌间隙入路患者L4/L5节段MRI横断面所示多裂肌术前面积为(997.2± 138.2) mm2,术后为(961.7±173.0) mm2;L5/S1节段术前面积为(1 216.4±185.6) mm2 ,术后为(1 138.3±204.8 ) mm2;S1平面术前面积为(1 292.2±230.9)mm2 ,术后为(1 192.2± 179.8)mm2。 传统开放式入路患者L4/L5节段MRI横断面所示多裂肌术前面积为(1 016.7±159.4)mm2,术后为(754.4±78.5)mm2;L5/S1节段术前面积为(1 155.4±164.6)mm2 ,术后为(791.5±142.3)mm2;S1平面术前面积为(1 276.8±155.7)mm2 ,术后为(919.6±102.4)mm2。数据经配对Wilcoxon符号秩和检验,小切口椎旁肌间隙入路患者L4/L5/S1各平面手术多裂肌面积差异无统计学意义(P>0.05),多裂肌萎缩轻微(见图 1);传统开放式入路患者手术前后差异有统计学意义(P<0.05),可见术后多裂肌面积明显萎缩(见图 2)。
|
图 1 小切口椎旁肌间隙入路患者L5/S1平面多裂肌MRI
Fig. 1 Multifidus muscle MRI at L5/S1of a typical patient treatment by Wiltse approach
a: 术前MRI b: 术后MRI a: Preoperative MRI b: Postoperative MRI |
|
图 2 传统入路患者L5/S1平面多裂肌MRI
Fig. 2 Multifidus muscle MRI at L5/S1 of a typical patient treatment by traditional approach
a: 术前MRI b: 术后MRI a: Preoperative MRI b: Postoperative MRI |
小切口椎旁肌间隙入路患者L4/L5节段多裂肌残存率为0.96±0.09,L5/S1节段为0.94±0.10,S1平面为0.93±0.13 ;传统开放式入路患者L4/L5节段多裂肌残存率为0.75±0.08 ,L5/S1节段为0.69±0.10,S1平面为0.72±0.06。数据经Wilcoxon符号秩和检验,小切口椎旁肌间隙入路患者与传统入路患者各平面多裂肌残存率的差异有统计学意义(P<0.05)。
3 讨论 3.1 多裂肌损伤的分析肌酸激酶主要存在于骨骼肌组织,骨骼肌受损伤时血浆肌酸激酶显著升高。实验表明,肌酸激酶的升高主要与肌肉退变过程相关[6],腰椎后路手术3 h后腰背肌开始发生退变,1周后肌肉开始再生,因此其升高主要发生在术后1周内,时间曲线表现为术后第1天达高峰,以后逐渐下降,7 d后基本恢复正常。因此肌酸激酶可用于椎旁肌早期损伤的评价。
MRI对肌肉组织的显影可反映肌肉的去神经化改变[7];Stevens等[8]发现T2释放时间和表现弥散系数(apparent diffusion coefficient,ADC)值可直观地看到腰背肌肉水肿信号的差别。MRI成像技术具有对软组织进行细致成像的特点[9, 10],椎旁肌特别是多裂肌的损伤变化均可在腰椎MRI上观察到。本研究认为传统开放式手术入路广泛剥离椎旁肌并不仅仅影响手术节段椎旁肌,对手术相邻节段也存在牵拉造成的损伤。考虑个体间差异,本研究采用了多裂肌残存率进行2种入路的比较,期待比较结果更能反映2种手术入路对手术节段及相邻节段多裂肌的影响。结果显示小切口经椎旁肌间隙入路患者术后手术节段及相邻节段多裂肌残存率明显高于传统入路患者。
3.2 椎旁肌损伤与FBSS针对传统腰椎后路开放式手术一些学者报道了切开和挤压椎旁肌可以导致多裂肌的萎缩和去神经化,并最终增加了FBSS的风险[11, 12]。而腰背肌无力则是由于椎旁肌的失神经支配萎缩所致[13]。Stevens等[8]通过临床实验证明,肌肉神经支配和肌肉功能受损是术后腰背痛发生的重要原因。Burton等[14]报道,术后手术区域组织纤维化在导致术后FBSS的各种因素中约占24%。
国外学者报道了慢性腰背痛患者的多裂肌快肌纤维与慢肌纤维的构成比发生改变[15],甚至萎缩[16]。慢性腰背痛患者的多裂肌功能减退与慢性腰背痛可能互为因果。多裂肌功能减退不能有效控制外在负荷,使腰椎不稳,增加了腰椎受损伤的危险,引起腰背痛。而腰背痛亦可反射性抑制脊髓前角运动神经元的兴奋性,引起肌肉萎缩。它们互为因果的关系导致了慢性腰背痛的反复发作。
3.3 小切口椎旁肌间隙入路的优势Villavicencio等[17]报道了在内镜下行此类手术,但常因髂后上棘而不能将套筒放在满意的位置,同时骶骨的斜坡使套筒不能将L5横突附近的软组织隔离而增加了手术的难度。
临床应用小切口经椎旁肌间隙行腰椎后路融合术,具有以下优势:①学习曲线短,熟悉椎旁肌解剖结构后均能很好掌握;②采用小切口可进行直视下操作,调节视野方便,避免了扩张管道配合内窥镜使用时视野范围小且单一、更换视野困难的缺点。③椎弓根螺钉置入时不需要强力拉钩即可充分暴露解剖定位标志,并轻松把握外展角度;④切口小,保留后柱稳定结构,维护脊柱的稳定性;可在小切口内清楚显露上下关节突,行走根及出口根,完成腰椎后路融合术;⑤可两侧交替进行手术,减少对椎旁肌的损伤,尤其是多裂肌及周围韧带的创伤水肿,避免术后腰痛;⑥可不显露椎管后壁的疤痕,在翻修时尤其适用;经济实用,易于推广。⑦可配合自行设计的微型拉钩,相对于价格昂贵的内窥镜及微创扩张管道更适合我国国情,有利于降低患者的医疗费用。
3.4 注意事项术者需正确定位椎旁肌间隙,钝性纵行分离多裂肌与最长肌的肌间隙,进行直视下操作。术中置钉的过程中,不进行上关节突及横突区以外的操作。持续侧向的强力持续牵拉椎旁肌,牵开器每隔40 min~1 h放松1次。置钉过程中“人字嵴”凹内的神经血管束建议使用神经剥离子将其向下牵拉,以减少置钉进程的损伤。行椎弓根固定时需注意保护神经根,如有出血点使用双极电凝止血。最后在肌间隙之间放置纵形连接棒时,特别注意棒的末端圆钝以减少医源性损伤。
| [1] | Zdeblick TA. Laparoscopic spinal fusion[J]. Orthop Clin North Am, 1998, 29(4):635-645. |
| [2] | Wiltse LL, Bateman JG, Hutchinson RH, The paraspinal sacrospinalis-splitting approach to the lumbar spine[J]. J Bone Joint Surg Am, 1968, 50(5):919-926. |
| [3] | Wewers ME, Lowe NK. A critical review of visual analogue scales in the measurement of clinical phenomena[J]. Res Nurs Health, 1990, 13(4):227-236. |
| [4] | Fairbank JC, Pynsent PB. The Oswestry Disability Index[J]. Spine (Phila Pa 1976), 2000, 25(22):2940-2952. |
| [5] | Tsutsumimoto T, Shimogata M, Ohta H, et al. Mini-open versus conventional open posterior lumbar interbody fusion for the treatment of lumbar degenerative spondylolisthesis: comparison of paraspinal muscle damage and slip reduction[J]. Spine (Phila Pa 1976), 2009, 34(18):1923-1928. |
| [6] | Kawaguchi Y, Matsui H, Tsuji H. Back muscle injury after posterior lumbar spine surgery. Part 1: Histologic and histochemical analyses in rats[J]. Spine (Phila Pa 1976), 1994, 19(22):2590-2597. |
| [7] | Wessig C, Koltzenburg M, Reiners K, et al. Muscle magnetic resonance imaging of denervation and reinnervation: correlation with electrophysiology and histology[J]. Exp Neurol, 2004, 185(2):254-261. |
| [8] | Stevens KJ, Spenciner DB, Griffiths KL, et al. Comparison of minimally invasive and conventional open posterolateral lumbar fusion using magnetic resonance imaging and retraction pressure studies[J]. J Spinal Disord Tech, 2006, 19(2):77-86. |
| [9] | Gold GE. Dynamic and functional imaging of the musculoskeletal system[J]. Semin Musculoskelet Radiol, 2003, 7(4):245-248. |
| [10] | Patten C, Meyer RA, Fleckenstein JL. T2 mapping of muscle[J]. Semin Musculoskelet Radiol, 2003, 7(4):297-305. |
| [11] | Sihvonen T, Herno A, Paljrvi L, et al. Local denervation atrophy of paraspinal muscles in postoperative failed back syndrome[J]. Spine (Phila Pa 1976), 1993, 18(5):575-581. |
| [12] | Weiner BK, Walker M, Brower RS, et al. Microdecompression for lumbar spinal canal stenosis[J].Spine (Phila Pa 1976), 1999, 24(21):2268-2272. |
| [13] | Boelderl A, Daniaux H, Kathrein A, et al. Danger of damaging the medial branches of the posterior rami of spinal nerves during a dorsomedian approach to the spine[J]. Clin Anat, 2002, 15(2):77-81. |
| [14] | Burton CV, Kirkaldy-Willis WH, Yong-Hing K, et al. Causes of failure of surgery on the lumbar spine[J]. Clin Orthop Relat Res, 1981 (157):191-199. |
| [15] | Biedermann HJ, Shanks GL, Forrest WJ, et al. Power spectrum analyses of electromyographic activity. Discriminators in the differential assessment of patients with chronic low-back pain[J]. Spine (Phila Pa 1976), 1991, 16(10):1179-1184. |
| [16] | Hides JA, Stokes MJ, Saide M, et al. Evidence of lumbar multifidus muscle wasting ipsilateral to symptoms in patients with acute/subacute low back pain[J]. Spine (Phila Pa 1976), 1994, 19(2):165-172. |
| [17] | Villavicencio AT, Burneikiene S, Bulsara KR, et al. Utility of computerized isocentric fluoroscopy for minimally invasive spinal surgical techniques[J]. J Spinal Disord Tech, 2005, 18(4):369-375. |
 2012, Vol. 10
2012, Vol. 10


