颈椎前路椎间盘切除减压、植骨融合术(anterior cervical discectomy with fusion,ACDF)和颈椎前路椎体次全切除减压、植骨融合术(anterior cervical corpectomy with fusion,ACCF)是治疗颈椎病的经典术式,手术效果好,广泛应用于临床。但是,颈椎前路手术后发生的相关并发症仍不能忽视,如呼吸困难、吞咽困难及喉返神经损伤等。上述并发症中,吞咽困难的发生率较高[1],可>50%,严重影响患者早期恢复及生活质量。吞咽困难具体发生机制尚不明确,可能和局部软组织肿胀相关[2]。本研究通过侧位X线片对颈椎病前路融合术后椎前软组织肿胀进行评估,比较分析单节段和双/多节段颈椎前路融合术后椎前软组织肿胀及吞咽困难的发生率,以期指导临床。
1 资料和方法 1.1 研究对象2013年1~11月因颈椎病于本院行ACDF和/或ACCF的患者,排除翻修手术、前后路联合手术、术前存在吞咽困难的患者,共纳入123例,平均年龄52.3岁(25~75岁),男91例,女32例;其中单节段50例,双节段48例,多节段25例。单节段组50例,男36例,女14例;年龄50.6±11.6岁,其中26例有吸烟史。双/多节段组73例,男55例,女18例;年龄53.5±9.5岁,其中37例有吸烟史。2组一般资料相比,差异无统计学意义(P>0.05)。吞咽困难是患者主观的感觉,本研究中吞咽困难的定义标准参考Bazaz-Yoo吞咽困难评分方法[3],将其分为4级:①无;②轻,吞咽液体食物无障碍,吞咽固体食物几乎没有障碍;③中,吞咽液体食物没有或偶有障碍,吞咽固体食物(仅针对某些特殊食物)常有障碍;④重,吞咽液体食物和固体食物均有障碍。本研究判定中/重症状者为吞咽困难。
1.2 研究方法 1.2.1 椎前软组织肿胀的测量所有患者术前及术后3 d摄颈椎侧位X线片。由于椎前软组织本身厚度较小,在传统的X线片上测量时误差较大。因而本研究应用了PACX影像系统进行测量,测量时首先将图片放大5倍,再应用系统中附带的测距软件进行测量,可以有效降低肉眼测量时产生的误差。测量C2至C7椎前软组织宽度。测量方法:测量每个椎体前下缘至气道阴影后缘的距离;当椎体缘明显增生、骨赘形成时,测量起始点选择在假定的非增生的椎体前下缘;术后X线片中,对于覆盖钛板的椎体,选择相对应的钛板前缘为测量起始点(见图 1)。计算术前术后椎前软组织的宽度变化值,即为椎前软组织肿胀的宽度。每个数据均测量2次,取平均值纳入统计分析。由于C3水平的椎前软组织肿胀最明显,因此选择C3水平进行数据分析。
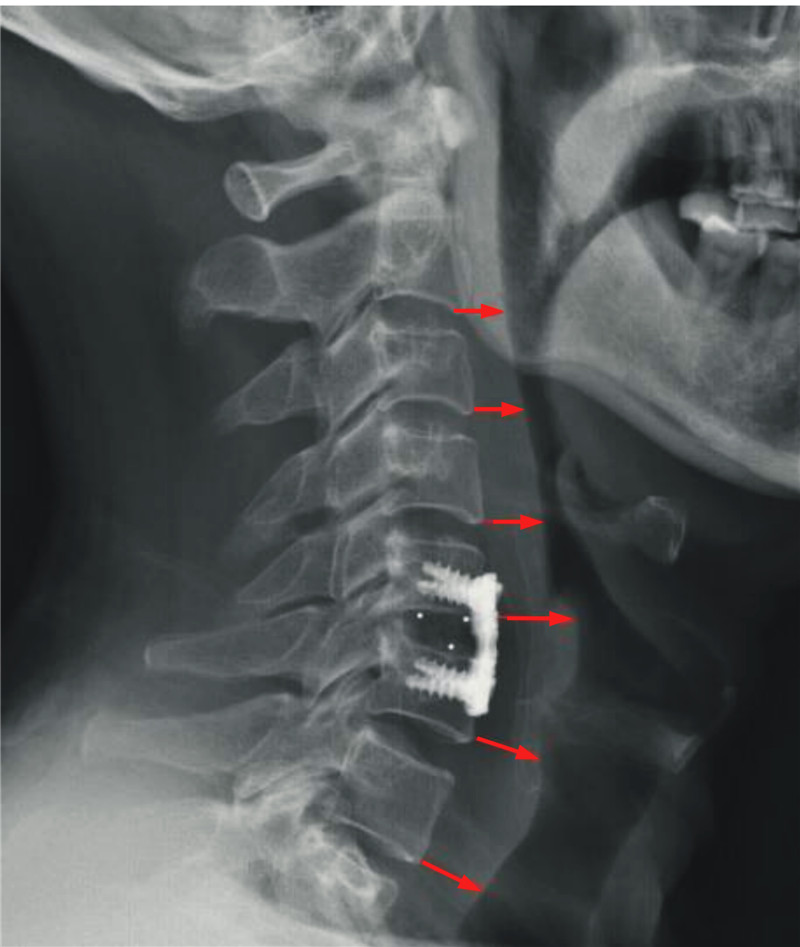 |
红色箭头:椎体前缘至气道后缘的距离 Red arrows:Distance between anterior surface of each vertebral body 图 1 椎前软组织肿胀测量示意图s Fig. 1 Sketch map of prevertebral soft tissue swelling(L1/L2 and L3/L4) |
根据测量结果,对单节段组(n=50)、双节段组(n=48)及多节段组(n=25)术后椎前软组织肿胀数据进行分析。记录并比较分析组间术后吞咽困难的发生率。
手术节段的高低可能是影响术后椎前软组织肿胀的原因之一。根据手术部位高低,将样本分为高位手术组(C4/C5及以上)和低位手术组(C5以下),再进行单节段和双/多节段组间的比较分析。根据测量结果,对比分析各组术后椎前软组织肿胀程度和吞咽困难发生率。
1.3 统计学分析研究结果应用SPSS 13.0统计软件进行分析,组间椎前软组织肿胀程度差异采用方差分析(ANOVA),不同组间吞咽困难发生率比较采用χ2检验,P<0.05时认为差异有统计学意义。
2 结 果术前椎前软组织宽度:C2水平(3.85±1.02) mm,C3水平(4.28±1.04) mm,C4水平(7.2±3.51) mm,C5水平(13.28±3.06) mm,C6水平(13.81±2.64)mm,C7水平(12.67±3.05) mm。术后椎前软组织宽度:C2水平(12.61±4.82) mm,C3水平(14.26±4.96) mm,C4水平(15.79±4.24) mm,C5水平(16.07±3.35) mm,C6水平(16.7±3.18)mm,C7水平(15.63±3.57) mm。椎前软组织肿胀宽度见图 2)。高位颈椎(C2~4)术后椎前软组织肿胀明显,其中C3水平最为明显。在C3水平椎前软组织肿胀宽度平均为9.98 mm。低位颈椎(C5~7)术后椎前软组织肿胀相对不明显,但结果仍有统计学意义(P< 0.05)。
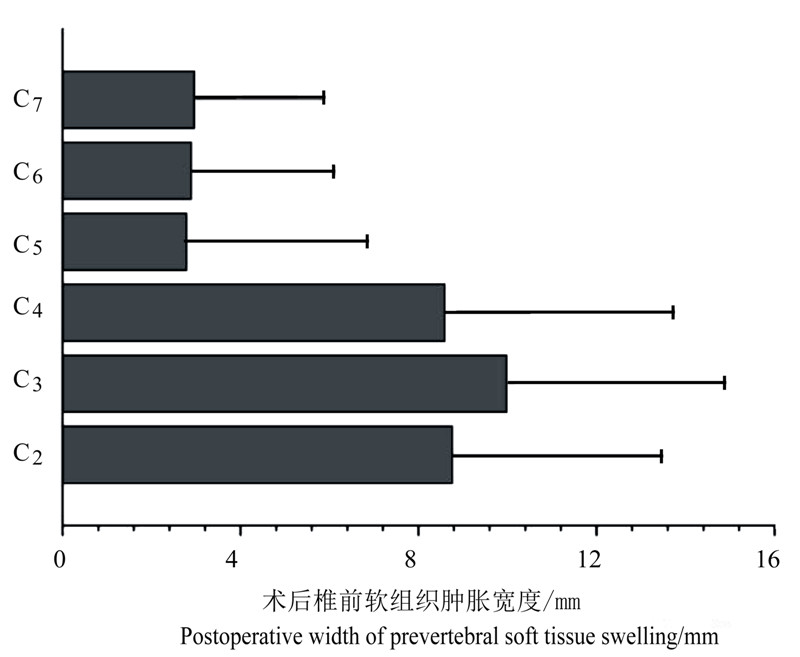 | 图 2 术后C2~7椎前软组织肿胀程度 Fig. 2 Postoperative prevertebral soft tissue swelling from C2-7 |
单节段组术后椎前软组织肿胀宽度及咽困难发生率明显低于双/多节段组,差异有统计学意义(见表 1,P<0.05)。高位手术(C4/C5及以上)及低位手术(C5以下),单节段组术后椎前软组织肿胀宽度及咽困难发生率均明显低于双/多节段组,差异有统计学意义(见表 2,3,P<0.05)。单节段和双节段组内比较,低位手术术后椎前软组织肿胀宽度及咽困难发生率均明显低于高位手术(见表 2,3,P<0.05)。
|
|
表 1 椎前软组织肿胀和吞咽困难发生率 Tab. 1 Postoperative prevertebral soft tissue swelling and dysphagia rate |
|
|
表 2 高位手术后椎前软组织肿胀和吞咽困难发生率 Tab. 2 Postoperative prevertebral soft tissue swelling and dysphagia rate after high-level operation |
|
|
表 3 低位手术后椎前软组织肿胀和吞咽困难发生率 Tab. 3 Postoperative prevertebral soft tissue swelling and dysphagia rate after low-level operation |
椎前软组织肿胀是吞咽困难的可能机制之一[4, 5, 6, 7, 8, 9]。颈椎前路手术时,必须对颈部相关软组织进行剥离和持续牵拉,术后局部充血、水肿,椎前软组织间隙内局部血肿聚积,影像学上可表现为椎前软组织肿胀。术后肿胀的椎前软组织可进一步压迫其前方的咽喉部、食管及气管等结构,进而造成吞咽困难。本研究通过侧位X线对颈椎病颈椎前路融合术后椎前软组织肿胀进行评估,比较分析了单节段和双/多节段颈椎前路融合术后椎前软组织肿胀程度及吞咽困难的发生率。结果提示,单节段组术后椎前软组织肿胀程度和吞咽困难发生率均明显低于双/多节段组。推测可能是由于单节段手术中对软组织剥离、牵拉较少,术后椎前软组织肿胀程度轻,所以单节段手术后吞咽困难的发生率较低。上述结果说明椎前软组织肿胀可能是颈椎前路术后发生吞咽困难的机制之一,而多节段手术可能是术后发生吞咽困难的危险因素。
根据临床观察,多数ACDF和ACCF术后的患者会出现不同程度的椎前软组织肿胀,而通过术后常规X线侧位片即可进行观察和测量。根据软组织充血水肿的病理生理学规律,椎前软组织肿胀的峰值时间位于术后3 d左右,此时颈部软组织处于充血水肿的高峰[10]。随着时间的延长,椎前软组织肿胀将逐渐消退,多数患者在6周后逐渐恢复正常[11]。因此,本研究椎前软组织肿胀的测量时间均选择在术后3 d。
不同颈椎节段的术后椎前软组织肿胀程度可能是不同的。本研究中,C3下缘水平的椎前软组织肿胀最为明显,明显高于低位颈椎。以往的研究认为C5以上的高位颈椎,尤其是C3/C4水平,是椎前软组织肿胀最宽的部位,而C5以下的低位颈椎椎前软组织肿胀相对较小[12]。不同节段颈椎的局部解剖学特点可能是造成上述差异的原因。高位颈椎对应咽部和下咽部,后方潜在的咽后空间相对较大,因此容易发生软组织肿胀。而低位颈椎对应食管、气管,软组织约束多,潜在的腔隙较小,限制了软组织的肿胀程度。因此,手术节段的高低也可能影响椎前软组织肿胀的程度。如果手术节段包含高位颈椎,则术后椎前软组织肿胀的程度可能会增加。因此,本研究中根据手术节段高低将样本分为高位手术组(C4/C5及以上)和低位手术组(C5以下),再进行单节段和双/多节段组间的比较分析,以消除手术部位高低对分析结果的影响。结果显示,无论是高位手术还是低位手术,单节段组术后椎前软组织肿胀程度和吞咽困难发生率均明显低于双/多节段组,进一步说明多节段手术可能是术后发生吞咽困难的相对独立危险因素。
本研究未对术中软组织牵拉进行分析,对各种并发症的分析并未采取量化分析, 因此研究结果具有一定的局限性。本研究结果中,多节段组的椎前软组织肿胀程度和吞咽困难发生率略低于双节段组。多节段手术软组织剥离更广,损伤增加,因此椎前软组织肿胀程度应更高。但多节段组手术切口大,显露充分,术中软组织牵拉相对较小,进而可能降低了术后软组织水肿的程度。上述推测仍需进一步研究证实。后续研究还应根据手术部位高低等其他因素进行分析,进一步阐明颈椎术后椎前软组织肿胀及吞咽困难发生的相关机制及危险因素。
综上所述,对于行颈椎前路融合术的颈椎病患者,多节段手术后椎前软组织肿胀较明显,吞咽困难的发生率较高。多节段手术可能是颈椎前路术后椎前软组织肿胀和吞咽困难发生的危险因素之一,术前针对相关人群的宣教具有一定的必要性和临床意义。
| [1] | Mendoza-Lattes S, Clifford K, Bartelt R, et al. Dysphagia following anterior cervical arthrodesis is associated with continuous, strong retraction of the esophagus[J]. J Bone Joint Surg Am, 2008, 90(2): 256-263. |
| [2] | Riley LH 3rd, Vaccaro AR, Dettori JR, et al. Postoperative dysphagia in anterior cervical spine surgery[J]. Spine (Phila Pa 1976), 2010, 35(9 Suppl):S76-85. |
| [3] | Bazaz R, Lee MJ, Yoo JU. Incidence of dysphagia after anterior cervical spine surgery: a prospective study[J]. Spine (Phila Pa 1976), 2002, 27(22):2453-2458. |
| [4] | Frempong-Boadu A, Houten JK, Osborn B, et al. Swallowing and speech dysfunction in patients undergoing anterior cervical discectomy and fusion: a prospective, objective preoperative and postoperative assessment[J]. J Spinal Disord Tech, 2002, 15(5):362-368. |
| [5] | Martin RE, Neary MA, Diamant NE. Dysphagia following anterior cervical spine surgery[J]. Dysphagia, 1997, 12(1):2-8. |
| [6] | Winslow CP, Winslow TJ, Wax MK. Dysphonia and dysphagia following the anterior approach to the cervical spine[J]. Arch Otolaryngol Head Neck Surg, 2001, 127(1):51-55. |
| [7] | Riley LH 3rd, Skolasky RL, Albert TJ, et al. Dysphagia after anterior cervical decompression and fusion: prevalence and risk factors from a longitudinal cohort study[J]. Spine (Phila Pa 1976), 2005, 30(22):2564-2569. |
| [8] | Fogel GR, McDonnell MF. Surgical treatment of dysphagia after anterior cervical interbody fusion[J]. Spine J, 2005, 5(2):140-144. |
| [9] | Seidl RO, Todt I, Ernst A. Esophagus atresia after cervical spine surgery: case report and literature review[J]. Eur Arch Otorhinolaryngol, 2007, 264(3):291-293. |
| [10] | Suk KS, Kim KT, Lee SH, et al. Prevertebral soft tissue swelling after anterior cervical discectomy and fusion with plate fixation[J]. Int Orthop, 2006, 30(4):290-294. |
| [11] | Sanfilippo JA Jr, Lim MR, Jacoby SM, et al. "Normal" prevertebral soft tissue swelling following elective anterior cervical decompression and fusion[J]. J Spinal Disord Tech, 2006, 19(6):399-401. |
| [12] | Andrew SA, Sidhu KS. Airway changes after anterior cervical discectomy and fusion[J]. J Spinal Disord Tech, 2007, 20(8):577-581. |
 2015, Vol.13
2015, Vol.13 


