乳腺癌是世界上女性最常见的恶性肿瘤之一[1]。随着乳腺癌预后的不断改善,骨转移的发生率也随之升高。流行病学调查提示,约有8%的乳腺癌患者发生骨转移,其中高度恶性患者的骨转移率达到69%[2]。脊柱是乳腺癌骨转移最常发生的部位,约占所有骨转移病例的2/3[3]。与其他脊柱转移的肿瘤相比,乳腺癌患者往往有较长的预期寿命[4]。但由于大多数乳腺癌脊柱转移癌呈溶骨性改变[5],压缩性骨折的发生率也较高[6]。因而乳腺癌脊柱转移更需要尽早的手术治疗,如果出现神经症状再手术减压,则术后神经功能恢复较差[7, 8]。虽然目前的治疗原则仍然是姑息性的,但随着脊柱外科及相关技术的不断进步,患者可以获得更为积极的手术治疗方案。本文就乳腺癌脊柱转移的诊断和外科治疗进展作一综述。
1 诊 断乳腺癌脊柱转移早期往往只表现为非特异性的疼痛,所以很容易被忽视。许多患者首诊时就已出现了神经损伤症状[9]。而神经损伤,特别是下肢肌力减退和马尾综合征严重影响预后[10, 11]。因而,对于新发腰背痛或颈痛,并且有乳腺癌病史的患者,应尽早检查排除脊柱转移可能。由于脊柱退行性病变较少累及胸椎,因而胸背部疼痛的患者更需要高度怀疑[10]。
影像学检查是乳腺癌脊柱转移的主要诊断方法。常用的影像学检查有X线片、计算机X射线断层造影(computed tomography,CT)、放射性核素骨扫描(emission computed tomography,ECT)、核磁共振成像(magnetic resonance imaging,MRI)以及正电子发射断层显像(positron emission tomography-CT,PET-CT)等。X线片和ECT是最常用的筛查方法。X线片只能发现骨质破坏>50%的病灶[12],更适用于诊断成骨性病变,因而对于乳腺癌脊柱转移的溶骨性病变的敏感性并不高。ECT可以显示最小达2 mm的肿瘤病灶[13],因而与X线片相比,ECT可以提早3 ~ 6个月发现转移瘤,敏感性极高[14]。然而ECT显像可能受炎症、感染或者是骨折干扰,而且难以区分具体节段,因而缺乏较高的特异性[11]。
CT可以进一步显示更小的病灶以及肿瘤的侵袭范围。CT还是术前评估骨性解剖结构及脊柱稳定性的重要手段[15]。但有报道显示CT的敏感性只有66%,诊断准确性为89%[16]。
全脊柱MRI是评估神经结构及多节段脊柱转移的首选检查方法[17]。增强的T1像和脂抑像MRI可以进一步显示软组织浸润范围,发现椎管内占位和骨折块等[18]。有研究表明,MRI拥有最高的敏感性(98.5%)和特异性(98.9%),综合准确率达98.7%,是明确手术指征的重要检查[16]。2010年脊柱肿瘤研究组(spine oncology study group,SOSG)提出了用MRI评估脊柱转移癌脊髓受压情况的6点量表[19]。其中0级代表肿瘤局限于椎体内无硬膜外侵犯,而3级(最高级)代表脊髓受压周围脑脊液不可见。2级和3级极有可能导致神经损伤,有外科减压的指征。此外MRI检查结果也可以辅助放疗方案的制定。Husband等[20]报道发现MRI改变53%的患者放疗方法,其中21%为重大调整。
笔者认为由于乳腺癌脊柱转移容易导致病理性骨折、脊髓损伤等严重后果,需要及时选择正确的影像学检查,以便尽早治疗。X线片可以作为最初的检查以发现压缩性骨折和评估脊柱稳定性。对于已出现明显神经症状或X线片结果不明确的患者,应尽量行急诊MRI评估肿瘤浸润范围和骨折块神经压迫程度。对由于禁忌证或受条件限制无法行急诊MRI的患者,应急诊手术以免耽误治疗造成不可逆的神经损伤[20]。
2 治疗方案的确立及手术指征乳腺癌脊柱转移的治疗需要多学科协作,十分复杂。治疗方案的确立可以参照一系列的评分系统。Harrington[21]根据椎体结构的塌陷程度及神经功能的损伤程度首次将肿瘤进行了分级。Tokuhashi等[22]提出了一个评分系统,主要用于脊柱转移肿瘤的术前评估,并在2010年又进行了修订,目前临床运用较为广泛。Tomita等[23]和Bauer等[24]各制定了一套评分系统,主要用于判断预后,进而指导治疗。
预期寿命是决定是否手术治疗的重要因素。一般情况下,如果预期寿命为3 ~ 6个月,更推荐非手术治疗[25]。Tokuhashi等[22]、Tomita等[23]和Bauer等[24]的评分均强调了原发肿瘤类型对于预后评估的重要性,其中乳腺癌患者的预后最佳,有较高的手术指征。然而,Leithner等[26]评估发现现存的脊柱肿瘤评分系统均存在一定的不准确性,临床确定是否手术不能单纯地依靠某一项评分系统,也必须考虑一些其他的因素,比如疼痛程度等。
笔者认为以上3种评分系统并没有对每种原发肿瘤进行单独研究,而且乳腺癌转移病例数较少,因此,可能并不完全适用于乳腺转移癌的患者。近年来,有一些针对性的研究提出了一些需要考虑的影响乳腺癌脊柱转移预后的指标。Sciubba等[27]认为雌激素受体阳性、接受辅助放疗的患者预后较好,而内脏转移或多节段脊柱转移对预后无影响。Chaichana等[7]发现与其他肿瘤相比,乳腺癌颈椎转移发生率偏高。以往有学者认为乳腺癌颈椎转移的患者预后相对较差[27]。但2014年Zadnik等[28]开展的一项回顾性分析显示颈椎转移对预后并没有影响,同时也指出年龄和术前生存质量卡氏体力状况(kanofsky performance status,KPS)评分对乳腺癌脊柱转移患者的术后生存率无明显影响。笔者认为虽然这些结论仍然需要大样本研究的支持,但从一定程度上说明乳腺癌脊柱转移的患者更适于接受积极的手术治疗。
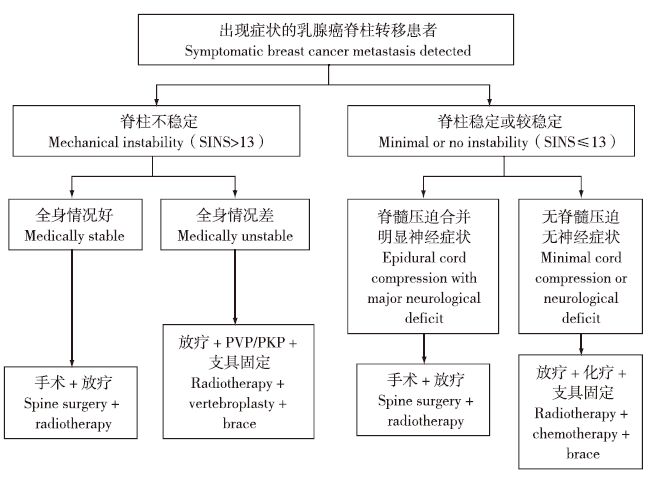
Bilsky等[29]提出了另一个确定治疗方案的方法,主要从4个方面考虑:①神经受累(neurologic factor,N);②原发肿瘤(oncologic factor,O);③脊柱稳定性(mechanical stability,M);④全身情况(systemic disease,S)。其中肿瘤浸润范围可通过Weinstein-Boriani-Biagini(WBB)评分系统评定[17]。而脊柱稳定性可以通过脊柱肿瘤不稳定性评分(spine instability neoplastic score,SINS)评估[30]。基于以上4个方面,有学者总结了一套乳腺癌脊柱转移的推荐治疗方案(见图 1)[27, 31],但准确性仍需要进一步的临床验证。
|
图 1 乳腺癌脊柱转移的推荐治疗方案[27, 31] Fig. 1 Proposed algorithm for treatment of patients with symptomatic spinal metastases from breast cancer[27, 31] |
乳腺癌脊柱转移患者的手术指征始终存在争论,同时由于参考文献不足,还没有相关的循证医学指南。目前普遍接受的手术适应证:①患者预期寿命>3个月;②有进行性加重的神经症状,脊柱不稳定,大剂量放疗无法控制肿瘤生长,或药物无法控制的疼痛等[17]。手术治仍然以姑息性为主,主要目的:①神经减压(75%神经功能恢复);②减轻疼痛(80% ~ 95%);③切除或部分切除肿瘤;④恢复脊柱稳定性,提高生活质量[32]。
3 治疗方法 3.1 非手术治疗药物化疗依然是治疗的主力。内分泌治疗(如选择性雌激素受体调节剂和芳香化酶抑制剂[33])及靶向治疗(如人表皮生长因子受体2抑制剂[34])也被用于治疗乳腺癌脊柱转移患者。糖皮质激素有拮抗乳腺癌肿瘤细胞及减少周围水肿的作用。有报道显示双磷酸盐联合维生素D及钙剂能抑制肿瘤相关的破骨细胞的活性[35]。此外,乳腺癌脊柱转移比其他来源的肿瘤对放疗敏感[4]。放疗可以作为术前、术后有效的辅助治疗。目前已有较为成熟的关于乳腺癌脊柱转移放疗的循证医学指南[36]。
3.2 传统手术方法乳腺癌脊柱转移的手术入路有多种,包括前路、后路、外侧入路或者多种入路联合。具体采用何种入路取决于转移癌的位置、范围及内固定的方式。
有文献报道传统的单纯后路椎板切除减压手术与单纯放疗相比对改善预后并无明显优势[17]。然而,单纯放疗虽然限制了肿瘤的生长,但无法解除神经压迫,因此对于疼痛以及神经压迫症状明显,特别是病灶累及多个节段、需要姑息性减压的患者,手术仍然是较好的选择[11]。2011年Tancioni等[4]报道了23例接受手术减压联合放疗的乳腺癌脊柱转移患者,96%的患者疼痛完全缓解,所有患者神经症状明显改善,并且保持至最后死亡或肿瘤复发。
乳腺癌脊柱转移大多局限于椎体,极少侵犯附件等后柱结构[17],因此前路椎体切除术提供了到达病灶的最佳途径,可以最大程度地进行肿瘤切除与脊髓减压,同时与后路单纯减压相比更能重建脊柱的稳定性[37],适用于位于WBB分区4 ~ 8区或5 ~ 9区的转移病灶。如果肿瘤侵犯后方结构,则需联合后路手术以较彻底地切除肿瘤、加强脊柱稳定性。但前后路手术由于手术时间长、切口大、范围广,术后并发症较多,因而只适用于一般情况较好的患者。2007年,Shehadi等[31]报道了接受大范围肿瘤切除减压及脊柱内固定的乳腺癌脊柱转移患者87例,术前神经损伤较轻的患者术后神经功能恢复正常76例;术前丧失行走功能的患者11例,术后可正常行走3例。此外术后疼痛明显改善,平均视觉模拟量表(visual analog scale,VAS)评分由术前6分降至2分。2011年,Chung等[38]报道了15例大范围肿瘤切除减压的病例,56%的患者术后神经症状明显改善,并且未复发。
3.3 全脊椎整块切除术(total enblocspondylectomy,TES)随着肿瘤血管栓塞术、内固定等相关技术的迅速发展,对乳腺癌脊柱转移的治疗理念正在由姑息向积极转变。与传统手术相比,TES可以通过在无肿瘤侵犯部位的截骨达到最大限度地对转移癌的整块切除[28, 39]。目前还没有针对乳腺癌脊柱转移患者接受TES手术疗效的报道。但在一些关于其他原发肿瘤研究中,TES与传统的分块切除手术比较,两者术后生存率差异无统计学意义,但局部复发率TES明显较低[40]。因而对于孤立或局限的转移灶,原发病灶治疗有效、预计生存期>6个月的患者,TES是理想的手术方案[41]。但单纯后路的TES也存在着许多争议,特别是腰椎部位的转移癌。由于腰椎椎体较大,低位腰椎还有两侧髂骨遮挡,神经根损伤等并发症较易发生,同时长距离重建难度大,往往需要联合前路手术。
3.4 微创技术近年来有报道新的微创技术治疗乳腺癌脊柱转移,手术效果良好,同时术中出血量、手术时间和术后并发症发生率明显降低[42]。其中最突出的治疗方法是经皮椎体成形术(percutaneous vertebroplasty,PVP)和经皮椎体后凸成形术(percutaneous kyphoplasty,PKP)[43]。PVP是在X线透视或CT引导下注入聚甲基丙烯酸甲酯(polymethylmethacrylate,PMMA)骨水泥,通过PMMA骨水泥在固化过程中释放的热量使肿瘤组织坏死。此外PMMA骨水泥还可以稳定前柱结构,防止进一步压缩性骨折,同时毁损神经末梢,以缓解疼痛。PKP与PVP类似,区别是预先在椎体内置入一个球囊,一方面降低注入骨水泥时的阻力,另一方面可以恢复椎体高度纠正后凸畸形[11, 44]。2008年,Lee等[45]报道了一项关于接受PKP治疗的脊柱转移癌患者的回顾性研究,其中8例原发肿瘤为乳腺癌的患者术后疼痛均立刻缓解,镇痛剂需求量明显下降。一般PKP常用于胸腰椎转移肿瘤,Druschel等[46]报道了1例前路PKP治疗多节段颈椎乳腺癌转移的病例,获得了不错的术后疗效。最近Papp等[47]也报道了10例经口入路椎体成形术联合后路枕颈固定治疗C2乳腺癌转移患者,也获得了不错的术后疗效。
综上所述,随着乳腺癌生存率的不断提高,骨转移的发生不容忽视。脊柱是乳腺癌骨转移最常见的部位。细致的病史询问、体格检查及影像学检查是早期诊断的必要条件。由于乳腺癌脊柱转移有独特的组织学特点和预后转归,因此在治疗方案的确立上和其他原发肿瘤不同。手术治疗的目的主要包括保护神经功能、维持脊柱稳定性、减轻疼痛等。虽然目前的治疗原则仍然是姑息性的,但随着脊柱外科及相关技术的不断进步,患者可以接受更为积极的手术方案。然而,各种手术的疗效评估还需要多中心大样本的临床研究。此外,针对乳腺癌脊柱转移的特定评估和治疗方案也有待建立。
| [1] | DeSantis C,Ma J,Bryan L,et al. Breast cancer statistics,2013[J]. CA Cancer J Clin,2014,64(1):52-62. |
| [2] | Lu X,Kang Y. Organotropism of breast cancer metastasis[J]. J Mammary Gland Biol Neoplasia,2007,12(2-3):153-162. |
| [3] | Briasoulis E,Karavasilis V,Kostadima L,et al. Metastatic breast carcinoma confined to bone:portrait of a clinical entity[J]. Cancer,2004,101(7):1524-1528. |
| [4] | Tancioni F,Navarria P,Mancosu P,et al. Surgery followed by radiotherapy for the treatment of metastatic epidural spinal cord compression from breast cancer[J]. Spine(Phila Pa 1976),2011,36(20):E1352-1359. |
| [5] | Suva LJ,Griffin RJ,Makhoul I. Mechanisms of bone metastases of breast cancer[J]. Endocr Relat Cancer,2009,16(3):703-713. |
| [6] | Saarto T,Vehmanen L,Blomqvist C,et al. Ten-year follow-up of 3 years of oral adjuvant clodronate therapy shows significant prevention of osteoporosis in early-stage breast cancer[J]. J Clin Oncol,2008,26(26):4289-4295. |
| [7] | Chaichana KL,Pendleton C,Sciubba DM,et al. Outcome following decompressive surgery for different histological types of metastatic tumors causing epidural spinal cord compression. Clinical article[J]. J Neurosurg Spine,2009,11(1):56-63. |
| [8] | Chaichana KL,Woodworth GF,Sciubba DM,et al. Predictors of ambulatory function after decompressive surgery for metastatic epidural spinal cord compression[J]. Neurosurgery,2008,62(3):683-692. |
| [9] | Levack P,Graham J,Collie D,et al. Don't wait for a sensory level-listen to the symptoms:a prospective audit of the delays in diagnosis of malignant cord compression[J]. Clin Oncol(R Coll Radiol),2002,14(6):472-480. |
| [10] | Quraishi NA,Gokaslan ZL,Boriani S. The surgical management of metastatic epidural compression of the spinal cord[J]. J Bone Joint Surg Br,2010,92(8):1054-1060. |
| [11] | Kaloostian PE,Zadnik PL,Etame AB,et al. Surgical management of primary and metastatic spinal tumors[J]. Cancer Control,2014,21(2):133-139. |
| [12] | Schirrmeister H. Detection of bone metastases in breast cancer by positron emission tomography[J]. Radiol Clin North Am,2007,45(4):669-676. |
| [13] | Costelloe CM,Rohren EM,Madewell JE,et al. Imaging bone metastases in breast cancer:techniques and recommendations for diagnosis[J]. Lancet Oncol,2009,10(6):606-614. |
| [14] | Marulanda GA,Mont MA,Lucci A,et al. Orthopedic surgery implications of breast cancer[J]. Expert Rev Anticancer Ther,2008,8(6):949-956. |
| [15] | Hamaoka T,Madewell JE,Podoloff DA,et al. Bone imaging in metastatic breast cancer[J]. J Clin Oncol,2004,22(14):2942-2953. |
| [16] | Buhmann Kirchhoff S,Becker C,Duerr HR,et al. Detection of osseous metastases of the spine:comparison of high resolution multi-detector-CT with MRI[J]. Eur J Radiol,2009,69(3):567-573. |
| [17] | Sciubba DM,Petteys RJ,Dekutoski MB,et al. Diagnosis and management of metastatic spine disease. A review[J]. J Neurosurg Spine,2010,13(1):94-108. |
| [18] | Khanna AJ,Shindle MK,Wasserman BA,et al. Use of magnetic resonance imaging in differentiating compartmental location of spinal tumors[J]. Am J Orthop(Belle Mead NJ),2005,34(10):472-476. |
| [19] | Bilsky MH,Laufer I,Fourney DR,et al. Reliability analysis of the epidural spinal cord compression scale[J]. J Neurosurg Spine,2010,13(3):324-328. |
| [20] | Husband DJ,Grant KA,Romaniuk CS. MRI in the diagnosis and treatment of suspected malignant spinal cord compression[J]. Br J Radiol,2001,74(877):15-23. |
| [21] | Harrington KD. Metastatic disease of the spine[J]. J Bone Joint Surg Am,1986,68(7):1110-1115. |
| [22] | Tokuhashi Y,Matsuzaki H,Oda H,et al. A revised scoring system for preoperative evaluation of metastatic spine tumor prognosis[J]. Spine(Phila Pa 1976),2005,30(19):2186-2191. |
| [23] | Tomita K,Kawahara N,Kobayashi T,et al. Surgical strategy for spinal metastases[J]. Spine(Phila Pa 1976),2001,26(3):298-306. |
| [24] | Bauer H,Tomita K,Kawahara N,et al. Surgical strategy for spinal metastases[J]. Spine(Phila Pa 1976),2002,27(10):1124-1126. |
| [25] | White BD,Stirling AJ,Paterson E,et al. Diagnosis and management of patients at risk of or with metastatic spinal cord compression:summary of NICE guidance[J]. BMJ,2008,337:a2538. |
| [26] | Leithner A,Radl R,Gruber G,et al. Predictive value of seven preoperative prognostic scoring systems for spinal metastases[J]. Eur Spine J,2008,17(11):1488-1495. |
| [27] | Sciubba DM,Gokaslan ZL,Suk I,et al. Positive and negative prognostic variables for patients undergoing spine surgery for metastatic breast disease[J]. Eur Spine J,2007,16(10):1659-1667. |
| [28] | Zadnik PL,Hwang L,Ju DG,et al. Prolonged survival following aggressive treatment for metastatic breast cancer in the spine[J]. Clin Exp Metastasis,2014,31(1):47-55. |
| [29] | Bilsky M,Smith M. Surgical approach to epidural spinal cord compression[J]. Hematol Oncol Clin North Am,2006,20(6):1307-1317. |
| [30] | Fourney DR,Frangou EM,Ryken TC,et al. Spinal instability neoplastic score:an analysis of reliability and validity from the spine oncology study group[J]. J Clin Oncol,2011,29(22):3072-3077. |
| [31] | Fourney DR,Frangou EM,Ryken TC,et al. Spinal instability neoplastic score:an analysis of reliability and validity from the spine oncology study group[J]. J Clin Oncol,2011,29(22):3072-3077. |
| [32] | Bhatt AD,Schuler JC,Boakye M,et al. Current and emerging concepts in non-invasive and minimally invasive management of spine metastasis[J]. Cancer Treat Rev,2013,39(2):142-152. |
| [33] | Morandi P,Rouzier R,Altundag K,et al. The role of aromatase inhibitors in the adjuvant treatment of breast carcinoma:the M. D. Anderson Cancer Center evidence-based approach[J]. Cancer,2004,101(7):1482-1489. |
| [34] | Jelovac D,Emens LA. HER2-directed therapy for metastatic breast cancer[J]. Oncology(Williston Park),2013,27(3):166-175. |
| [35] | Addison CL,Pond GR,Zhao H,et al. Effects of de-escalated bisphosphonate therapy on bone turnover biomarkers in breast cancer patients with bone metastases[J]. Springerplus,2014,3:577. |
| [36] | Souchon R,Wenz F,Sedlmayer F,et al. DEGRO practice guidelines for palliative radiotherapy of metastatic breast cancer:bone metastases and metastatic spinal cord compression(MSCC)[J]. Strahlenther Onkol,2009,185(7):417-424. |
| [37] | Molina CA,Gokaslan ZL,Sciubba DM. Diagnosis and management of metastatic cervical spine tumors[J]. Orthop Clin North Am,2012,43(1):75-87. |
| [38] | Chung C,Srikun D,Lim CS,et al. A two-photon fluorescent probe for ratiometric imaging of hydrogen peroxide in live tissue[J]. Chem Commun(Camb),2011,47(34):9618-9620. |
| [39] | Tomita K,Toribatake Y,Kawahara N,et al. Total en bloc spondylectomy and circumspinal decompression for solitary spinal metastasis[J]. Paraplegia,1994,32(1):36-46. |
| [40] | Li H,Gasbarrini A,Cappuccio M,et al. Outcome of excisional surgeries for the patients with spinal metastases[J]. Eur Spine J,2009,18(10):1423-1430. |
| [41] | Murakami H,Kawahara N,Demura S,et al. Total en bloc spondylectomy for lung cancer metastasis to the spine[J]. J Neurosurg Spine,2010,13(4):414-417. |
| [42] | Molina CA,Gokaslan ZL,Sciubba DM. A systematic review of the current role of minimally invasive spine surgery in the management of metastatic spine disease[J]. Int J Surg Oncol,2011,2011:598148. |
| [43] | Chen KY,Ma HI,Chiang YH. Percutaneous transpedicular vertebroplasty with polymethyl methacrylate for pathological fracture of the spine[J]. J Clin Neurosci,2009,16(10):1300-1304. |
| [44] | Anselmetti GC,Manca A,Kanika K,et al. Temperature measurement during polymerization of bone cement in percutaneous vertebroplasty:an in vivo study in humans[J]. Cardiovasc Intervent Radiol,2009,32(3):491-498. |
| [45] | Lee B,Franklin I,Lewis JS,et al. The efficacy of percutaneous vertebroplasty for vertebral metastases associated with solid malignancies[J]. Eur J Cancer,2009,45(9):1597-1602. |
| [46] | Druschel C,Schaser KD,Melcher I,et al. Minimally invasive combined anterior kyphoplasty for osteolytic C2 and C5 metastases[J]. Arch Orthop Trauma Surg,2011,131(7):977-981. |
| [47] | Papp Z,Marosfői M,Szikora I,et al. Treatment of C-2 metastatic tumors with intraoperative transoral or transpedicular vertebroplasty and occipitocervical posterior fixation[J]. J Neurosurg Spine,2014,21(6):886-891. |
 2016, Vol.14
2016, Vol.14 


