颈椎前路椎间盘切除减压融合术(ACDF)在治疗颈椎病方面一直是“金标准”,但是融合导致相邻椎间隙退变加速[1-2]。颈人工椎间盘置换术(CTDR)能在解除神经压迫的同时保留生理活动功能,理论上比ACDF更适合治疗颈椎病,近期疗效较为满意,但术后后凸畸形、异位骨化等并发症时有报道[3-7]。自CTDR用于治疗颈椎病以来,相继有Bryan、Prodisc-C和Prestige等假体应用于临床。近年Discover假体进入临床并逐步得到广泛应用。为探讨其临床疗效,本院2009年1月—2011年10月,共收治单节段颈椎病患者81例,采用ACDF或CTDR治疗并获得 > 4年的随访,现将随访结果报告如下。
1 资料和方法 1.1 一般资料病例纳入标准:①单纯颈椎椎间盘退变、椎间盘突出或局限性骨赘形成导致颈脊髓和/或神经根压迫的单节段颈椎病患者,无明确外伤史或其他神经压迫因素(如后纵韧带骨化等)存在,无骨质疏松症、结缔组织疾病或癌症等系统性重大疾病。②随访 > 4年。③考虑到术后患者随访的依从性、颈椎功能障碍指数(NDI)[8]中所从事工作等社会功能的评估以及排除年龄相关性骨质疏松发生,选择患者年龄男≤50岁,女≤45岁。④动力位X线片示病变节段上下终板成角变化 < 11°,终板前后移位 < 3 mm;终板光滑,无毛糙、缺损等征象;MRI检查未见终板Modic病变。⑤术前日本骨科学会(JOA)[9]评分≥8分。采用CTDR治疗者41例,采用ACDF治疗者40例,所有手术均由同一位高年资主任医师完成,两组患者术前一般情况差异无统计学意义(P > 0.05,表 1),具有可比性。
|
|
表 1 一般资料 Table 1 General data |
ACDF组患者取仰卧位,全身麻醉后予颈部垫软枕保持后伸,常规取右侧颈前横切口,逐层切开皮肤、皮下组织、颈阔肌及深筋膜,纵向钝性分离颈内脏鞘和颈血管鞘并分别牵向内外两侧,显露椎前筋膜,经C形臂X线机透视示定位无误后,尖刀切除前纵韧带及椎间盘纤维环前部,用枪式咬骨钳及刮勺交替清除全部纤维环、上下软骨终板、后纵韧带、椎体后缘增生骨赘及双侧小部分钩椎关节。彻底减压完毕后,在减压间隙置入填满自体骨的椎间融合器进行支撑,并用钛板(Slim-loc,DePuy Spine,美国)固定。用生理盐水冲洗后进行创面止血,伤口内留置橡皮引流管,逐层缝合切口。
CTDR组患者取仰卧位,全身麻醉后保持颈椎自然中立位,切忌颈椎过伸位,因为Discover假体(DePuy Spine,美国)自身带有7°的前凸角且不具备椎间盘稳定性,术后由过伸位恢复至中立位时易出现假体上位终板前滑移位或上下终板间成角。手术显露、减压方法及过程与单间隙ACDF一致,达到充分减压目的后尽量保留全部终板。减压后骨创面采用骨蜡涂抹止血,假体的安置严格遵循Discover操作流程。
1.3 评价指标术后第1、3、6、12、24个月及以后逐年定期随访。采用JOA评分和NDI综合评估颈椎术后患者功能恢复。考虑到有患者NDI中一些项目的评分并不理想,但却认为该项功能的恢复已经不影响独立生活,因此本研究在每项后面另设一条问卷项目,即“该项功能术后几周后不影响您日常生活”,进一步评价患者独立生活能力恢复情况。
患者在术前及术后各随访时间点行颈椎正侧位、左右屈曲正位、过屈过伸侧位X线检查,测量手术节段、上下邻近节段活动度(ROM)以及C2~7 Cobb角,ROM为该间隙过伸位和过屈位的角度之差。并采用McAfee分级[10]评定CTDR术后异位骨化情况。
1.4 统计学处理使用SPSS 17.0软件对数据进行统计学分析。术前和术后各随访时间点JOA评分、NDI、上下邻近节段ROM以及C2~7 Cobb角组内比较使用方差分析,组间对比使用重复测量设计资料的方差分析,以P < 0.05为差异有统计学意义。
2 结果术中可见各手术节段椎间隙不同程度退变且椎体高度下降,椎间盘髓核突出压迫脊髓和/或相应的神经根,所有患者终板均较为光滑,轻度增生,与术前X线所见一致。人工椎间盘置入顺利,术中C形臂X线机透视下见人工椎间盘位置良好。所有患者围手术期使用抗生素1~2次,术后3 d内使用甲泼尼龙、呋塞米(速尿)抗炎消肿,颈部伤口留置引流管,于术后1~2 d拔除,术后24 h可以下床活动。CTDR组术后口服非甾体类抗炎药物2周,颈托保护1周;ACDF组颈托保护3个月。
2.1 功能改善情况两组术后各时间点JOA评分与术前相比均有明显改善,差异有统计学意义(P < 0.05,表 2),术后6个月及以后随访时JOA评分无进一步改善。各时间点JOA评分组间比较差异无统计学意义(P > 0.05,表 2)。
|
|
表 2 2组各时间点JOA评分 Table 2 JOA scores of 2 groups at each time point |
两组术后各时间点NDI与术前相比均有明显改善,差异有统计学意义(P < 0.05,表 3),术后6个月及以后随访时NDI无进一步改善。两组间术前、术后6个月及末次随访时NDI差异无统计学意义(P > 0.05),术后1个月两组间NDI差异有统计学意义(P < 0.05,表 3),CTDR组优于ACDF组;NDI中各项功能的恢复不影响其独立生活的时间,CTDR组为(1.8±0.6)周,较ACDF组的(2.7±1.5)周明显缩短,差异有统计学意义(P < 0.05);进一步分析颈部功能差异主要表现在工作、驾车和娱乐3个项目,CTDR组均优于ACDF组,差异有统计学意义(P < 0.05,表 3)。
|
|
表 3 2组各时间点NDI Table 3 NDI of 2 groups at each time point |
在上、下邻近节段ROM和C2~7 Cobb角方面,CTDR组术前、术后变化不明显;ACDF组上位邻近节段ROM术后明显增加,C2~7 Cobb角术后明显减小,与术前相比差异均有统计学意义(P < 0.05,表 4)。两组间术前上、下邻近节段ROM以及C2~7 Cobb角差异无统计学意义(P > 0.05,表 4);术后6个月及末次随访时CTDR组与ACDF组相比,上位邻近节段ROM及C2~7 Cobb角差异有统计学意义(P < 0.05,表 4)。
|
|
表 4 2组各时间点邻近节段ROM和C2~7 Cobb角 Table 4 ROM between adjacent segments and C2-7 Cobb's angle of 2 groups at each time point |
CTDR组术后1年有5例患者出现异位骨化,其中Ⅰ级4例,Ⅱ级1例;术后2年有13例出现异位骨化,其中Ⅰ级8例,Ⅱ级5例;末次随访时有15例出现异位骨化,其中Ⅰ级3例,Ⅱ级11例,Ⅲ级1例。CTDR组中有2例患者出现假体轻度下沉,均为上位假体终板上陷。1例出现C5椎体前下缘骨赘吸收,但JOA评分、NDI均无明显变化(图 1)。ACDF组中无椎间融合器下沉、植骨不愈合、畸形愈合、内固定松动断裂等并发症发生。所有患者无术后创口内血肿形成、神经损伤加重、喉返神经或气管食管损伤等并发症发生。随访期内无再次颈椎手术者。
|
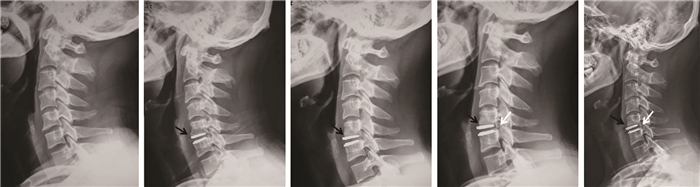
a:术前 b:术后2 d c:术后6个月可见C5椎体前下缘骨赘明显吸收 d:术后2年上终板界面轻度吸收 e:术后4年时假体轻度下沉并局部异位骨化 a:Pre-operation b:Postoperative 2 d c:Roentgenograph at postoperative 6 months shows absorption of C5 antero-inferior border osteophytes d:Roentgenograph at postoperative 2 years shows mild absorption of upper endplate interface e:Roentgenograph at postoperative 4 years shows prosthesis mild sinking and heterotopic ossification 图 1 CTDR组骨赘吸收及异位骨化患者影像学资料 Figure 1 Imaging data of a typical case in CTDR group with osteophyte absorption and heterotopic ossification |
近年来,随着社会发展和技术进步,CTDR在临床应用逐步增加。作为治疗颈椎病的一种新型非融合手术方式,CTDR有其严格的指征、操作步骤和适宜人群,以此为前提,其临床疗效才能得到正确评价。CTDR能有效改善脊髓神经功能[3-4],部分学者报道其改善神经功能效果等同甚至优于ACDF[11-12]。虽然在术后近期随访获得较为满意的临床效果,但颈椎后凸畸形和人工椎间盘周围异位骨化甚至置换节段自发性融合等并发症报道也并不少见[5-7, 13],以上并发症的发生违背了对椎间盘进行置换的目的与初衷,进一步发展可能导致手术节段ROM下降、假体移位等问题。并发症的发生与相应人工椎间盘的设计、复杂的手术操作过程以及适应证的选择有关,因此颈人工椎间盘的设计和操作一直在不断改进和完善。
Discover颈人工椎间盘是DePuy Spine于2007年推出的球-窝型颈人工椎间盘假体,与Prestige等半限制型颈人工椎间盘相比,其允许屈、伸、侧屈和轴向旋转等各个方向的活动,更接近颈椎椎间盘的生理运动。此外,Discover颈人工椎间盘在矢状位存在7°的前凸角,更适于手术节段生理曲度的维持,较为简便的手术操作可能会使其更容易在临床上推广应用。目前对Discover假体治疗颈椎病的临床研究表明,患者NDI、疼痛视觉模拟量表(VAS)评分、JOA评分均得到明显改善,颈椎的生理曲度可恢复,颈椎ROM得以保留[14]。而且一些学者通过CTDR与ACDF进行比较,发现CTDR可获得更为满意的疗效[15-16]。本研究发现,CTDR与ACDF对脊髓神经功能JOA评分的改善并无明显差异,可能原因:①两组患者术前神经功能无明显差异,未将脊髓信号改变的患者纳入研究范围;②两组患者的减压方式相同;③两组患者术后治疗和功能锻炼相同。由此提示,颈椎病患者术后脊髓神经功能的恢复取决于术中减压是否彻底,而不是手术方式。
术后1个月CTDR组的NDI较ACDF组改善明显。进一步分析,NDI改善明显项目为工作、驾车和娱乐3个方面,颈部疼痛、头痛、自我照顾、提重物、阅读、注意力集中及睡眠等7项并无明显差别。而且CTDR组患者认为NDI各项功能恢复至不影响其日常生活的时间也明显短于ACDF组,原因可能是ACDF组颈托固定时间长于CTDR组,这也从侧面反映接受CTDR治疗的患者术后的独立生活能力更能快速地改善和恢复。术后康复时间缩短、早日恢复正常工作,对白领等有特殊职业要求的从业者显得尤为重要。有文献报道CTDR较ACDF在改善颈部疼痛(VAS评分)方面更加有效[17]。本研究结果显示术后6个月及末次随访时两组患者NDI差异并不明显,但均较术前得到明显改善。颈椎退行性疾患的颈部疼痛与颈部生理弧度、颈椎稳定性及神经受压有关,本研究中患者颈部疼痛改善原因:①术中脊髓和神经根均得到充分减压;②术后生理弧度均较术前得到明显改善;③术前过伸、过屈位均未发现颈椎不稳定表现。Discover颈人工椎间盘为非限制型假体,自身设计并不具备稳定椎间隙功能,颈椎不稳引起的颈痛不宜采用CTDR治疗。
CTDR对相邻节段ROM无明显影响,而ACDF却能增加相邻椎节段ROM,相邻椎间隙ROM的增大提示该椎间盘具有更大的运动负荷[18-19]。本研究中CTDR组上下相邻节段ROM术后增加均不明显,而ACDF组上位相邻节段ROM增加明显,说明CTDR较ACDF更利于保护相邻椎间隙的功能。在C2~7 Cobb角方面,CTDR组术后变化不明显,ACDF组较术前减小,这与颈椎局部节段融合有关。
异位骨化是CTDR术后常见的并发症,严重的异位骨化可导致置换节段融合。异位骨化发生在颈人工椎间盘周围,侧位X线片能观察到假体前方、间隙及后方密度增高,随访12个月时异位骨化发生率为17.8%~71.4%[7, 13]。Tu等[20]报道如果进一步用CT扫描进行评估,异位骨化的发生率可能更高。异位骨化确切发生机制尚不清楚,可能与基因差异、术中组织损伤、终板边缘骨赘切除、假体种类等因素有关。有学者认为术前严格把握手术适应证,选择退变程度较低的节段进行置换可以减少异位骨化的发生[21]。应用Discover假体进行CTDR后出现异位骨化的报道并不多见,在术后 > 12个月的随访中发生率也普遍较低。Coric等[15]报道随访24个月的16例患者中发现异位骨化1例,Du等[14]报道获得12~18个月随访的23例患者中未发现异位骨化。但本组获得4年随访的CTDR组患者总共有15例出现异位骨化,大部分为Ⅰ级和Ⅱ级,并呈现出随着随访时间的增加而增加的趋势。但即便是Ⅲ级骨化,人工椎间盘活动严重受限者,伴随骨化的产生,患者并未感觉明显不适,对临床疗效未产生影响。这说明接受CTDR治疗者即使在长期随访中由于异位骨化等原因而失去活动范围,但在中期随访中运动范围可保留、相邻节段得到保护,所以置换可以作为融合的一种替代选择,其临床效果至少不低于融合术。
在本组研究中CTDR组有2例患者上位终板假体出现轻度下沉,可能与假体上位终板骨接触面吸收有关。1例患者出现C5椎体前下缘骨赘吸收,原因尚不清楚,文献报道中未见Discover假体下沉及相邻椎体边缘骨赘吸收的报道,其他种类颈人工椎间盘的相关报道也少见,有待于临床随访继续观察分析。
综上所述,CTDR操作简便、手术创伤小,在严格掌握手术适应证的情况下,治疗单节段颈椎病疗效满意,尤其在早期改善患者的生活质量上较ACDF有着明显的优势。经过 > 4年的中期随访,虽然随着随访时间延长出现了较高的异位骨化发生率,但仍能较好地维持置换节段生理曲度和手术节段各方向ROM,起到保护邻近节段的作用。
| [1] | Eck JC, Humphreys SC, Lim TH, et al. Biomechanical study on the effect of cervical spine fusion on adjacentlevel intradiscal pressure and segmental motion[J]. Spine (Phila Pa 1976), 2002, 27(22): 2431–2434. DOI:10.1097/00007632-200211150-00003 |
| [2] | Matsunaga S, Kabayama S, Yamamoto T, et al. Strain on intervertebral discs after anterior cervical decompression and fusion[J]. Spine (Phila Pa 1976), 1999, 24(7): 670–675. DOI:10.1097/00007632-199904010-00011 |
| [3] | Phillips FM, Allen TR, Regan JJ, et al. Cervical disc replacement in patients with and without previous adjacent level fusion surgery: a prospective study[J]. Spine (Phila Pa 1976), 2009, 34(6): 556–565. DOI:10.1097/BRS.0b013e31819b061c |
| [4] | 肖嵩华, 王岩, 王征, 等. 人工颈椎椎间盘置换治疗单节段颈椎病的前瞻性随机对照研究[J]. 脊柱外科杂志, 2011, 9(5): 263–267. |
| [5] | Sasso RC, Metcalf NH, Hipp JA, et al. Sagittal alignment after Bryan cervical arthroplasty[J]. Spine (Phila Pa 1976), 2011, 36(13): 991–996. DOI:10.1097/BRS.0b013e3182076d70 |
| [6] | 蒋涛, 任先军, 王卫东, 等. Bryan人工颈椎椎间盘置换术后中长期临床疗效及相关问题分析[J]. 脊柱外科杂志, 2011, 9(5): 268–272. |
| [7] | Yi S, Kim KN, Yang MS, et al. Difference in occurrence of heterotopic ossification according to prosthesis type in the cervical artificial disc replacement[J]. Spine (Phila Pa 1976), 2010, 35(16): 1556–1561. DOI:10.1097/BRS.0b013e3181c6526b |
| [8] | Vernon H, Mior S. The neck disability index: a study of reliability and validity[J]. J Manipulative Physiol Ther, 1991, 14(7): 409–415. |
| [9] | Yonenobu K, Wada E, Tanaka T, et al. Japanese Orthopaedic Association Cervical Myelopathy Evaluation Questionnaire (JOACMEQ): Part 2. Endorsement of the alternative item[J]. J Orthop Sci, 2009, 12(3): 241–248. |
| [10] | McAfee PC, Yuan HA, Fredrickson BE, et al. The value of computed tomography in thoracolumbar fractures. An analysis of one hundred consecutive cases and a new classification[J]. J Bone Joint Surg Am, 1983, 65(4): 461–473. DOI:10.2106/00004623-198365040-00006 |
| [11] | Heller JG, Sasso RC, Papadopoulos SM, et al. Comparison of BRYAN cervical disc arthroplasty with anterior cervical decompression and fusion: clinical and radiographic results of a randomized, controlled, clinical trial[J]. Spine (Phila Pa 1976), 2009, 34(2): 101–107. DOI:10.1097/BRS.0b013e31818ee263 |
| [12] | 张雪松, 张永刚, 肖嵩华, 等. 单节段人工椎间盘置换治疗颈椎病的中长期疗效[J]. 中国脊柱脊髓杂志, 2012, 22(10): 879–883. DOI:10.3969/j.issn.1004-406X.2012.10.05 |
| [13] | Heidecke V, Burkert W, Brucke M, et al. Intervertebral disc replacement for cervical degenerative disease-clinical results and functional outcome at two years in patients implanted with the Bryan cervical disc prosthesis[J]. Acta Neurochir (Wien), 2008, 150(5): 453–459. DOI:10.1007/s00701-008-1552-7 |
| [14] | Du J, Li M, Liu H, et al. Early follow-up outcomes after treatment of degenerative disc disease with the discover cervical disc prosthesis[J]. Spine J, 2012, 11(4): 281–289. |
| [15] | Coric D, Cassis J, Carew JD, et al. Prospective study of cervical arthroplasty in 98 patients involved in 1 of 3 separate investigational device exemption studies from a single investigational site with a minimum 2-year followup[J]. J Neurosurg Spine, 2010, 13(6): 715–721. DOI:10.3171/2010.5.SPINE09852 |
| [16] | Skeppholm M, Lindgren L, Henriques T, et al. The discover artificial disc replacement versus fusion in cervical radiculopathy-a randomized controlled outcome trial with 2-year follow-up[J]. Spine J, 2015, 15(6): 1284–1294. DOI:10.1016/j.spinee.2015.02.039 |
| [17] | Cheng L, Nie L, Zhang L. Fusion versus Bryan cervical disc in two-level cervical disc disease: a prospective, randomized study[J]. Int Orthop, 2009, 33(2): 1347–1351. |
| [18] | Rabin D, Pickett GE, Bisnaire L. The kinematics of anterior cervical discectomy and fusion versus artificial cervical disc: a pilot study[J]. Neurosurgery, 2007, 61(3 Suppl): 100–104. |
| [19] | Park DK, Lin EL, Phillips FM. Index and adjacent level kinematics after cervical disc replacement and anterior fusion-in vivo quantitative radiographic analysis[J]. Spine (Phila Pa 1976), 2011, 36(9): 721–730. DOI:10.1097/BRS.0b013e3181df10fc |
| [20] | Tu TH, Wu JC, Huang WC, et al. Heterotopic ossification after cervical total disc replacement: determination by CT and effects on clinical outcomes[J]. J Neurosurg Spine, 2011, 14(4): 457–465. DOI:10.3171/2010.11.SPINE10444 |
| [21] | 周非非, 孙宇, 赵衍斌, 等. 颈椎人工椎间盘置换术患者选择与异位骨化形成的相关性分析[J]. 中华骨科杂志, 2015, 35(4): 362–367. |
 2017, Vol.15
2017, Vol.15  Issue(2): 65-70
Issue(2): 65-70


