脊柱结核是临床常见的肺外结核,病变严重者常有脊柱后凸、神经损害或窦道形成,严重影响患者的生活质量。近年来,由于部分国家和地区获得性免疫缺陷综合征的流行,接受化疗、放疗和免疫抑制治疗的患者不断增多,导致免疫力低下群体增大,特别是由于耐药菌株的增加,导致各种类型结核病的发生率呈增长趋势,脊柱结核亦应引起临床关注[1]。脊柱结核多见于胸椎,其次是腰椎和胸腰段,而颈椎和骶椎则很少发生。颈椎结核虽然相对少见,但发生后凸成角畸形甚至瘫痪的危险性更高[2]。
颈椎结核经早期诊断和及时治疗能够显著降低死亡率,促进骨性融合。Arora等[3]的研究充分显示了非手术治疗的优势,然而非手术治疗并不能有效降低颈椎后凸畸形及神经症状发生率。一期病灶清除及植骨融合内固定手术治疗可即刻解除脊髓压迫,重建脊柱稳定,有效改善临床症状,降低并发症的发生率,促进颈椎结核的治愈[4-6]。本研究回顾性分析2008年1月—2014年12月本院行一期病灶清除并植骨融合内固定术治疗的26例颈椎结核患者资料,总结一期手术在颈椎结核治疗时的手术指征、病灶清除范围、手术入路及内固定方式选择,探讨一期病灶清除联合植骨融合内固定术在颈椎结核治疗中的应用价值。
1 资料与方法 1.1 一般资料病例纳入标准:术前颈椎影像学检查及实验室检查明确为颈椎结核。排除标准:①经胸部X线片及CT扫描,并经结核内科会诊,诊断为肺部血行播散性肺结核等活动性结核的患者;②存在心肺等全身功能障碍,不能耐受手术者。
本研究共纳入26例患者,男17例,女9例;年龄26~75岁,平均45.4岁。其中累及单椎体7例(C2 2例,C4 2例,C5 2例,C6 1例),相邻双椎体12例(C1,2 1例,C2,3 1例,C3,4 4例,C4,5 5例,C5,6 1例),3椎体4例(C3~5 1例,C4~6 2例,C5~7 1例);合并脊柱其他部位结核病灶3例(T5 1例、T12 1例、L3 1例)。合并颈椎后纵韧带骨化症1例。术前颈部疼痛视觉模拟量表(VAS)评分4~9分,平均5.9分;日本骨科学会(JOA)评分7~12分,平均10.5分;术前病变节段Cobb角26.7°±9.1°;美国脊髓损伤协会(ASIA)分级C级2例,D级3例,E级21例。
本组患者临床均表现为颈部疼痛、僵硬、屈伸旋转活动受限(前屈24.6°±11.6°,后伸16.0°±5.7°)。8例存在咽部肿痛,吞咽困难;5例伴有四肢麻木、无力、腱反射亢进等神经症状;7例伴有低热、盗汗、乏力等典型结核中毒症状。实验室检查示红细胞沉降率(ESR)为25~82(65.7±21.2)mm/h;抗结核抗体均阳性。
所有患者术前均摄颈椎正侧位X线片并行颈椎CT和MRI检查。X线片示椎体塌陷19例(73.1%);颈椎生理曲度减小7例(26.9%),反屈10例(38.5%);累及椎间盘14例(53.8%),表现为椎间隙高度降低、关节间隙模糊。颈椎CT扫描及重建示受累椎节骨质破坏,死骨形成,椎旁软组织中散在呈碎片状的低密度影。MRI示活动性颈椎结核病灶呈明显骨质及椎间盘信号改变,T1加权呈低信号,T2加权呈高信号,无明显强化;21例患者有椎前脓肿形成,T2加权呈明显高信号,脓肿边界光滑;23例可见脊髓明显受压。
1.2 术前准备均行颈部围领制动并规范抗结核治疗≥2周。应用四联抗结核药物,包括异烟肼0.3 g/次、利福平0.45 g/次、乙胺丁醇0.75 g/次和吡嗪酰胺1.0 g/次;每天1次,均清晨空腹顿服。注意观察抗结核药物不良反应。定期复查肝、肾功能,根据患者反应加用保护胃黏膜及促进胃动力药物。颈椎结核骨质破坏明显伴严重后凸畸形者术前均行颅骨牵引治疗,初始牵引质量2 kg。牵引中复查床边X线片,以明确寰枢椎脱位及颈椎后凸纠正情况。牵引质量依摄片情况可逐渐增加至6 kg。牵引过程中注意观察患者神经功能变化,一旦出现神经受牵拉损害症状加重,如上肢放射痛及麻木加重等,则应及时减少牵引质量。术前补液,改善贫血和低蛋白血症等。本组23例患者均待ESR < 50 mm/h时进行手术;3例患者行抗结核药物治疗8周后ESR仍≥80 mm/h,无其他手术禁忌证,行手术治疗,术后7 d降至35 mm/h以内。
1.3 手术方法所有患者均行气管插管全身麻醉,根据手术节段及病变情况决定手术入路。
常规颈椎前路和高位颈前咽后入路:骨质破坏严重者术中行颅骨牵引。上颈椎结核患者采用高位颈前咽后入路,共3例;下颈椎结核患者采用常规的右侧颈前入路,共18例。根据病灶范围结合术中透视定位,术中常可见因炎性反应及脓液集聚而饱满的椎前筋膜。切开椎前筋膜及前纵韧带可见有脓液及干酪样坏死组织,清除病灶、死骨、椎间盘和结核性肉芽肿等。于正常椎体置入撑开器螺钉,撑开器撑开的同时可以矫正颈椎的后凸畸形。椎管彻底减压后,搔刮相邻椎体至渗出鲜血。反复冲洗病灶。另取三面皮质的自体髂骨,修剪成相应大小,在撑开器牵拉下植入颈椎骨缺损处,此时应注意椎间隙撑开的高度。所有患者均未行钛网植骨融合。常规局部应用链霉素粉剂。然后行颈椎前路钢板固定。术毕病灶组织等标本常规送病理检查。
颈椎后路手术:只有在上颈椎结核患者需要后路枕颈固定时,或者在下颈椎结核患者需要联合后路内固定时可采用。3例寰枢椎结核患者均行寰椎后弓切除、枕颈内固定、植骨融合术。枕颈部在寰椎后弓切除减压完毕后用单面骨皮质的髂骨块植于枕骨隆突和枢椎棘突之间,并用螺钉固定于枕骨上。
2例下颈椎结核患者行后路侧块钢板固定或者颈椎椎弓根螺钉固定并联合颈椎前路手术。
1.4 术后处理患者术后卧床1周后,在颈托保护下可下床行走。常规佩戴颈托3个月。术后继续规范抗结核治疗9~12个月。术后1、3、6、12个月随访,术后1年以后每半年或病情变化时门诊复查,内容包括ESR、肝功能、肾功能、颈椎正侧位X线片、CT,检查植骨融合情况,必要时行颈椎MRI检查观察脊髓减压情况。每次随访疗效评估包括JOA评分、VAS评分、病变节段后凸Cobb角情况。
1.5 统计学处理采用SPSS 17.0软件进行数据分析。计量资料以x±s表示,先行正态性检验,符合正态分布的数据行单因素方差分析,不符合正态分布的数据行Wilcoxon秩和检验。以P < 0.05为差异有统计学意义。
2 结果 2.1 一般情况本组26例患者均获得随访,随访时间为13~49个月,平均25.3个月;自体髂骨植骨均获得较好骨性融合,融合时间为3~6个月,平均4.5个月。本组1例患者术后出现髂骨取骨区切口脂肪液化、不愈合,再次清创缝合后2周切口二期愈合。余患者未出现相应并发症,末次随访时未发生颈椎结核复发、植骨块移位及假关节形成。术后连续规范抗结核治疗12~18个月,待患者复查符合以下标准后停药。①全身情况好,无结核中毒症状,食欲好,体温正常,恢复日常活动;②颈项部局部症状消失,无疼痛不适;③每月1次,连续复查3次ESR正常;④影像学检查示病变节段有骨小梁通过,已骨性融合,脓肿消失。
2.2 JOA评分、VAS评分、病变节段后凸Cobb角情况术后所有患者神经症状及疼痛程度均较术前明显改善。1例术前不全瘫患者术后4周下床行走,ASIA恢复至E级。末次随访时JOA评分、VAS评分分别与术前比较,差异均有统计学意义(P < 0.05,表 1)。术后所有患者下颈椎后凸畸形明显改善,差异有统计学意义(P < 0.05,表 1)。典型病例影像学资料见图 1。
|
|
表 1 统计数据 Table 1 Statistical data |
|
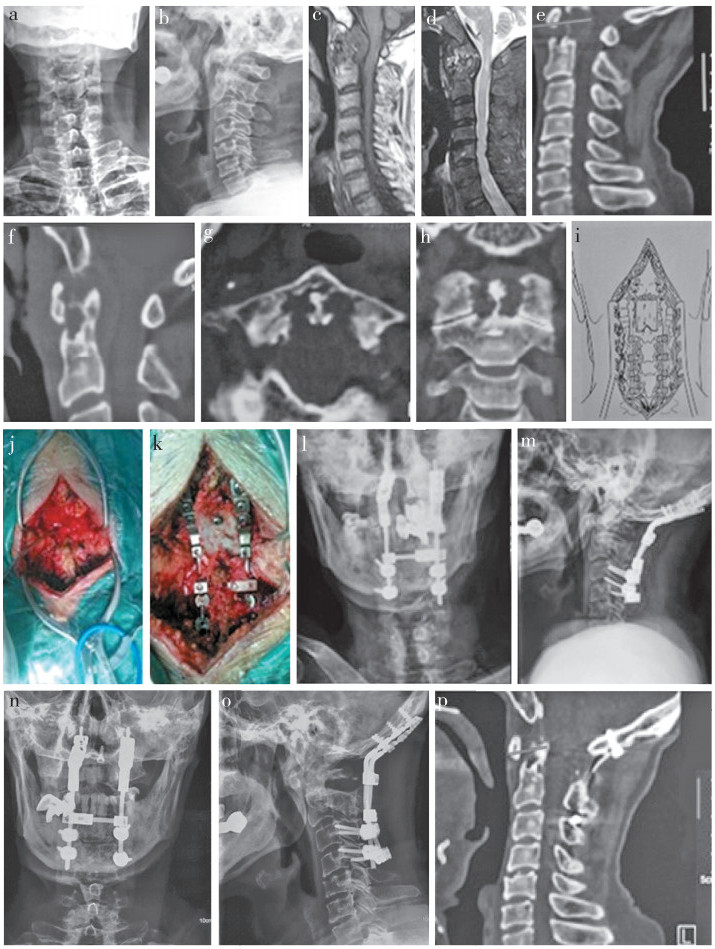
男,69岁,寰枢椎结核,ASIA D级,颈椎病 a~e:术前位X线片及CT示寰枢椎骨质破坏,死骨形成,齿突脓肿最宽处约3.2 cm f~h:术前MRI示寰枢椎椎体破坏,脓肿形成,脊髓压迫严重,脊髓信号改变合并下颈椎多节段椎间盘突出 i~k:一期后路枕颈融合术 l,m:术后X线片示内固定位置满意 n,o:术后10个月X线片示内固定位置满意 p:术后CT示齿突脓肿最宽处2.1 cm Male, 69 years old, atlantoaxial TB, ASIA D and cervical spondylosis a-e:Preoperative roentgenographs and CTs show atlantoaxial bone destruction and bone sequestration, and widest site of odontoid abscess is 3.2 cm f-h:Preoperative MRIs show vertebral body destruction with signal change, severe spinal cord compression, vertebral abscess and multilevel lumbar disc herniation of inferior cervical vertebrae j-k:One-stage posterior occipital cervical fusion l, m:Postoprative roentgenographs show good internal fixation and deformity correction n, o:Roentgenographs at 10 months show good internal fixation and deformity correction p:Postoprative saggital CT shows widest site of odontoid abscess is 2.1 cm 图 1 典型病例影像学资料 Figure 1 Imaging data of a typical case |
颈椎结核进行性加重会形成脓肿,进一步发展导致椎体破坏、塌陷进而导致颈椎后凸畸形可压迫脊髓,出现神经症状甚至瘫痪。未经有效治疗的颈椎结核甚至进一步形成皮肤窦道,经久不愈合,使治疗难度进一步增大。及时、彻底手术干预清除结核病灶、重建颈椎稳定性可大幅缩短疗程,有效防止脊柱畸形[2, 6]。
冷脓肿、死骨形成、窦道、椎体破坏严重、严重后凸畸形、神经压迫症状及截瘫等均为颈椎结核的手术适应证[7-8]。实施手术前还应明确有无手术禁忌证和患者对手术的耐受能力。应选择适当的手术时机,确保手术疗效,减少手术并发症。颈椎结核手术时机选择应注意以下几点。①在冷脓肿破溃、窦道形成前手术;②尽量于出现脊髓压迫、截瘫症状前手术,对于已经出现截瘫的患者应尽快手术;③患者一般状况好转,体温正常或仅有低热,贫血及低蛋白血症得到纠正,心肺功能检查无手术禁忌证,此时宜手术。本组患者术前均接受规范的抗结核治疗 > 2周,23例患者ESR控制在50 mm/h以内,接受手术治疗;3例患者行抗结核药物治疗8周ESR仍≥80 mm/h,无其他手术禁忌证,行手术治疗,术后7 d ESR降至35 mm/h以内。在强调手术治疗的同时,应采取行之有效的非手术治疗,包括规范的抗结核药物治疗、局部制动、营养支持治疗等[9]。
3.2 颈椎结核的病灶清除脊柱结核手术的目的在于清除结核病灶、解除脊髓压迫、重建脊柱稳定性。病灶清除以后尽可能早期重建病灶清除所造成的骨缺损,恢复脊柱序列。本组患者均一期行植骨融合内固定术。根据文献报道[10-11],结核病灶处理分为两种方式,即病灶根治性切除术(radical resection)和病灶清除术(debridement)。前者要求将硬脊膜周围的病变组织尽最大可能完全切除,直至流血的健康骨组织,该术式将产生广泛的骨缺损,为脊柱重建带来困难。后者仅要求清除脓肿、肉芽组织、干酪组织、坏死的椎间盘组织、死骨以及为了彻底减压而需要切除的部分活性骨。本研究认为结核病灶清除术不同于肿瘤切除术,不应过于扩大切除,应保留健康的骨质及“亚健康骨”。病灶清除范围过大不但会影响颈椎的稳定,增加损伤周围血管、神经的风险,而且也会影响内固定对颈椎的固定效果。结核病灶清除后可以改善局部血供,使结核药物更好地渗透到局部,从而更有利于发挥作用。在合理的抗结核药物作用下,“亚健康骨”将变为健康骨。结核的最终治愈有赖于抗结核药物的规范、合理应用。本组所采用的术式均为病灶清除术,术中仅限于取出死骨,对于未受侵犯的健康骨,甚至有疑问的骨组织均未切除。本组患者术后经规范抗结核治疗均未出现结核病灶复发。
3.3 手术入路及稳定性重建应根据患者的具体病情制定个体化的综合治疗方案,根据病变累及节段及局部畸形情况采取不同的手术方式[7, 12]。寰枢椎结核可采用经颌下入路清除病灶或经口穿刺抽脓,同时后路行寰枢椎融合或枕颈融合[13-15]。本组有1例寰枢椎结核患者脊髓明显受压,一期行后路寰椎后弓切除、椎管减压、枕颈融合内固定术,术后规范抗结核药物治疗,患者神经压迫症状明显改善,定期复查可见脓肿范围逐渐缩小。与经口入路相比,经颌下入路具有创伤小、手术时间短、出血量少、术后感染概率低的特点,对于上颈椎结核病灶清除尤为适用。但由于咽后壁脓肿常伴周围软组织、咽部及高位食管壁水肿,同时术中为获得较好的视野会过度向内牵拉内脏鞘,所以易损伤咽部及高位食管。穿刺抽脓可能会诱发窦道形成,与口腔内细菌形成混合感染,经久不愈。应根据患者病情采取个性化治疗。本研究枕颈融合后路植骨组采用单面皮质骨片,于枕骨隆突制作植骨创面,骨片嵌于枕骨隆突与枢椎棘突之间,用螺钉将骨片固定于枕骨隆突。
下颈椎结核一般采用颈前右侧入路病灶清除植骨融合内固定术[16-17]。本组中累及单椎体或多椎体的颈椎结核均行颈前路病灶清除或椎间隙减压植骨内固定术,术后均获得较好骨性融合,未发生植骨块松动移位、塌陷及假关节形成等并发症。本组患者均行髂骨块植骨,未行钛网植骨。由于局部病灶处理并不能确保将结核分枝杆菌完全清除,钛网直接暴露于病灶内,其网状结构为结核分枝杆菌提供了较大、较粗糙的接触面,并且抗结核药物不能到达无血管的钛网网格内,可能为细菌的生长繁殖提供了条件。内固定在脊柱结核手术中的应用已经广为接受。笔者认为对于累及≥3个椎体颈椎结核者病灶清除会更多破坏颈椎正常结构,颈椎稳定性差。应尽量减少对“亚健康骨”的破坏,减少骨质缺损,增加颈椎稳定性。本组研究共4例患者累及3个椎体,均行一期前路病灶清除,尽量保留较多的健康骨、亚健康骨,增加颈椎稳定性,取三面骨皮质的髂骨植骨,颈椎前路钢板内固定。术后严格颈部围领制动,规范抗结核药物治疗。
综上所述,对于有手术指征的颈椎结核患者在规范抗结核药物控制下应早期行彻底的病灶清除及稳定性重建,以有效减少后凸畸形的发生,降低脊髓损伤的风险。手术方式可根据病变累及节段及局部畸形情况采取一期病灶清除术联合不同的稳定性重建术式。术后继续长程、规范化抗结核治疗,是取得良好疗效和避免结核复发的关键因素[6, 18-19]。
| [1] | Garg RK, Somvanshi DS. Spinal tuberculosis: a review[J]. J Spinal Cord Med, 2011, 34(5): 440–454. DOI:10.1179/2045772311Y.0000000023 |
| [2] | Turgut M. Spinal tuberculosis (Pott's disease): its clinical presentation, surgical management, and outcome. A survey study on 694 patients[J]. Neurosurg Rev, 2001, 24(1): 8–13. DOI:10.1007/PL00011973 |
| [3] | Arora S, Sabat D, Maini L, et al. The results of nonoperative treatment of craniovertebral junction tuberculosis: a review of twenty-six cases[J]. J Bone Joint Surg Am, 2011, 93(6): 540–547. DOI:10.2106/JBJS.J.00634 |
| [4] | Hodgson AR, Stock FE. Anterior spinal fusion a preliminary communication on the radical treatment of Pott's disease and Pott's paraplegia[J]. Br J Surg, 1956, 44(185): 266–275. DOI:10.1002/(ISSN)1365-2168 |
| [5] | 李宏伟, 罗小波, 鲍达. 前路病灶清除植骨内固定治疗下颈椎结核的中期随访研究[J]. 脊柱外科杂志, 2012, 10(2): 97–100. |
| [6] | 马远征. 脊柱结核的治疗应遵循个体化综合治疗原则[J]. 中华外科杂志, 2007, 45(18): 1227–1229. DOI:10.3760/j.issn:0529-5815.2007.18.002 |
| [7] | Elsawaf A. Outcome of surgical versus conservative management of cervical spine myelopathy secondary to cervical tuberculosis[J]. Neurosurg Rev, 2013, 36(4): 621–628. DOI:10.1007/s10143-013-0475-9 |
| [8] | 陈华江, 王建喜, 滕红林, 等. 一期病灶清除术治疗颈椎结核[J]. 中华骨科杂志, 2014, 34(2): 149–155. |
| [9] | 王传庆. 脊柱结核外科治疗的现状与进展[J]. 结核病与肺部健康杂志, 2013, 2(1): 64–68. |
| [10] | Oguz E, Sehidioglu A, Altinmakas M, et al. A new classification and guide for surgical treatment of spinal tuberculosis[J]. Int Orthop, 2008, 32(1): 127–133. DOI:10.1007/s00264-006-0278-5 |
| [11] | 金大地. 再谈脊柱结核的外科治疗[J]. 中华外科杂志, 2007, 45(18): 1225–1226. DOI:10.3760/j.issn:0529-5815.2007.18.001 |
| [12] | 瞿东滨, 金大地. 成人颈椎结核外科治疗的术式选择[J]. 临床骨科杂志, 2007, 10(5): 385–387. |
| [13] | Lifeso R. Atlanto-axial tuberculosis in adults[J]. J Bone Joint Surg Br, 1987, 69(2): 183–187. |
| [14] | Jain AK, Dhammi IK, Prashad B, et al. Simultaneous anterior decompression and posterior instrumentation of the tuberculous spine using an anterolateral extrapleural approach[J]. J Bone Joint Surg Br, 2008, 90(11): 1477–1481. |
| [15] | 任先东, 王卫军, 张峡, 等. 高位颈椎的前路手术治疗[J]. 脊柱外科杂志, 2005, 3(3): 145–147. |
| [16] | Hassan MG. Anterior plating for lower cervical spine tuberculosis[J]. Int Orthop, 2003, 27(2): 73–77. |
| [17] | Ramani PS, Sharma A, Jituri S, et al. Anterior instrumentation for cervical spine tuberculosis: an analysis of surgical experience with 61 cases[J]. Neurol India, 2005, 53(1): 83–89. DOI:10.4103/0028-3886.15067 |
| [18] | Jain AK. Tuberculosis of the spine: a fresh look at an old disease[J]. J Bone Joint Surg Br, 2010, 92(7): 905–913. |
| [19] | 陈兴, 鲍达, 马远征, 等. 颈椎结核耐药性观察及个体化治疗[J]. 脊柱外科杂志, 2008, 6(5): 284–287. |
 2017, Vol.15
2017, Vol.15  Issue(2): 94-99
Issue(2): 94-99


