钙化型腰椎椎间盘突出症包括椎体后缘离断症和退变性腰椎椎间盘钙化,其手术治疗是临床上的难题。后正中入路的腰椎开放手术或经椎板间入路经皮内窥镜下椎间盘切除术,均需要将马尾神经牵拉过中线才能取出致压物,特别是中央型突出的椎间盘,马尾神经一般牵拉较重,神经牵拉损伤的风险较高[1-3];且钙化物的去除需要用骨凿凿除或者磨钻磨除,神经损伤或硬膜损伤的风险较高[4-5]。因此,本研究回顾性分析后外侧经椎间孔入路经皮内窥镜下椎间盘切除术(PETD)治疗钙化型腰椎椎间盘突出症,并对术后疗效进行评价。
1 资料和方法1.1 一般资料回顾性分析本院2013年9月—2014年9月收治的20例钙化型腰椎椎间盘突出症患者的临床资料,所有患者行PETD并钙化物取出。其中男12例,女8例;年龄18~36(31±4)岁;L5/S1节段4例(中央型2例,旁中央型2例),L4/L5节段16例(中央型5例,旁中央型11例)。所有患者病程3~16个月,以一侧下肢放射痛为主,非手术治疗 > 3个月无明显缓解。所有患者术前均行腰椎CT和MRI检查,显示存在手术节段一侧为主的神经根管狭窄,15例患者的钙化灶与症状侧在同侧,5例患者在对侧。所有患者术前患侧的直腿抬高试验均 < 60°,加强试验阳性。1例患者存在马尾综合征。术前根据CT对钙化物的形态进行了分型:孤立型(钙化物长度 < 3 mm,10例)、半月型(钙化物长度≥3 mm且≤10 mm,6例)、连续型(钙化物长度 > 10 mm,4例)。根据MRI上旁中央型突出物与行走根的关系分为肩上型(11例)和腋下型(2例)。
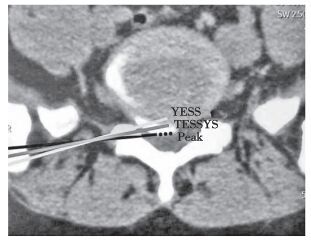
1.2 手术方法所有患者采用局麻,取俯卧位,均选择症状严重的一侧进行穿刺,采用顶点技术(Peak技术,图 1),该技术入路正对突出物/钙化物的顶点,目的是可在镜下从外向内使用环锯或骨凿切除钙化物。在术前完善患者MRI及CT检查,在CT片上对手术的入路进行精确的测量,从椎间盘突出的顶端处作一条切线,该切线与腹膜后穹窿距离为1~2 cm,该切线与水平面的夹角即手术穿刺路径与水平面的成角,该切线与皮肤的交点到中线的距离,可作为手术穿刺点与中线距离的参考。当钙化物与症状在对侧时,手术中通过环锯切除上关节突腹侧的骨赘后,将工作通道放置于椎管内正对突出物的顶端处,先用髓核钳取出突出的髓核组织,充分显露钙化物后,用镜下剪刀(Joimax,德国)将小片钙化物(孤立型或半月型)与周围的纤维环游离后取出;用镜下环锯或骨凿(Joimax,德国)对大片环状钙化物(半月型或连续型)进行“分块”后切除。当钙化物与症状侧在同侧时,将工作通道放置于椎管内正对突出物的顶端处;对较小的钙化物(孤立型或半月型),用镜下剪刀将钙化物充分游离后整块取出;对于大片环状钙化物(半月型或连续型),在镜下使用镜下小号环锯或电动磨钻切开钙化物表面,进行“开窗减压”后摘除钙化物内部的髓核,再用镜下小号骨凿凿除压迫神经根的钙化物。该手术的禁忌证为严重的骨性椎管狭窄。对于肩上型的旁中央型突出,可将工作通道建立至棘突中线附近进行减压。对于腋下型旁中央型突出,先建立通道至椎弓根内侧缘,减压出部分髓核后,再深入行走神经根腋下进行减压。对于中央型的钙化物,神经根在术中可能会遮挡手术视野,可采用镜下小号环锯,在水流的搏动下绕过行走神经根,并将其挡开后,正对钙化物的顶部进行切割,然后将钙化物逐块取出,操作时要小心避免误伤神经根,否则会造成硬膜破裂。对于高髂嵴L5/S1腰椎椎间盘突出症,由于髂嵴的阻挡,穿刺点不能靠外,需要磨除更多的上关节突,甚至部分髂嵴来获得足够的手术视野。
|
图 1 YESS、TESSYS和Peak技术入路的区别 Figure 1 Difference between YESS, TESSYS and Peak approach |
患者术前、术后及随访时的腰腿痛采用疼痛视觉模拟量表(VAS)[6]进行评价。手术效果采用MacNab标准[7]进行评价。记录术中、术后的并发症发生情况。
1.4 统计学处理所有数据应用SPSS 13.0软件进行统计分析。计量资料以x±s表示。对术前、术后的评分先行正态性检验,符合正态分布的数据行单因素ANOVA方差分析;检验水准α值取双侧0.05。以P < 0.05为差异有统计学意义。
2 结果所有手术顺利完成,均采用单一手术切口,长8~10 mm。患者住院3~7 d,术后卧床3~5 d,以避免复发。患者随访 > 3个月,手术时间为(105±23)min。术前腰痛VAS评分为(6.3±2.5)分,术后即刻为(1.2±2.2)分,术后3个月为(0.9±0.3)分,与术前相比,差异均有统计学意义(P < 0.05)。术前腿痛VAS评分为(7.4±2.8)分,术后即刻为(0.4±0.3)分,术后3个月为(0.2±0.1)分,与术前相比,差异均有统计学意义(P < 0.05)。本组患者术后未出现下肢神经功能恶化、肠道损伤及椎间隙感染等并发症,仅1例患者出现脑脊液漏,平卧1周后痊愈出院。所有患者术后3个月按MacNab标准评价的疗效均为优。典型病例影像学资料见图 2。
|
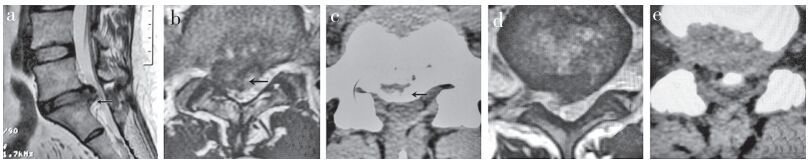
L5/S1椎间盘突出症伴钙化a:术前矢状面MRI T2加权像示L5/S1节段椎间盘突入椎管内,呈低信号影b:术前横断面MRI T2加权像示椎管内巨大的突出物,呈低信号影c:术前CT示连续型钙化的突出物,骶骨上关节突增生、肥大、内聚,伴侧隐窝狭窄d:术后MRI示L5/S1右侧突出的椎间盘被切除,S1的上关节突尖部被切除,部分增生的黄韧带被切除后S1神经根管获得彻底减压e:术后CT示L5/S1右侧的钙化物被切除,上关节突腹侧被切除,S1神经根管获得彻底减压 L5/S1 lumbar disc herniation with calcification a:Preoperative sagittal MRI T2 weighted imaging shows L5/S1 intervertebral disc herniating into spinal canal which is low signal intensity b:Preoperative transverse MRI T2 weighted imaging scan shows intraspinal giant protrusion with low signal intensity c:Preoperative CT shows continuous calcified protrusion and superior articular process of sacrun hyperplasia, with lateral recess stenosis d:Postoperative MRI shows right side herniated intervertebral disc and tip of S1 superior articular process are removed. After partial resection of ligamentum flavum, S1 nerve root canal is completely decompressed e:Postoperative CT shows right side calcification disc and ventral side of superior articular process are removed, and S1 nerve root canal is completely decompressed 图 2 典型病例影像学资料 Figure 2 Radiologic data of a typical case |
本研究结果表明,PETD是一种有效治疗钙化型椎间盘突出症的手术方法,具有创伤小、恢复快的优点。由于从侧后方入路,避免了后正中入路手术中对神经根的牵拉[8],降低了神经根损伤的风险,本组病例未出现术后神经功能恶化。有研究将椎间盘钙化作为内窥镜下腰椎椎间盘切除术的相对禁忌证之一,经椎板间入路对钙化物进行切除时往往需要使用磨钻[9-10],神经损伤或硬膜损伤的风险较高[4-5]。本研究采用侧后方经椎间孔入路,在直视下采用镜下环锯对钙化物进行分割后切除,具有简便和安全的优点。另外,本研究提出了钙化型腰椎椎间盘突出症的分型,较小的钙化物,如孤立型或半月型,充分游离后可整块切除;较大的钙化物,如半月型或连续型,则需采用分块切除的方法。脱出的髓核一般是根性症状的来源,因此手术入路应选择症状侧,首先找到脱出的髓核,取出后再切除钙化物,扩大神经根管。钙化物通常会伴有与神经根的粘连,应当充分分离与神经根的粘连,以获得较好的临床疗效。
PETD治疗钙化型腰椎椎间盘突出症,要求入路与水平面的夹角尽量小,故穿刺点应尽量靠外。本研究采用“顶点技术”(Peak技术),在安全的前提下采用水平入路,并且磨除更多的上关节突,使工作套管进入椎管内,并正对突出椎间盘钙化物的顶部,这与YESS技术、TESSYS技术和靶向技术是有所区别的。YESS技术的入路朝向椎间盘内部,TESSYS技术的入路朝向下位椎体的后上缘,靶向技术的入路对准突出物的中心;在冠状面上,YESS技术入路平行于椎间隙平面,TESSYS技术入路斜向尾端对准上关节突,靶向技术入路对准突出的椎间盘[11-12]。“顶点技术”最适用的节段是L4/L5和低髂嵴的L5/S1。当L5/S1椎间盘突出症伴高髂骨,高髂骨或高骶骨翼会阻挡进入L5/S1椎间孔的通道,可利用环锯或骨钻在髂骨上开窗,以获得合适的入路角度。
若患者的主要症状是神经根性的下肢放射痛,神经根管入口区增生的上关节、肥厚的黄韧带、椎体后缘增生的骨赘、突出的髓核和钙化物是引起行走神经根受压的主要原因。因此,神经根管处的减压较中央处的减压更为重要。磨除上关节突的尖部和腹侧面,既可切除黄韧带和椎间孔韧带位于此处的止点,以彻底松解出口神经根,也可获得减压行走神经根入口区和中间区的操作空间。本研究中,对患者术后影像学资料的观察,发现位于中央部位的小部分钙化物并未被彻底切除,而直腿抬高试验术中即转为阴性,表明下肢放射痛症状已完全消失,证实中央部的钙化物并非都需要彻底切除,神经根管处的减压较中央突出钙化物的切除更为重要[13]。若患者的症状侧和钙化侧并非同一侧,应从症状侧入路,摘除突出的髓核组织,钙化物如不引起神经症状则无须切除。
“顶点技术”在应用时要防止腹腔脏器、出口神经根和行走神经根的损伤。对于L4/L5节段,由于腹膜后穹隆的存在,水平入路可能伤及腹膜及腹腔脏器,术前需要在CT上仔细评估计算穿刺点和穿刺角度。侧卧位可使患侧的腹膜前移,降低穿刺引起腹膜损伤的概率;工作套管保护下的环锯处理技术可以预防出口神经根的损伤。环锯操作时要防止超过椎弓根内缘而导致行走神经根的损伤,尤其对于L3/L4及以上节段。中央型的钙化物,在遇到行走神经根阻挡时,可利用水压的搏动,将镜下环锯绕过行走神经根,或利用工作套管挡开行走神经根后,再对钙化物进行处理。
由于钙化物是由慢性炎症产生,一般在突出椎间盘的表面,采用YESS或TESSYS技术时,对于钙化物的切除都是“从内向外”,利用侧方钬激光或镜下磨钻,从钙化物的腹侧向背侧切除[16-17],这在切除中央型钙化物时,有可能对纤维环造成较大的损害。“顶点技术”是对准钙化物顶端,从外向内进行切除,采用普通工具,操作简便,可最大程度地保护纤维环的完整性。
综上所述,PETD避免过度牵拉神经根,可降低术中发生神经损伤的概率,可切除神经根管处的钙化物,有效缓解患者症状,治疗钙化型腰椎椎间盘突出症安全,有效。
| [1] | 汤俊君, 王新伟, 袁文. 腰椎椎体间融合术研究现状[J].脊柱外科杂志, 2006, 4(1): 58–60. |
| [2] | Liu J, Deng H, Long X, et al. A comparative study of perioperative complications between transforaminal versus posterior lumbar interbody fusion in degenerative lumbar spondylolisthesis[J].Eur Spine J, 2016, 25(5): 1575–1580. DOI:10.1007/s00586-015-4086-8 |
| [3] | 陈宣煌, 许卫红, 胡建伟, 等. 小切口椎旁肌间隙入路和传统开放式入路腰椎后路融合术的比较[J].脊柱外科杂志, 2012, 10(2): 101–104. |
| [4] | Karamouzian S, Eskandary H, Faramarzee M, et al. Frequency of lumbar intervertebral disc calcification and angiogenesis, and their correlation with clinical, surgical, and magnetic resonance imaging findings[J].Spine(Phila Pa 1976), 2010, 35(8): 881–886. DOI:10.1097/BRS.0b013e3181b9c986 |
| [5] | Choi JW, Lee JK, Moon KS, et al. Transdural approach for calcified central disc herniations of the upper lumbar spine. Technical note[J].J Neurosurg Spine, 2007, 7(3): 370–374. DOI:10.3171/SPI-07/09/370 |
| [6] | Huskisson EC. Measurement of pain[J].Lancet, 1974, 2(7889): 1127–1131. |
| [7] | MacNab I. Negative disc exploration. An analysis of the causes of nerve-root involvement in sixty-eight patients[J].J Bone Joint Surg Am, 1971, 53(5): 891–903. DOI:10.2106/00004623-197153050-00004 |
| [8] | Cong L, Zhu Y, Tu G. A meta-analysis of endoscopic discectomy versus open discectomy for symptomatic lumbar disk herniation[J].Eur Spine J, 2016, 25(1): 134–143. DOI:10.1007/s00586-015-3776-6 |
| [9] | Nellensteijn J, Ostelo R, Bartels R, et al. Transforaminal endoscopic surgery for lumbar stenosis:a systematic review[J].Eur Spine J, 2010, 19(6): 879–886. DOI:10.1007/s00586-009-1272-6 |
| [10] | Dabo X, Ziqiang C, Yinchuan Z, et al. The clinical results of percutaneous endoscopic interlaminar discectomy(PEID) in the treatment of calcified lumbar disc herniation:a case-control study[J].Pain Physician, 2016, 19(2): 69–76. |
| [11] | Xin G, Shi-Sheng H, Hai-Long Z. Morphometric analysis of the YESS and TESSYS techniques of percutaneous transforaminal endoscopic lumbar discectomy[J].Clin Anat, 2013, 26(6): 728–734. DOI:10.1002/ca.v26.6 |
| [12] | Pan Z, Ha Y, Yi S, et al. Efficacy of transforaminal endoscopic spine system(TESSYS) technique in treating lumbar disc herniation[J].Med Sci Monit, 2016(22): 530–539. |
| [13] | Choi KC, Lee JH, Kim JS, et al. Unsuccessful percutaneous endoscopic lumbar discectomy:a singlecenter experience of 10228 cases[J].Neurosurgery, 2015, 76(4): 372–380. DOI:10.1227/NEU.0000000000000628 |
| [14] | Yeung AT, Tsou PM. Posterolateral endoscopic excision for lumbar disc herniation:Surgical technique, outcome, and complications in 307 consecutive cases[J].Spine(Phila Pa 1976), 2002, 27(7): 722–731. DOI:10.1097/00007632-200204010-00009 |
| [15] | Gibson JN, Subramanian AS, Scott CE. A randomised controlled trial of transforaminal endoscopic discectomy vs microdiscectomy[J].Eur Spine J, 2016, 26(3): 847–856. |
 2017, Vol.15
2017, Vol.15  Issue(3): 146-149
Issue(3): 146-149


