腰椎椎间盘突出症(LDH)是导致腰腿痛最常见的原因之一,L4/L5、L5/S1是LDH的好发部位。目前临床上治疗LDH的手术方法主要包括传统开放手术及微创手术,微创手术主要借助脊柱内窥镜系统经皮入路完成减压融合手术。传统开放式手术多经后正中切口,广泛的椎旁肌剥离对组织破坏较大,术后易残留慢性腰痛;Wiltse入路是经最长肌与多裂肌的肌间隙到达关节突和横突,实现腰椎后外侧的植骨融合,该入路对椎旁肌的损伤较小,有利于降低术后腰痛的发生率[1-2]。本研究旨在通过比较2种手术入路治疗LDH的围术期及术后疗效,探讨减少术后慢性残留腰痛的方法。
1 资料与方法 1.1 一般资料纳入标准:①符合LDH诊断标准的患者,且经过≥6个月的严格非手术治疗,症状未明显缓解,或缓解后再次复发且复发后症状如前甚至加重。②经CT及MRI证实为L3/L4、L4/L5或L5/S1椎间盘突出合并该节段椎管狭窄,伴有腰部疼痛或者一侧下肢疼痛、麻木。③所有患者均接受单节段椎间盘髓核摘除植骨融合术。排除标准:①既往有腰椎手术史,或伴腰椎骨折、脊柱侧凸、腰椎感染、严重骨质疏松等疾病者,不包括行胶原酶溶解术者。②有其他急性或难以控制的慢性疾病,不包括6个月非手术治疗期间出现二便障碍和马尾综合征者。③临床中无法有效合作者。本研究由本院临床伦理委员会批准施行。
2012年1月—2015年12月,本院收治的85例LDH患者纳入本研究。其中男57例、女28例,年龄42 ~ 65岁。经CT及MRI证实压迫左侧神经根者47例,压迫右侧神经根者38例;累及L3/L4 8例,L4/L5 29例,L5/S1 48例。所有手术均由同一组医师完成。采用统计分析系统(SAS)进行随机分组,凡符合纳入标准并签署知情同意书的患者随机分为2组。经Wiltse入路(A组)43例,男28例,女15例;年龄为(49.8±15.02)岁,体质量指数(BMI)为(23.11± 4.87)kg/m2;传统后正中入路(B组)42例,男29例,女13例;年龄为(46.8±12.49)岁,BMI为(22.88± 4.11)kg/m2。2组一般资料差异无统计学意义。
1.2 手术方法及术后处理患者全身麻醉,取俯卧位,C形臂X线机透视定位手术节段,标记手术切口。
A组:以手术节段为中心,取后正中切口长3~ 5 cm,切开皮肤、皮下组织及腰背筋膜,另于正中切口两旁各做1个3 cm纵行小切口,指尖分离腰背筋膜后经多裂肌与最长肌肌间隙直达关节突及横突。C形臂X线机透视定位,于上、下位椎体置入椎弓根螺钉。定位正确后,保留关节突关节(除极外侧椎间盘),咬除黄韧带,保留硬膜外脂肪组织,先通过椎间盘摘除解除神经根压迫,再依次用不同型号的铰刀处理椎间隙,直至神经根压迫完全解除。将大小合适、填充自体骨的椎间融合器置入椎间隙。C形臂X线机透视证实融合器的白色亮点位于上、下终板之间,未超过椎体前后缘,位置满意后适当加压固定、锁定钉棒。
B组:以手术节段为中心,取后正中切口,长6 ~ 8 cm,逐层切开皮肤及皮下组织,纵行切开腰背筋膜,沿棘突和椎板两侧剥离椎旁肌群,至关节突关节,在C形臂X线机透视下常规置入椎弓根螺钉。椎间盘处理及经椎间孔椎体间融合术操作同A组。
术后放置引流管24 ~ 48 h,若48 h后引流量仍 > 50 mL则延长拔管时间1 d。在腰围保护下逐步下床活动,行腰背肌功能锻炼,严格佩戴腰围3个月,术后6个月内避免久坐及负重。
1.3 观察指标记录2组患者手术时间、术中出血量、术后引流量、住院天数,采用视觉模拟量表(VAS)[3]对患者术前、术后腰部和下肢疼痛进行评分;采用Oswestry功能障碍指数(ODI)[4]评价患者术前、术后功能状况;采用日本骨科学会(JOA)评分[5]评价患者术后腰椎功能。
1.4 统计学处理采用SPSS 20.0软件对数据进行统计分析。计数资料采用χ2检验进行比较;计量资料以x±s表示,采用成组设计t检验进行比较。以P < 0.05为差异有统计学意义。
2 结果所有手术均顺利完成,2组患者平均随访时间26个月。A组术中出血量、术后引流量、住院天数少于B组,差异均有统计学意义(P < 0.05);2组手术时间差异无统计学意义(P > 0.05),具体见表 1。2组患者术前腰痛VAS评分、下肢痛VAS评分、JOA评分及ODI差异均无统计学意义(P > 0.05);术后各时间点2组患者所有指标均较术前明显改善,差异有统计学意义(P < 0.05),具体见表 2。术后各时间点2组间相比,下肢痛VAS评分、JOA评分及ODI差异均无统计学意义(P > 0.05);腰痛VAS评分A组优于B组,差异有统计学意义(P < 0.05),具体见表 2。
|
|
表 1 统计数据 Table 1 Statistical data |
|
|
表 2 VAS、JOA评分及ODI Table 2 VAS, JOA score and ODI |
A组1例术后出现一过性左下肢麻木,给予激素、脱水等治疗,于术后2周症状消失。B组1例术中硬膜囊出现破口,发生脑脊液漏,延期1 d拔管后痊愈。2组术后均未发生感染、内固定失败、假关节形成等并发症,邻近节段退变情况仍在随访之中。典型病例影像学资料见图 1。
|
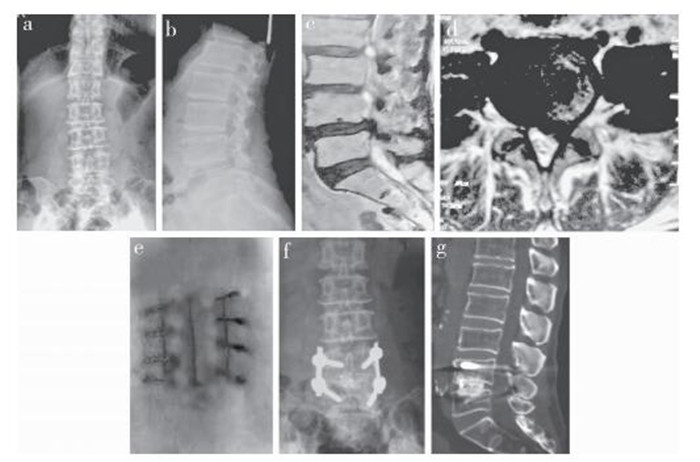
女,45岁,腰部疼痛,左下肢麻木10年a,b:术前正侧位X线片示腰椎向右侧轻度侧凸,L4/L5椎间隙变窄c:术前矢状面T2WI MRI示L4/L5中央椎管狭窄,压迫马尾神经d:术前横断面MRI示L4/L5椎间盘突出,压迫L5神经根,神经根管和侧隐窝狭窄e:术后14 d伤口拆线,愈合良好f:术后6个月X线片示内固定位置良好,无松动g:术后26个月矢状面CT示植骨融合 Female, 45 years old, low back pain and left lower limbs numbness for 10 years a, b:Preoperative anteroposterior and lateral roentgenographs show slightly scoliosis to right side, and narrowing of L4/L5 intervertebral space c:Preoperative saggital T2WI MRI shows L4/L5 central spinal stenosis and compression of cauda equina d:Preoperative transverse MRI shows L4/L5 disc herniation, compression of L5 nerve roots, stenosis of nerve root canals and lateral recess e:Postoperative 14 d, stitches is removed, and incision heal well f:Roentgenograph at postoperative 6 months shows internal fixation in good position without loosening g:CT at postoperative 26 months shows bone graft fusion 图 1 典型病例影像学资料 Figure 1 Imaging data of a typical case |
1959年Watkins[6]首次报道了通过腰方肌间隙与骶棘肌外侧的间隙来完成腰椎后外侧融合手术,用于腰椎滑脱、腰椎骨折术后翻修、有后路手术感染史的后路翻修手术、关节突关节间植骨融合等。1968年,Wiltse等[1]提出了一种改良的椎弓根置钉技术,采用后路双侧椎旁纵行切口,从内侧的多裂肌与外侧的最长肌之间的肌间隙进行腰椎后外侧横突间融合,而不需椎管减压,该入路被称为椎旁肌间隙入路,又称Wiltse入路。目前多采用后路单个后正中切口向双侧分离至最长肌和多裂肌的间隙。解剖学研究发现Wiltse入路为自然肌间隙入路,血管分布少,术中无需切断、剥离肌肉,出血量少;可直接显露神经根管、小关节及横突,有利于神经根管减压;容易确定椎弓根钉进针点及置钉;避免剥离和损伤腰神经后支,防止骶棘肌失神经支配;显露时不破坏棘上韧带的连接,最大限度保留了脊柱解剖结构的完整性,保持脊柱后部的稳定结构[7-9]。
传统后正中入路经棘突沿椎板向两侧剥离并牵开椎旁肌群,直接显露椎板、关节突关节,手术视野较大,解剖关系显露清楚。然而,研究发现术中对椎旁肌的广泛剥离易造成脊神经后内侧支和腰动脉损伤,其并发症影响患者恢复[10-12]。有学者对Wiltse入路与传统后正中入路治疗腰椎退行性疾病的疗效进行Meta分析,发现Wiltse入路与传统后正中入路相比具有出血少、术后住院时间短、腰背痛残留率低、功能恢复好等优点[11]。本研究同样发现,术后6个月及术后2年,Wiltse入路组腰痛VAS评分优于传统后正中入路组。这是由于L3以下椎体位置较深,尤其是L5、S1,在显露时往往需要广泛剥离椎旁肌,以达到充分显露手术野的目的,剥离后的软组织在操作中需要长时间用撑开器强力撑开,增加了椎旁肌缺血损伤的发生率,而且对手术邻近节段的肌肉也易造成牵拉伤。影像学研究发现,Wiltse入路对椎旁肌的损伤要小于传统后正中入路[10-13]。Tsutsuminoto等[13]报道采用椎旁肌间隙入路与后正中入路治疗腰椎滑脱症,通过对比两组椎旁肌肉损伤和影像学指标,发现椎旁肌间隙入路组肌萎缩和变性更少。
准确定位多裂肌和最长肌肌间隙是Wiltse入路的关键。Wiltse等[2]通过解剖学研究发现,在L4以上,筋膜切口应该位于中线旁2 cm,确定肌间隙后以手指探查,确认上关节突后再分离进入;在L4以下,虽然肌间隙更加明显,但是与中线的距离较大。Vialle等[7-8]认为,L4以下肌间隙与中线的距离个体差异较大,容易出血,手术时需要注意。Olivier等[9]通过对20具尸体进行解剖分析,其中后正中入路10例,椎旁肌间隙入路10例,发现椎旁肌间隙血管分布少,而且在下腰椎水平距离正中线3 cm处血管分布更少,此处进入更为合适。对于该肌间隙距正中线的距离,Warren等[14]则认为术前应进行MRI检查,结合在MRI上进行的测量更为妥当,这一观点也得到越来越多学者的认可[15-16]。本组的做法是于正中旁开3 cm附近寻找多裂肌与最长肌肌间隙,然后分离进入手术区域。
本研究显示,采用Wiltse入路患者在术中出血量、术后引流量、住院天数、术后腰痛VAS评分方面要优于传统入路组,这说明该入路手术治疗腰椎退行性变疾病时,在加快围手术期恢复和减少手术创伤方面具有较大的优势。在远期恢复方面,本研究结果显示,2年时随访腰痛VAS评分优于传统后路手术,说明其在腰痛的改善方面优于传统入路组。可能原因为Wiltse入路减小切口及剥离范围,降低了对腰椎后韧带复合体在腰椎屈伸、旋转以及平衡稳定性方面的影响,避免了脊柱不稳导致的下肢神经根症状。2组在手术时间上并无明显差异,可能原因为经Wiltse入路手术野较小,术者操作空间不大,术中随时需要调整牵开角度,需要多人参与手术,而助手观察深部情况的角度有限,增加了手术的难度和操作时间,随着技术的成熟及手术器械的改进,Wiltse入路手术时间可能会少于传统手术入路[17]。
值得注意的是,腰椎中央管狭窄、椎管内马尾神经病变、腰椎感染范围较大以及广泛转移的脊柱肿瘤等患者都不适宜采用Wiltse入路,因为该入路并不就近,反而增加了手术操作距离,提高了手术的难度。
综上所述,采用Wiltse入路手术治疗LDH相对于传统后正中入路而言,显露简单直接,创伤小,出血少,手术效果好,对于不需要椎管减压的LDH患者是一种值得选择的手术方式。
| [1] | Wiltse LL, Bateman JG, Hutchinson RH, et al. The paraspinal sacrospinalis-splitting approach to the lumbar spine[J]. J Bone Joint Surg Am, 1968, 50(5): 919–926. DOI:10.2106/00004623-196850050-00004 |
| [2] | Wiltse LL, Spencer CW. New uses and refinements of the paraspinal approach to the lumbar spine[J]. Spine (Phila Pa 1976), 1988, 13(6): 696–706. DOI:10.1097/00007632-198813060-00019 |
| [3] | Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127–1131. |
| [4] | Fairbank JC, Couper J, Davies JB, et al. The Oswestry low back pain disability questionnaire[J]. Physiotherapy, 1980, 66(8): 271–273. |
| [5] | Fukui M, Chiba K, Kawakami M, et al. Japanese Orthopaedic Association Back Pain Evaluation Questionnaire. Part 2. Verification of its reliability:The Subcommittee on Low Back Pain and Cervical Myelopathy Evaluation of the Clinical Outcome Committee of the Japanese Orthopaedic Association[J]. J Orthop Sci, 2007, 12(6): 526–532. DOI:10.1007/s00776-007-1168-4 |
| [6] | Watkins MB. Posterolateral bonegrafting for fusion of the lumbar and lumbosacral spine[J]. J Bone Joint Surg Am, 1959, 41-A(3): 388–396. |
| [7] | Vialle R, Court C, Khouri N, et al. Anatomical study of the paraspinal approach to the lumbar spine[J]. Eur Spine J, 2005, 14(4): 366–371. DOI:10.1007/s00586-004-0802-5 |
| [8] | Vialle R, Wicart P, Drain O, et al. The Wiltse paraspinal approach to the lumbar spine revisited:an anatomic study[J]. Clin Orthop Relat Res, 2006, 445: 175–180. |
| [9] | Olivier E, Beldame J, Ould Slimane M, et al. Comparison between one midline cutaneous incision and two lateral incisions in the lumbar paraspinal approach by Wiltse:a cadaver study[J]. Surg Radiol Anat, 2006, 28(5): 494–497. DOI:10.1007/s00276-006-0123-y |
| [10] | Waschke A, Hartmann C, Walter J, et al. Denervation and atrophy of paraspinal muscles after open lumbar interbody fusion is associated with clinical outcome-electromyographic and CT-volumetric investigation of 30 patients[J]. Acta Neurochir(Wien), 2014, 156(2): 235–244. DOI:10.1007/s00701-013-1981-9 |
| [11] | 冉兵, 严磊, 蔡林. Wiltse入路与传统后正中入路手术治疗腰椎退行性疾病疗效的Meta分析[J]. 中南大学学报(医学版), 2015, 40(1): 90–101. DOI:10.11817/j.issn.1672-7347.2015.01.015 |
| [12] | 陈宣煌, 许卫红, 胡建伟, 等. 小切口椎旁肌间隙入路和传统开放式入路腰椎后路融合术的比较[J]. 脊柱外科杂志, 2012, 10(2): 101–104. |
| [13] | Tsutsumimoto T, Shimogata M, Ohta H, et al. Mini-open versus conventional open posterior lumbar interbody fusion for the treatment of lumbar degenerative spondylolisthesis:comparison of paraspinal muscle damage and slip reduction[J]. Spine(Phila Pa 1976), 2009, 34(18): 1923–1928. DOI:10.1097/BRS.0b013e3181a9d28e |
| [14] | Warren A, Prasad V, Thomas M. Pre-operative planning when using the Wiltse approach to the lumbar spine[J]. Ann R Coll Surg Engl, 2010, 92(1): 74–75. DOI:10.1308/rcsann.2010.92.1.74 |
| [15] | Palmer DK, Allen JL, Williams PA, et al. Multilevel magnetic resonance imaging analysis of multifidus-longissimus cleavage planes in the lumbar spine and potential clinical applications to Wiltse's paraspinal approach[J]. Spine(Phila Pa 1976), 2011, 36(16): 1263–1267. DOI:10.1097/BRS.0b013e3181f520e8 |
| [16] | Deng X, Zhu Y, Wang S, et al. CT and MRI determination of intermuscular space within lumbar paraspinal muscles at different intervertebral disc levels[J]. PLoS One, 2015, 10(10): e0140315.. DOI:10.1371/journal.pone.0140315 |
| [17] | Tian NF, Wu YS, Zhang XL, et al. Minimally invasive versus open transforaminal lumbar interbody fusion:a meta-analysis based on the current evidence[J]. Eur Spine J, 2013, 22(8): 1741–1749. DOI:10.1007/s00586-013-2747-z |
 2017, Vol.15
2017, Vol.15  Issue(5): 274-278
Issue(5): 274-278

