2. 军委政治工作部原机关门诊部, 北京 100120
2. Department of Organ Outpatient, Political Work Department of Central Military Commission, Beijing 100120, China
骨质疏松性椎体压缩骨折(OVCF)是骨质疏松症导致的严重后果之一[1]。经皮椎体后凸成形术(PKP)常用于治疗OVCF,该方法通过向椎体内注入填充材料来强化椎体,使压缩的椎体部分恢复,矫正后凸畸形,稳定脊柱并止痛[2]。但PKP术后常发生邻近椎体骨折,椎体自身力学因素、骨水泥用量和骨水泥渗漏等均与邻近椎体骨折的发生相关[3]。本研究应用中间椎体压缩骨折的体外骨质疏松五联椎体模型,模拟经单侧(右侧)穿刺的PKP,注入不同剂量的骨水泥后得出相关力学数据,探讨骨水泥用量与椎体生物力学之间的关系。
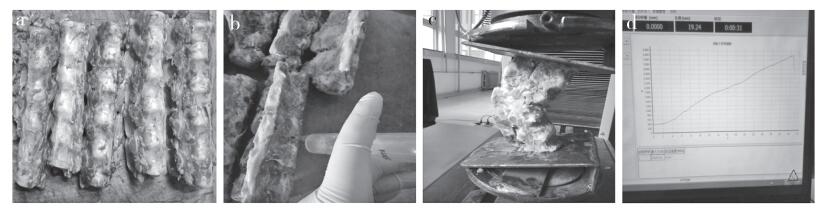
1 材料与方法 1.1 实验材料模型取自普通肉食猪的脊柱胸腰段椎体,节段为T12~L2,称之为五联椎体脊柱单元(图 1a)。经过处理、固定、筛选后共选取60具符合实验要求的脊柱单元,随机分为A、B、C、D 4组,每组15具。
|
a:五连椎体脊柱单元b:中间椎体脱钙c:中间椎体Ⅱ度压缩骨折模型制备d:载荷-位移曲线 a:Extracorporal quintuplet osteoporosis vertebral model b:Decalcification of middle vertebral body c:Preparation ofⅡdegree compression fracture model d:Load-displacement curve 图 1 模型的制备 Figure 1 Preparation of model |
分别称取183 g EDTA-Na2和20 g NaOH,将两者混匀后加入800 mL蒸馏水,剧烈搅拌,直至粉剂完全溶解后定容至1 000 mL,检测其pH值约为7.0,浓度为0.491 6 mmol/L。用此法大量配制EDTA-Na2脱钙液备用。将脊柱单元的中间椎体经双侧椎弓根打孔后,使用20 mL空针抽取配制好的EDTA-Na2脱钙液,从一侧椎弓根打孔处向内缓慢推注,使脱钙液从另外一侧椎弓根孔处流出,重复此步骤2次/d,共脱钙3周(图 1b)。
采用电子力学实验机并配合自制压缩模具,先用1 mm/min的加载速度预压,当显示屏上显示的试验力达到100 N时停止加压,并重新将实验力调零。采用5 mm/min的负荷加载速度进行压缩,实验力精确度设置为0.01 N,位移精确度设置为0.05 mm,当中间椎体的高度被压缩至原高度的50%(图 1c)时停止压缩;判断椎体出现塌陷或压缩性骨折的标准是电脑屏幕上实时生成的载荷-位移曲线上出现了波峰,即椎体的抗压力在达到最大值后开始出现下降。压力和线性位移分别由设置在实验机内的传感器同步记录并输出到计算机软件中,并实时生成每个时相的载荷-位移曲线;根据曲线上出现的波峰拐点(载荷-位移曲线最高处的载荷数值)及曲线的斜率(载荷为弹性范围内曲线的斜率)得出各组脊柱单元的极限抗压强度(S)及刚度(R)(图 1d)。A组脊柱单元压缩完成后行伤椎椎体手法复位。然后将所有脊柱单元放置于0.491 6 mmol/L的EDTA-Na2脱钙液中浸泡3周,3周后再次行骨密度检测,记录每个脊柱单元的骨密度值。
1.3 PKP术操作在C形臂X线机辅助透视下,将B、C、D 3组脊柱单元行经右侧椎弓根穿刺PKP术,穿刺针深入至骨折椎体前中1/3交界处,插入导丝后退出穿刺针并插入工作套管,插入球囊后,分别将B、C、D组伤椎椎体体积撑大其测量体积的15%、25%、35%,并相应地将调配好的骨水泥在粘丝期时经工作套管缓慢注入伤椎,B、C、D组伤椎骨水泥注入量分别为其测量体积的15%、25%、35%,观察骨水泥有无渗漏并记录渗漏情况。其中脊柱单元中央椎体的体积计算方法:v = πr2h,r=(d1+ d2)/4;d1为椎体前后径,d2为椎体左右径,h为椎体高度。
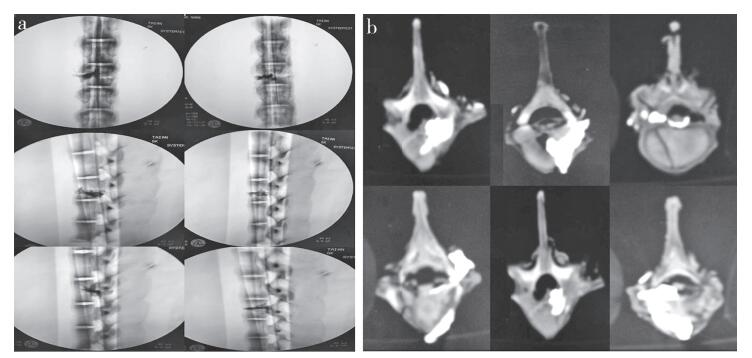
1.4 观察骨水泥渗漏情况骨水泥出现椎旁渗漏情况一般可用肉眼直接观察;骨水泥若发生椎管内渗漏或椎间盘渗漏则通过X线片以及CT扫描后观察分析而得出(图 2)。只要存在任意一种类型的骨水泥渗漏情况都统计为发生骨水泥渗漏。
|
a:X线片b:CT扫描 a:Roentgenograph b:CT scanning 图 2 骨水泥渗漏情况观察 Figure 2 Observation of bone cement leakage |
采用电子力学实验机并配合自制压缩模具进行力学压缩实验。载荷-位移曲线第1次出现显著波峰时的实验力数值即为强化后脊柱单元的极限抗压强度(S’),此期间弹性范围内曲线斜率为强化后脊柱单元的刚度(R’)。由于A组脊柱单元未行PKP,对其统计新发骨折椎体位置无意义,故A组脊柱单元得出S’和R’后压缩停止。B、C、D组脊柱单元得出S’和R’后实验机继续施加压力,出现第1个新发的骨折椎体时实验继续,出现第2个新发的骨折椎体(去除伤椎本身)时,停止压缩,观察并记录新发骨折椎体的位置。
1.6 统计学处理采用SPSS 18.0软件对数据进行统计学分析,结果用x±s表示,组间差异采用单因素方差分析进行比较,组内差异采用配对样本t检验进行比较;对新发骨折情况及骨水泥渗漏情况的比较采用χ2检验。以P < 0.05为差异有统计学意义。
2 结果 2.1 骨质疏松模型建立情况60个脊柱单元脱钙前骨密度为(1.058±0.013)g/cm2,脱钙后为(0.613±0.044)g/cm2,下降率 > 40%,证明脊柱单元中央椎体骨质疏松模型建立。
2.2 各组极限抗压强度和刚度的比较由表 1可见,B、C、D组强化后的刚度均优于A组,差异有统计学意义(P < 0.05);说明行PKP注入骨水泥后,可恢复脊柱单元的刚度,且随着骨水泥用量增大,刚度值也增大。B、C、D组强化后的极限抗压强度均大于A组,差异有统计学意义(P < 0.05);表明骨水泥的注入使伤椎得到强化,在脊柱单元整体的极限抗压强度方面得到显著改善,但随着骨水泥用量增大,脊柱单元极限抗压强度随之减小。
|
|
表 1 极限抗压强度及刚度 Table 1 Ultimate compressive strength and rigidity |
B、C、D组强化椎相邻位置新发骨折椎体的个数分别为17、21、27,经χ2检验,认为新发骨折椎体情况差异有统计学意义(P < 0.05),强化椎骨水泥用量越高,越易发生强化椎邻近椎体骨折。
2.4 骨水泥渗漏情况B、C、D组发生骨水泥渗漏的椎体个数分别为1、3、11,经χ2检验,认为骨水泥渗漏情况差异有统计学意义(P < 0.05),表明PKP术中,骨水泥渗漏的发生率与注射剂量有关,随着骨水泥用量加大而显著提高。
3 讨论OVCF在行PKP后再发骨折影响因素比较复杂,张伟等[3]指出与再发骨折相关的临床因素可归纳为两大类:一类是椎体本身因素,如椎体骨质疏松状态的持续存在或加重、椎体自身结构的改变(包括后凸角、椎体刚度与强度)等,另一类是外部因素,如手术方式,填充材料的类型,骨水泥的注射方式、注射量、分布形态、渗漏状况以及后期药物治疗、康复功能锻炼、日常活动强度的差别等。本研究主要从骨水泥用量方面探讨PKP术后邻近节段再发骨折的原因。单就骨水泥注入量来讲,并非越多越好,适量的骨水泥灌注量能有效避免再发骨折[4]。包拥政等[5]应用三维有限元分析法,通过分析椎体成形术不同体积骨水泥注射后伤椎及其邻近椎体的应力变化,发现伤椎及其邻近椎体的应力在骨水泥注射后均较注射前明显增加,并且随着骨水泥注入量的增加,伤椎及其邻近椎体承受的应力也随之增大,故认为骨水泥的用量可能是导致邻近椎体骨折的因素之一。有学者提出由于骨质疏松患者的椎体强度普遍降低,行椎体成形术后伤椎内注入骨水泥,虽然可明显提高伤椎的极限抗压强度,但其相邻椎体的极限抗压强度并没有得到同样程度的强化,这种差距会使邻近椎体之间的强度差增大,应力更多地集中在小部分区域,使相邻椎体承受的应力载荷增大,从而更容易导致新发骨折的出现[6]。张兴州等[7]也提出,OVCF在行椎体成形术后,伤椎内大量的骨水泥填充可造成椎体间产生巨大的刚度级差,容易导致与强化椎相邻的椎体发生骨折。以上结论都与本研究结果一致。关于椎体成形术骨水泥注射量尚无统一标准,赵勇等[8]认为以止痛为主要目的的椎体成形术不必过分追求椎体高度的恢复。恢复伤椎高度可改善Cobb角,使整个脊柱单元应力接近生理状态,但过度追求伤椎高度的恢复势必造成骨水泥用量的加大。本研究发现随着骨水泥用量加大会导致骨水泥渗漏率增大,且脊柱单元极限抗压强度也随之降低,使强化椎邻近椎体更易发生骨折。Nieuwenhuijse等[9]发现当骨水泥体积分数达到24%或更高时会发生骨水泥渗漏或新发骨折,认为骨水泥的渗漏是椎体再发骨折的重要因素,他同时也提出当椎间盘骨水泥渗漏量 > 1 mL时,有96%的邻近椎体会发生骨折,椎间盘骨水泥渗漏量越大,邻近椎体再发骨折的风险越高。本研究也发现,随着骨水泥用量的增大,发生骨水泥渗漏的风险随之增大,这说明较大剂量的骨水泥注射可直接引起骨水泥渗漏率增加,并间接增大了邻近椎体再发骨折的概率。
本实验采用猪的脊柱作为实验对象,主要原因如下。①符合WHO制定的3R原则,即减少(reduction)、替代(replacement)和优化(refinement)[10];②猪为杂食动物,与人类的某些生理状态较一致,且其骨密度也与人类相近;③猪的骨组织形态及骨的重建与人类相似;④猪的椎体结构及体积与人类相似[11]。应用五联椎体单元作为实验对象,将强化椎对其他椎体的影响扩大到非邻近椎体,且实验中将脊柱单元看作一个整体,通过自制的压缩模型进行上下两侧的力学性能压缩实验,获得反映整个脊柱单元的强度与刚度值,进而达到本实验的目的。
综上所述,PKP术后骨水泥的渗漏是邻近椎体再发骨折的重要因素,为防止骨水泥渗漏的发生,骨水泥的注入量是不可忽视的重要因素之一。笔者认为应根据患者治疗需要及具体病情合理控制骨水泥的用量,在止痛及充实强化伤椎的同时,应考虑强化椎对邻近椎体力学方面的影响,在保证临床手术效果的同时,尽量减少骨水泥用量,从而降低邻近椎体骨折的发生率。本研究发现,骨水泥用量应控制在椎体体积的15%~25%,由于椎体体积测量结果的平均数为19.57 mL,故换算成骨水泥的具体用量为2.93~4.89 mL;这样既能充分提高脊柱单元的刚度及极限抗压强度,又可以降低脊柱单元再发骨折的概率。
| [1] | 王清泽, 王相利, 张金锋, 等. 椎体成形术与非手术治疗骨质疏松性椎体压缩性骨折安全性的Meta分析[J]. 脊柱外科杂志, 2016, 14(5): 306–311. |
| [2] | 何飞平, 盖景颖, 李如求. 经皮椎体后凸成形术治疗老年重度骨质疏松性椎体压缩骨折[J]. 脊柱外科杂志, 2015, 13(6): 360–363. |
| [3] | 张伟, 刘峰, 范新成. 椎体压缩骨折经皮椎体成形术后邻近节段再骨折的研究现状[J]. 中国矫形外科杂志, 2014, 22(6): 516–519. |
| [4] | Zhan Y, Jiang J, Liao H, et al. Risk factors for cement leakage after vertebroplasty or kyphoplasty:a meta-analysis of published evidence[J]. World Neurosurg, 2017, 101: 633–642. DOI:10.1016/j.wneu.2017.01.124 |
| [5] | 包拥政, 祝周兴, 冯云升, 等. 骨水泥注射体积与骨质疏松压缩性骨折椎体及邻近椎体应力的关系[J]. 中国组织工程研究, 2015, 19(52): 8365–8372. DOI:10.3969/j.issn.2095-4344.2015.52.001 |
| [6] | 张中兴, 许峰, 陈焕诗, 等. PVP术后相邻椎体骨折的因素研究进展[J]. 颈腰痛杂志, 2014, 35(1): 53–55. |
| [7] | 张兴州, 张曦. 椎体成形术后相邻椎体骨折病因与预防策略的研究进展[J]. 中国骨伤, 2010, 23(10): 792–795. |
| [8] | 赵勇, 竺湘江, 范湧, 等. 体位过伸复位联合经皮椎体后凸成形术治疗老年骨质疏松性椎体压缩骨折[J]. 中国微创外科杂志, 2013, 13(4): 336–338, 342. |
| [9] | Nieuwenhuijse MJ, Bollen L, van Erkel AR, et al. Optimal intravertebral cement volume in percutaneous vertebroplasty for painful osteoporotic vertebral compression fractures[J]. Spine(Phila Pa 1976), 2012, 37(20): 1747–1755. DOI:10.1097/BRS.0b013e318254871c |
| [10] | Simpson AH, Murray IR. Main differences in osteoporotic fracture models:which should I use?[J]. Injury, 2016, 47(Suppl 1): S15–20. |
| [11] | Engelke EC, Post C, Pfarrer CD, et al. Radiographic morphometry of the lumbar spine in Munich miniature pigs[J]. J Am Assoc Lab Anim Sci, 2016, 55(3): 336–345. |
 2017, Vol.15
2017, Vol.15  Issue(6): 361-365
Issue(6): 361-365


