2. 哈尔滨医科大学附属第四医院骨科, 哈尔滨 150001
2. Department of Orthopaedics, 4th Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang, China
腰椎椎间盘退行性变是腰椎椎间盘突出、退行性椎管狭窄、腰椎滑脱和椎间盘源性腰痛等一系列下腰痛疾病的主要病因及始动因素。椎间盘包括髓核、纤维环及上下软骨终板,腰椎软骨终板的退行性变是腰椎椎间盘发生退行性变最重要的机制[1-2]。软骨终板位于椎间盘上下界面,是椎间盘营养物质供给的重要通道。软骨终板发生退行性变不但能够引起腰背痛症状,还会直接加速椎间盘退行性变的发生[3-4]。本研究旨在探讨人类腰椎软骨终板的组织学特征,为更好地理解腰椎椎间盘退行性变的发生机制提供参考。
1 资料与方法 1.1 研究对象选取因车祸伤死亡或意外猝死的遗体捐赠者新鲜标本18具,男10具,女8具;死亡时年龄20 ~ 40岁,平均33.7岁;无腰椎骨折、腰椎椎间盘突出症、腰椎椎管狭窄症或腰椎肿瘤等腰椎疾病;无糖尿病或风湿病既往史。所有遗体捐赠者生前均签署器官捐赠同意书,符合伦理学审查标准。
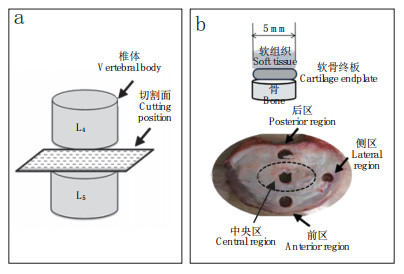
1.2 软骨终板样本制备将取下的新鲜腰椎标本用双层塑料袋密封包裹后立即置于-20℃低温冰箱中冷冻保存。用骨锤凿将标本沿横断面切割成厚约10 mm的组织厚片,保留髓核/纤维环、软骨终板、骨组织3层结构(图 1a)。用Delta机械打孔机分别在椎间盘前区、后区、中央区、侧区(图 1b)沿椎体矢状面打孔,取直径为5 mm的圆形标本,标注上下界面,观察其大体结构。启动Leica滑动式切片机降温装置,待机器操作板温度降至-20℃时,将标本放置在操作板上,利用OCT试剂冷冻包裹标本,3 min后待标本固定牢固,用滑片刀以每片5 μm厚度切割上层松质骨组织,至表面由红变白即可停止。解冻标本,翻转置于切片机,用纸巾擦掉表面融化的OCT,重复上述步骤,以每片2 μm厚度切割分离椎体终板上方的软组织部分(髓核/纤维环),确保不要切到椎体终板。
|
a:椎间盘切割面示意图 b:椎间盘取材部位示意图 a:Schematic diagram of intervertebral disc cutting position b:Schematic diagram of the intervertebral disc selection position 图 1 椎间盘切割面和取材部位示意图 Figure 1 Schematic diagram of intervertebral disc cutting and selection position |
利用高敏感测高仪测量10具标本椎体终板前区、后区、中央区、侧区的厚度,每个标本每区测量3个点,取3个点均值。利用锤凿和解剖器械取剩余8具脊柱标本中央区和后区组织块,大小约为1.0 cm×1.0 cm×0.5 cm(上层为髓核/纤维环,中层为椎体终板,下层为松质骨结构),置于4%的多聚甲醛溶液中固定5 d,于15%的EDTA溶液中脱钙4周,每周更换EDTA溶液。脱钙后常规梯度乙醇脱水,石蜡包埋,5 μm厚连续切片,HE染色,显微镜下观察、拍照。
1.4 统计学处理采用SPSS 18.0软件对数据进行统计学分析,组间差异比较采用方差分析,以P < 0.05为差异有统计学意义。
2 结果利用高敏感测高仪测量10具标本L4/L5节段8个位点共80组软骨终板厚度,终板厚度为0.696~1.045 mm,方差分析显示8个区域的终板厚度差异有统计学意义(P < 0.05),后区下部终板最厚,中央区上部最薄(表 1)。
|
|
表 1 软骨终板厚度 Table 1 Thickness of cartilage endplate |
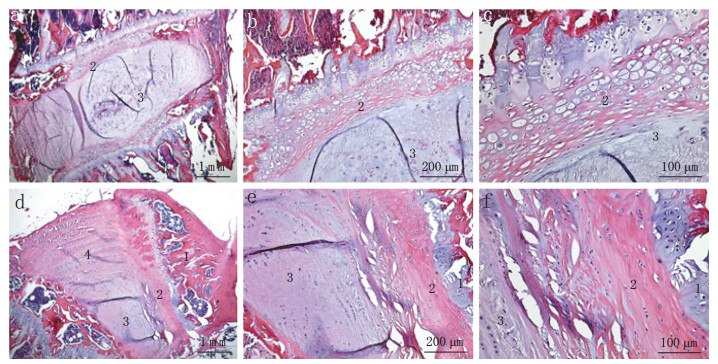
镜下观察发现,软骨终板是位于髓核/纤维环与椎体之间的薄透明软骨层,有大小不等的孔隙结构,中央区厚度小于后区,与大体实验测量结果一致。软骨终板的细胞密度比髓核和纤维环的细胞密度高,软骨终板中央区和侧区的胶原纤维比髓核和纤维环组织中的胶原纤维更加紧密(图 2)。
|
a ~ c:中央区 d ~ f:后区 1,骨 2,软骨终板 3,髓核 4,纤维环 a-c:Central region d-f: Posterior region 1, Bone 2, Cartilage endplate 3, Nucleus pulposus 4, Annulus fibrosus 图 2 腰椎软骨终板组织学形态 Figure 2 Histology of lumbar cartilage endplate |
腰椎椎间盘的退行性变与多种因素相关,如椎间盘异常的应力负荷、营养代谢障碍、基质金属蛋白酶活性增高、细胞因子的激活等[5]。软骨终板主要通过渗透作用为椎间盘供给营养物质。软骨终板的微骨折和破坏将直接导致相应的毛细血管网络受损,而终板的钙化导致其渗透性下降50% ~ 60%,这些最终都会造成椎间盘养分供应不足和代谢产物的积累[1, 6]。钙化是软骨终板发生退行性变的主要特征[7]。近年来,软骨终板退行性变在腰椎椎间盘退行性变中的作用引起学者们的关注,研究发现腰椎软骨终板的不规则形变、钙化,使蛋白多糖含量减少,阻碍了椎间盘的营养吸收,加速了腰椎椎间盘的退行性变[4, 8]。由此可见,腰椎椎间盘上下临界软骨终板层的孔状结构与椎间盘退行性变有着密切联系。
终板可分为骨性终板和软骨终板,即终板钙化层和非钙化层,2种终板具有不同类型的运输方式,终板特殊的2层结构可以更有效地发挥其运输功能[9]。从生物力学角度分析,终板可以为椎体和椎间盘提供生物力学支撑,结构致密并且厚的终板力学性能较好,但是过密或者过厚的终板则会直接导致椎间盘的营养供应障碍,从而造成椎间盘的退行性变[10-11]。软骨终板边缘较厚而中间较薄,并且在力学负载较大的区域厚于负载较小的区域。这样的解剖学结构有利于椎间盘的营养供给,但也导致了终板中央的生物力学性能下降[12]。Wu等[13]的压痕实验证明,终板的刚度和强度从外周到中心逐级降低。Gullbrand等[14]通过对动物标本的力学研究证明,适量的动态负载能够促进发生退行性变的椎间盘的物质运输,从而达到修复椎间盘的目的。Edwards等[15]测量了20具新鲜成人尸体标本腰椎软骨终板的厚度,发现腰椎软骨终板的厚度不等且差异较大,但因列入研究人群的种族差异,不具有统计学意义。Pitzen等[16]研究发现成人颈椎软骨终板厚度和Edwards等[15]的研究结果大体相同,无论腰椎还是颈椎的软骨终板,其中央区域都是最薄的,且伴有大量孔隙结构。这与本实验研究结果一致,健康成人腰椎与颈椎软骨终板的形态学方面具有相似性。
腰椎软骨终板的解剖学形态、生物力学特性与软骨终板的退行性变是互相关联的,椎间盘从机体获取营养最主要的途径是软骨终板的弥散功能,如果腰椎软骨终板受内外环境的影响而受损,必然会对腰椎椎间盘的营养代谢产生重要影响[17]。Dudli等[18]研究发现腰椎软骨终板越厚,越容易造成椎间盘营养供给的缺失;但是腰椎软骨终板越薄,其生物力学性能就越差。同一终板的外周密度相对较高,前方区域与中央区域密度相对较低,密度最高处是后外侧区域[19]。完整的软骨终板可以防止椎间盘破裂及纤维环撕裂,维护椎间盘统一的应力分布,调节椎间盘营养物质和代谢产物的运输[1, 3-4]。
综上,腰椎软骨终板的组织学特点与椎间盘的营养供应相关,发生退行性变的终板可以影响并加速腰椎椎间盘的退行性变。阐明腰椎软骨终板发生退行性变的机制有助于理解腰椎椎间盘退行性变的始发理论因素,为建立新的腰椎椎间盘退行性变临床诊断思路和治疗策略提供依据。
| [1] | DeLucca JF, Cortes DH, Jacobs NT, et al. Human cartilage endplate permeability varies with degeneration and intervertebral disc site[J]. J Biomech, 2016, 49(4): 550–557. |
| [2] | Crockett MT, Kelly BS, Van Baarsel S, et al. Modic type 1 vertebral endplate changes:injury, inflammation, or infection?[J]. AJR Am J Roentgenol, 2017, 209(1): 167–170. DOI:10.2214/AJR.16.17403 |
| [3] | Lotz JC, Fields AJ, Liebenberg EC. The role of the vertebral end plate in low back pain[J]. Global Spine J, 2013, 3(3): 153–164. DOI:10.1055/s-0033-1347298 |
| [4] | Yuan W, Che W, Jiang YQ, et al. Establishment of intervertebral disc degeneration model induced by ischemic sub-endplate in rat tai[J]. Spine J, 2015, 15(5): 1050–1059. DOI:10.1016/j.spinee.2015.01.026 |
| [5] | 王海生, 官建中. 椎间盘软骨终板退变的研究进展[J]. 中国矫形外科杂志, 2016, 24(5): 436–438. |
| [6] | 孙毅, 吕松岑. 腰椎椎体终板的特征与临床意义的研究进展[J]. 医学综述, 2016, 22(2): 301–303. DOI:10.3969/j.issn.1006-2084.2016.02.027 |
| [7] | Xu HG, Zheng Q, Song JX, et al. Intermittent cyclic mechanical tension promotes endplate cartilage degeneration via canonical Wnt signaling pathway and E-cadherin/β-catenin complex cross-talk[J]. Osteoarthritis Cartilage, 2016, 24(1): 158–168. |
| [8] | Wang YX, Griffith JF. Menopause causes vertebral endplate degeneration and decrease in nutrient diffusion to the intervertebral discs[J]. Med Hypotheses, 2011, 77(1): 18–20. DOI:10.1016/j.mehy.2011.03.014 |
| [9] | Yamaguchi T, Goto S, Nishigaki Y, et al. Microstructural analysis of three-dimensional canal network in the rabbit lumbar vertebral endplate[J]. J Orthop Res, 2015, 33(2): 270–276. DOI:10.1002/jor.v33.2 |
| [10] | Zehra U, Robson-Brown K, Adams MA, et al. Porosity and thickness of the vertebral endplate depend on local mechanical loading[J]. Spine (Phila Pa 1976), 2015, 40(15): 1173–1180. DOI:10.1097/BRS.0000000000000925 |
| [11] | Berg-Johansen B, Han M, Fields AJ, et al. Cartilage endplate thickness variation measured by ultrashort echo-time MRI is associated with adjacent disc degeneration[J]. Spine(Phila Pa 1976), 2018, 43(10): E592–E600. DOI:10.1097/BRS.0000000000002432 |
| [12] | Liu J, Hao L, Suyou L, et al. Biomechanical properties of lumbar endplates and their correlation with MRI findings of lumbar degeneration[J]. J Biomech, 2016, 49(4): 586–593. |
| [13] | Wu Y, Cisewski SE, Sun Y, et al. Quantifying baseline fixed charge density in healthy human cartilage endplate:a two-point electrical conductivity method[J]. Spine (Phila Pa 1976), 2017, 42(17): E1002–E1009. DOI:10.1097/BRS.0000000000002061 |
| [14] | Gullbrand SE, Peterson J, Ahlborn J, et al. ISSLS prize winner:dynamic loading-induced convective transport enhances intervertebral disc nutrition[J]. Spine(Phila Pa 1976), 2015, 40(15): 1158–1164. DOI:10.1097/BRS.0000000000001012 |
| [15] | Edwards WT, Zheng Y, Ferrara LA, et al. Structural features and thickness of the vertebral cortex in the thoracolumbar spine[J]. Spine (Phila Pa 1976), 2001, 26(2): 218–225. DOI:10.1097/00007632-200101150-00019 |
| [16] | Pitzen T, Schmitz B, Georg T, et al. Variation of endplate thickness in the cervical spine[J]. Eur Spine J, 2004, 13(3): 235–240. DOI:10.1007/s00586-003-0648-2 |
| [17] | Määttä JH, Wadge S, MacGregor A, et al. ISSLS prize winner:vertebral endplate(modic) change is an independent risk factor for episodes of severe and disabling low back pain[J]. Spine(Phila Pa 1976), 2015, 40(15): 1187–1193. DOI:10.1097/BRS.0000000000000937 |
| [18] | Dudli S, Haschtmann D, Ferguson SJ. Fracture of the vertebral endplates, but not equienergetic impact load, promotes disc degeneration in vitro[J]. J Orthop Res, 2012, 30(5): 809–816. DOI:10.1002/jor.v30.5 |
| [19] | Wu Y, Cisewski SE, Wegner N, et al. Region and strain-dependent diffusivities of glucose and lactate in healthy human cartilage endplate[J]. J Biomech, 2016, 49(13): 2756–2762. |
 2019, Vol.17
2019, Vol.17  Issue(1): 47-50
Issue(1): 47-50


