随着人口的老龄化,腰椎退行性疾病已成为影响人们日常生活的常见病之一,其发生率在老年人群中 > 50%[1]。腰椎融合术在临床上被证实为是治疗腰椎退行性疾病的有效方法,微创路径下完成椎间盘切除、椎体间融合是近年来兴起的一种治疗腰椎退行性疾病的新方法,较传统腰椎开放性手术具有创伤小、融合效果确切、最大限度保持术后脊柱稳定性、降低腰椎手术失败综合征发生率等优点[2-3]。微创腰椎椎间融合术主要包括微创经椎间孔入路腰椎椎间融合术(MIS-TLIF)与极外侧入路腰椎椎间融合术(XLIF)。目前已有不少研究比较了这2种微创术式与传统开放手术的安全性及有效性,如MIS-TLIF与传统TLIF的比较[4-5]、XLIF与前路腰椎椎间融合术的比较等[6-7],但国内尚未见有关这2种微创术式临床疗效比较的报道。本研究旨在比较MIS-TLIF和XLIF治疗腰椎退行性疾病近期临床疗效,为微创外科选择最佳手术方法提供参考。
1 资料与方法 1.1 临床资料回顾性分析2013年3月—2014年6月收治的微创手术指征明确的单节段或连续双节段腰椎退行性疾病患者临床资料。纳入标准:①年龄≥18岁;②临床表现为严重的下肢放射痛和/或间歇性跛行伴/不伴腰痛;③影像学提示典型L1~5单节段或连续双节段的腰椎Ⅰ度或Ⅱ度滑脱合并中央型椎管狭窄或侧隐窝狭窄,有明确的椎间融合指征;④经过≥6个月的严格非手术治疗无效或症状逐渐加重。排除标准:①临床症状和影像学表现不相符;②影像学提示椎间盘纤维环破裂或椎间隙塌陷、椎间隙明显变窄;③合并类风湿性关节炎、强直性脊柱炎等自身免疫性疾病;④有腰部手术、骨折、感染、肿瘤史;⑤因各种原因不能行MRI检查;⑥患有其他严重的全身系统性疾病不能手术。根据以上标准共纳入患者75例,其中行MIS-TLIF者36例,行XLIF者39例,2组患者术前一般资料差异无统计学意义(P > 0.05,表 1),具有可比性。
|
|
表 1 一般资料 Table 1 General information |
患者全身麻醉后取俯卧位,根据椎弓根体表投射点,经多裂肌与最长肌间隙入路,用1号空心套管触及病变节段的关节突关节,随后逐级置入扩张套管,建立扩张通道系统,安装固定装置及专用冷光源。显露病变节段椎板外缘和上下关节突关节,透视确认无误后,在病变节段上下椎体双侧各置入2枚椎弓根螺钉。用椎板咬钳沿上关节突外侧缘向内咬除上下关节突及部分椎板,切除相应的黄韧带,显露突出的椎间盘、神经根及硬膜囊,探查神经根管,狭窄者予以充分减压。将减压咬下的自体骨块或同种异体骨块修剪后植入椎间隙,或将填满骨粒的单枚椎间融合器斜行置入椎间隙。最后以裁剪和预弯的钛棒连接双侧椎弓根螺钉,探查无活动性出血后,在硬膜表面覆盖明胶海绵防止硬膜粘连,逐层关闭手术切口。
1.2.2 XLIF患者全身麻醉后取标准90°右侧卧位,调整腰桥以张开髂嵴至肋缘间距,髋关节屈曲。根据术前透视确认并标记切口(位于左侧腋中线病变椎间盘的中心点或稍偏前),切口长30 mm,切开皮肤及深筋膜,以手指经肌层钝性分离至腹膜后间隙,触及椎体侧方。经切口插入导针和初级扩张管,透视确认导针和初级扩张管位于病变椎间盘侧位中心点或偏前位置(L4/L5节段通常位于椎间盘前中1/3交界处)。依次逐级递增旋转插入扩张管,分离扩张腰大肌肌束,使其到达椎间盘侧面。扩张管在腰大肌前中1/3间走行,使腰丛位于扩张通道后方。置入通道管,连接自由臂,固定并撑开工作通道,暴露椎体及椎间盘侧方,撑开后的工作通道不超越椎体前后缘。再次直视下确认腰丛未被卷入手术通道内,并透视确认通道位置准确。切开病变椎间盘侧方纤维环,逐级刮除椎间盘及上下终板至软骨下骨。注意避免过度处理终板,以免造成术后植骨与融合器下沉。处理椎间盘需贯通至对侧,并采用Cobb剥离器松解对侧纤维环。将自体骨或人工骨材料填入椎间融合器,将融合器置入椎间隙,其长轴朝向对侧。透视下确认融合器位置完全占据椎间隙前中部且边缘被上下终板边缘硬骨质覆盖。患者改俯卧位,透视下确认椎体椎弓根穿刺点(通常以透视标准正位椎体及其相邻椎体双侧椎弓根卵圆形影外缘连线与该椎体横突中线的交点为穿刺点)。用空心穿刺套管针穿刺椎弓根,经空心穿刺针将导针置入椎弓根内。取出穿刺针,将经皮椎弓根螺钉沿左右椎弓根穿刺口的导针拧入椎体。透视确认螺钉位置良好,取出导针。自一端切口沿肌层深处置入预弯棒,并确认其位于椎弓根钉槽内,拧入螺帽固定,透视确认固定良好,逐层关闭手术切口。
1.3 观察指标围手术期记录手术时间、术中出血量。术前及术后6周、3个月、6个月、1年、2年,采用视觉模拟量表(VAS)评分[8]评估腰痛及下肢痛,采用Oswestry功能障碍指数(ODI)[9]评估腰痛对日常活动的影响,采用SF-36量表[10]评估生活质量(包括生理评分和心理评分),并调查患者对手术的满意度(“非常满意或者稍微满意”视为“满意”,“非常不满意或者稍微不满意”视为“不满意”)。在围手术期及随访期间及时记录相关并发症及再次手术的相关情况并做相关处理。
1.4 统计学处理采用SPSS 21.0软件对数据进行统计学分析。计量资料以x±s或中位数表示,组间比较采用独立样本t检验或非参数检验,各组内不同随访时间点的比较采用重复测量方差分析;率的比较采用χ2检验;以P < 0.05为差异有统计学意义。
2 结果所有患者均由同一组脊柱外科医师顺利完成手术,典型病例影像学资料见图 1,2。所有患者随访 > 2年。MIS-TLIF组与XLIF组行单节段融合的患者分别为32例和30例,行双节段融合的患者分别为4例和9例。MIS-TLIF组中位手术时间为169(82~ 406)min,XLIF组中位手术时间为182(92 ~ 336)min,2组差异无统计学意义(P > 0.05);MIS-TLIF组术中出血量为70 ~ 130(90±20)mL,XLIF组为30 ~ 70(50±10)mL,XLIF组明显低于MIS-TLIF组,差异有统计学意义(P < 0.05)。
|
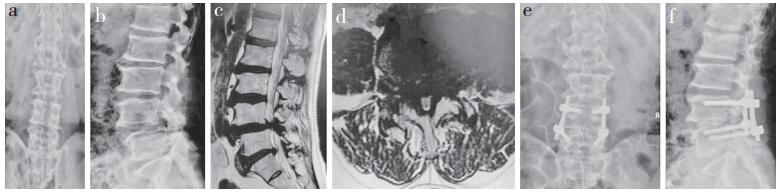
a,b:术前正侧位X线片 c,d:术前矢状面和横断面MRI e,f:术后3个月正侧位X线片 a, b:Preoperative anteroposterior and lateral roentgenographs c, d:Preoperative saggital and transverse plane MRIs e, f:Anteroposterior and lateral roentgenographs at postoperative 3 months 图 1 MIS-TLIF组典型病例影像学资料 Figure 1 Radiologic data of a typical case in MIS-TLIF group |
|
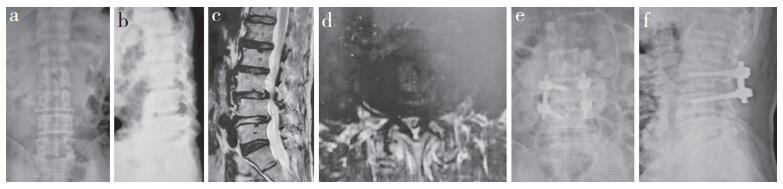
a,b:术前正侧位X线片 c,d:术前矢状面和横断面MRI e,f:术后3个月正侧位X线片 a, b:Preoperative anteroposterior and lateral roentgenographs c, d:Preoperative saggital and transverse plane MRIs e, f:Anteroposterior and lateral roentgenographs at postoperative 3 months 图 2 XLIF组典型病例影像学资料 Figure 2 Radiologic data of a typical case in XLIF group |
2组各时间点观察指标见表 2。术前2组患者下肢痛和腰痛VAS评分、ODI及SF-36评分差异均无统计学意义(P > 0.05);2组患者术后6周、3个月、6个月、1年、2年下肢痛和腰痛VAS评分、ODI及SF-36评分均较术前明显改善,差异有统计学意义(P < 0.05);但组间差异均无统计学意义(P > 0.05)。MIS-TLIF组术后2年患者满意度为91.7%(33/36),XLIF组为92.3%(36/39),差异无统计学意义(P > 0.05)。
|
|
表 2 观察指标 Table 2 Observation index |
MIS-TLIF组患者术后均未出现髋部屈肌肌力减弱表现;2例(5.6%)出现下肢皮肤浅感觉减退,术后1年完全恢复。XLIF组中有9例(23.1%)术后出现髋部屈肌肌力减弱,术后6个月完全恢复,未经特殊处理;3例(7.7%)出现下肢皮肤感觉减退,术后1年完全恢复。随访2年,2组患者均未行翻修手术。
3 讨论近年来,关于微创技术,尤其是对于腰椎退行性疾病微创治疗的临床疗效研究,主要集中在微创技术与传统开放手术疗效的比较,多数研究一致认为微创手术具有软组织损伤小、周围结构破坏少、临床疗效可靠、术中出血量少、住院时间短、并发症少等优势[12-13]。目前,由于器械的不同,产生了多种微创术式,对于相同的部位、相同的疾病可选择不同的微创术式,因此,对于同一种腰椎退行性疾病,如何选择一种优化的微创术式,对于临床医师来说是一个挑战。国外文献报道,MIS-TLIF和XLIF分别通过直接减压和间接减压的方式治疗退行性腰椎滑脱合并椎管狭窄,且中远期临床疗效相似[5, 14-15]。本研究对MIS-TLIF与XLIF治疗腰椎退行性疾病的近期临床疗效进行了比较。
MIS-TLIF是在传统TLIF的基础上,通过可扩张通道,以更小的切口提供足够的手术视野,减少椎旁肌肉的剥离,降低对椎旁肌肉、周围血管及神经结构的破坏[2, 16-17]。MIS-TLIF仅行一侧减压,最大限度保留脊柱结构完整性,减小手术瘢痕形成,为再次手术提供条件。术中部分切除上位椎体下关节突及下位椎体上关节突,直接暴露硬膜囊及神经根,使用神经根拉钩牵开硬膜囊及神经根,暴露椎间盘,切除增生骨赘及椎间盘组织,植骨后置入椎间融合器,对硬膜囊及神经根进行直接减压。XLIF是近年来出现的经外侧穿过腹膜后间隙和腰大肌到达腰椎的一种新的微创技术[18-20]。与传统的前路手术相比,该技术的优点在于不经腹腔,不需要分离大血管和神经丛,大大减少了并发症的发生。XLIF可置入椎间融合器,恢复椎体高度,间接改善椎间孔的容积从而减少放射痛的发生。该术式不破坏前、后纵韧带,使脊柱的生物力学稳定性得以维持;前路置入融合器有利于改善和维持脊柱矢状面平衡,有利于双侧终板的恢复,从而矫正冠状面平衡。本研究结果提示,2种术式治疗腰椎退行性疾病,患者术后下肢痛和腰痛VAS评分、ODI及SF-36生活质量评分均获得明显改善,组间差异无统计学意义。
本研究中,MIS-TLIF组中有2例术后出现下肢皮肤浅感觉减退,分析其原因:①手术视野受限,且术中需要特殊外科器械,造成神经根牵拉,降低神经根的血流供应,引起神经功能损伤;②内置物直接损伤神经根[21-22]。根据笔者的经验,降低神经根牵拉的时间和张力,在椎间隙准备和置入物放置过程轻柔操作、注意保护神经等措施可降低神经损伤发生率;遇到巨大椎间盘突出,神经根受压严重无移动余地时,可从对侧容易暴露处将椎间盘摘除,使神经根张力降低后再从突出侧探查;正确的置钉方法和术中影像学监测螺钉的位置有助于进一步避免和及时发现置钉位置错误和可能造成的神经损伤。XLIF组中有9例术后出现髋部屈肌肌力减弱,3例出现下肢皮肤感觉减退,分析其原因主要是极外侧入路对腰神经丛及其分支(如生殖股神经、股外侧皮神经等)的损伤,手术牵拉神经时间过长及建立工作通道时腰大肌被过度扩张等。一项关于XLIF并发症的大样本研究指出,600例接受XLIF治疗的患者围手术期并发症总体发生率为6.2%,其中4例(0.7%)出现术后一过性运动神经损伤表现,11例(1.8%)需附加其他手术方式或翻修;其中大腿前方痛或髋部屈肌肌力减弱的表现非常普遍。但在6周内症状逐渐消失,且认为术中腰大肌损伤是直接相关因素[23]。结合笔者经验及既往相关研究[24-26],可从以下几方面来降低手术相关并发症的发生率。①提高微创手术操作技能,丰富操作经验,并对脊柱的解剖结构有深入的认识和理解。②术中在建立极外侧入路工作通道时一定要强调椎间盘入针处精确位于侧位椎间盘前后中点处或稍偏前,并及时行正侧位透视确认;保持屈髋体位,此举可松弛腰大肌,减少扩张时损伤,同时神经松弛使肌肉易被牵开。③熟悉手术入路中的解剖结构,直视下仔细观察术野中与神经相似的组织,小心操作,尽可能避免过度牵拉腰大肌与压迫周围软组织,条件允许情况下术中应用肌电图监测。术中应用神经监测仍有运动神经损伤情况的发生,尤其是L4/L5节段;术前静脉注射10 mg地塞米松可预防神经损伤的发生,明显降低一过性运动神经损伤的发生率。
本研究不足之处:①微创术式为患者自愿选择,不是随机分组,因此可能存在一定的选择偏倚;但2组患者基本资料比较差异无统计学意义,具有可比性。②本研究样本量较少,无法更普遍及细致地对2种手术之间的细微差异进行详细比较,以至于本研究结论存在一定局限性;但2组患者随访期间疗效差异无统计学意义,因此,该结论可在临床中作为参考。③由于解剖结构的原因,XLIF无法在L5/S1节段实施;但L5/S1节段却是腰椎椎间融合术常见手术节段,本研究为控制研究的可比性,未纳入L5/S1节段患者。
综上所述,本研究对MIS-TLIF与XLIF的近期疗效进行对比研究,虽然2种术式减压机制不同,但2年随访的近期疗效无显著差异。MIS-TLIF术中的出血量高于XLIF,但平均出血量均 < 100 mL;XLIF术后髋部屈肌肌力减弱发生情况多于MIS-TLIF,但症状均为暂时性,最终均完全改善;同时,随访2年,2组患者均未行手术翻修,且满意度均较高,提示MIS-TLIF与XLIF都是治疗腰椎退行性疾病的有效微创术式。
| [1] | Villavicencio AT, Burneikiene S, Roeca CM, et al. Minimally invasive versus open transforaminal lumbar interbody fusion[J]. Surg Neurol Int, 2010, 1: 12. DOI:10.4103/2152-7806.63905 |
| [2] | Ozgur BM, Aryan HE, Pimenta L, et al. Extreme lateral interbody fusion (XLIF):a novel surgical technique for anterior lumbar interbody fusion[J]. Spine J, 2006, 6(4): 435–443. |
| [3] | Youssef JA, McAfee PC, Patty CA, et al. Minimally invasive surgery:lateral approach interbody fusion:results and review[J]. Spine(Phila Pa 1976), 2010, 35(26 Suppl): S302–S311. |
| [4] | McGirt MJ, Parker SL, Lerner J, et al. Comparative analysis of perioperative surgical site infection after minimally invasive versus open posterior/transforaminal lumbar interbody fusion:analysis of hospital billing and discharge data from 5170 patients[J]. J Neurosurg Spine, 2011, 14(6): 771–778. DOI:10.3171/2011.1.SPINE10571 |
| [5] | Parker SL, Mendenhall SK, Shau DN, et al. Minimally invasive versus open transforaminal lumbar interbody fusion for degenerative spondylolisthesis:comparative effectiveness and cost-utility analysis[J]. World Neurosurg, 2014, 82(1/2): 230–238. |
| [6] | Lucio JC, Vanconia RB, Deluzio KJ, et al. Economics of less invasive spinal surgery:an analysis of hospital cost differences between open and minimally invasive instrumented spinal fusion procedures during the perioperative period[J]. Risk Manag Healthc Policy, 2012, 5: 65–74. |
| [7] | Rodgers WB, Gerber EJ, Rodgers JA. Lumbar fusion in octogenarians:the promise of minimally invasive surgery[J]. Spine(Phila Pa 1976), 2010, 35(26 Suppl): S355–S360. |
| [8] | Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127–1131. |
| [9] | Fairbank JC, Couper J, Davies JB, et al. The Oswestry low back pain disability questionnaire[J]. Physiotherapy, 1980, 66(8): 271–273. |
| [10] | Ware JE Jr, Sherbourne CD. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection[J]. Med Care, 1992, 30(6): 473–483. DOI:10.1097/00005650-199206000-00002 |
| [11] | American Spinal Injury Association. Standards for neurological classification of spinal injury patients[M]. Chicago: American Spinal Injury Association, 1992. |
| [12] | Goldstein CL, Macwan K, Sundararajan K, et al. Comparative outcomes of minimally invasive surgery for posterior lumbar fusion:a systematic review[J]. Clin Orthop Relat Res, 2014, 472(6): 1727–1737. DOI:10.1007/s11999-014-3465-5 |
| [13] | Sun ZJ, Li WJ, Zhao Y, et al. Comparing minimally invasive and open transforaminal lumbar interbody fusion for treatment of degenerative lumbar disease:a metaanalysis[J]. Chin Med J(Engl), 2013, 126(20): 3962–3971. |
| [14] | Parker SL, Adogwa O, Bydon A, et al. Cost-effectiveness of minimally invasive versus open transforaminal lumbar interbody fusion for degenerative spondylolisthesis associated low-back and leg pain over two years[J]. World Neurosurg, 2012, 78(1/2): 178–184. |
| [15] | Lehmen JA, Gerber EJ. MIS lateral spine surgery:a systematic literature review of complications, outcomes, and economics[J]. Eur Spine J, 2015, 24(Suppl 3): 287–313. |
| [16] | Kim CW. Scientific basis of minimally invasive spine surgery:prevention of multifidus muscle injury during posterior lumbar surgery[J]. Spine(Phila Pa 1976), 2010, 35(26 Suppl): S281–S286. |
| [17] | Wang J, Zhou Y, Zhang ZF, et al. Comparison of one-level minimally invasive and open transforaminal lumbar interbody fusion in degenerative and isthmic spondylolisthesis grades 1 and 2[J]. Eur Spine J, 2010, 19(10): 1780–1784. DOI:10.1007/s00586-010-1404-z |
| [18] | 张烽, 段广超, 金国华. 下腰椎极外侧椎体间融合术的应用解剖[J]. 中国脊柱脊髓杂志, 2007, 17(11): 859–861. DOI:10.3969/j.issn.1004-406X.2007.11.016 |
| [19] | 胡万坤, 贺石生, 李明. 极外侧入路腰椎椎间融合术[J]. 中国脊柱脊髓杂志, 2009, 19(8): 634–635. |
| [20] | 郑扬, 李危石, 陈仲强, 等. 微创与开放经椎间孔椎体间融合术治疗腰椎单节段退行性疾病的临床疗效比较[J]. 中国脊柱脊髓杂志, 2014, 24(12): 1064–1071. DOI:10.3969/j.issn.1004-406X.2014.12.03 |
| [21] | 肖波, 毛克亚, 王岩, 等. 微创经椎间孔腰椎椎体间融合术与传统后路腰椎椎体间融合术并发症的比较分析[J]. 脊柱外科杂志, 2013, 11(1): 23–27. DOI:10.3969/j.issn.1672-2957.2013.01.005 |
| [22] | Peng CW, Yue WM, Poh SY, et al. Clinical and radiological outcomes of minimally invasive versus open transforaminal lumbar interbody fusion[J]. Spine (Phila Pa 1976), 2009, 34: 1385–1389. DOI:10.1097/BRS.0b013e3181a4e3be |
| [23] | Rodgers WB, Gerber EJ, Patterson J. Intraoperative and early postoperative complications in extreme lateral interbody fusion:an analysis of 600 cases[J]. Spine (Phila Pa 1976), 2011, 36(1): 26–32. DOI:10.1097/BRS.0b013e3181e1040a |
| [24] | 刘希麟, 席焱海, 马俊, 等. 微创极外侧入路腰椎椎间融合术治疗退行性腰椎椎管狭窄症的初步应用和早期疗效分析[J]. 脊柱外科杂志, 2015, 13(4): 198–202. DOI:10.3969/j.issn.1672-2957.2015.04.002 |
| [25] | Anand N, Rosemann R, Khalsa B, et al. Mid-term to long-term clinical and functional outcomes of minimally invasive correction and fusion for adults with scoliosis[J]. Neurosurg Focus, 2010, 28(3): E6. |
| [26] | Knight RQ, Schwaegler P, Hanscom D, et al. Direct lateral lumbar interbody fusion for degenerative conditions:early complication profile[J]. J Spinal Disord Tech, 2009, 22(1): 34–37. DOI:10.1097/BSD.0b013e3181679b8a |
 2019, Vol.17
2019, Vol.17  Issue(2): 84-89
Issue(2): 84-89


