多节段退行性腰椎椎管狭窄是指≥2个节段的椎管狭窄, 常合并退行性腰椎滑脱、脊柱侧凸及椎间不稳。狭窄的椎管可压迫神经等结构, 引起一系列临床症状和体征, 部分患者需手术治疗[1]。研究表明, 椎管狭窄的影像学表现与患者的临床症状无明确相关性, 尤其是多节段腰椎椎管狭窄症患者, 引起症状的责任节段可能仅是单个节段[2]。因此, 不能单纯以影像学的多节段狭窄作为诊断依据, 特别是不能作为手术治疗的判断标准。本研究回顾性分析2014年9月—2016年10月本院采用经皮显微内窥镜下责任节段减压治疗的40例多节段腰椎椎管狭窄症患者的临床资料, 以探讨责任节段减压的临床疗效, 现报告如下。
1 资料与方法 1.1 一般资料纳入标准:①年龄35 ~ 80岁; ②非手术治疗 > 3个月症状无改善; ③影像学证实多节段腰椎椎管狭窄; ④有明确的神经根痛症状、神经源性跛行或神经损伤; ⑤手术节段无既往手术史。排除标准:①影像学提示腰椎明显不稳; ②腰椎肿瘤及感染; ③精神异常; ④凝血功能异常。根据以上标准纳入患者40例, 其中男26例、女14例, 年龄53 ~ 76 (63.6±10.4)岁; 病程9 ~ 240(98.4±20.4)个月。病变节段:L2~5 12例, L2 ~ S1 12例, L3 ~ S1 16例。40例患者中, 合并高血压27例, 心脏疾病19例, 糖尿病12例, 重度骨质疏松20例。所有患者均有反复发作的间歇性跛行, 伴双侧下肢症状18例, 单侧下肢症状22例。术前针对内科疾患进行相应对症治疗, 麻醉科会诊后明确无明显麻醉禁忌证后择期手术。
1.2 手术方法术前根据临床症状、体征、影像学检查、运动学负荷试验, 必要时行神经根封闭试验以明确责任节段。全身麻醉成功后取俯卧位, 腹部悬空, C形臂X线机透视下确定手术节段。常规消毒铺巾, 棘突旁开0.5 ~ 1.0 cm, 纵行切开皮肤2.0 cm及深筋膜, 逐级扩张管剥离棘突旁肌肉, 置入工作套管, 并再次透视确定导管位置。切除部分上位椎板下缘, 游离并切除部分增生肥厚的黄韧带, 显露硬膜, 切除部分上下关节突及增生内聚的骨赘, 扩大侧隐窝, 解除神经根压迫。然后向对侧倾斜工作通道, 切除对侧肥厚的黄韧带及增生的骨赘, 扩大侧隐窝, 解除对侧神经根的压迫。如果术前影像学检查提示椎间隙明显变窄, 则需将对侧椎板多磨除一部分, 将工作通道尽量向对侧椎间孔倾斜, 以解除椎间孔狭窄。如果椎间盘脱出, 或存在钙化等可给予切除, 如果属于包容性椎间盘突出, 根据神经根紧张程度及受压因素, 部分可不予切除, 保持局部完整性。部分患者骨质增生严重、椎板间隙消失, 术中需辅助使用磨钻磨除骨质。彻底止血后冲洗伤口, 留置半管引流管, 逐层缝合切口。术后第2天拔除引流管后即可在支具保护下下床活动, 术后第3天出院, 同时指导患者腰背部肌锻炼。术后3周去除支具。
1.3 疗效评价记录患者手术时间、术中出血量、住院时间及并发症发生情况, 记录术前、术后腰腿痛视觉模拟量表(VAS)评分[3]及日本骨科学会(JOA)[4]评分。采用VAS评分评估患者腰腿疼痛程度, 采用JOA评分评估临床疗效。
1.4 统计学处理采用SPSS 13.0软件对数据进行统计学分析, 数据以x±s表示, 术前术后数据比较采用t检验; 以P < 0.05为差异有统计学意义。
2 结果所有患者均顺利完成手术, 切口均一期愈合, 随访12 ~ 36(21±3)个月。手术时间50 ~ 150(70±15)min, 术中出血量50 ~ 400(60±5)mL, 住院时间3 ~ 7(4±1)d。末次随访时, 腰痛VAS评分由术前(5.7±1.4)分改善至(1.8±1.7)分, 腿痛VAS评分由术前(7.2±2.3)分改善至(1.7±0.9)分; JOA评分由术前(11.0±2.8)分改善至(23.0±2.2)分; 差异均有统计学意义(P < 0.05)。临床疗效优23例(57.6%), 良12例(30.0%), 可5例(12.5%), 优良率为87.5%。末次随访时影像学检查无腰椎不稳及滑脱, 手术及邻近节段未发生椎管再狭窄。典型病例影像学资料见图 1。
|
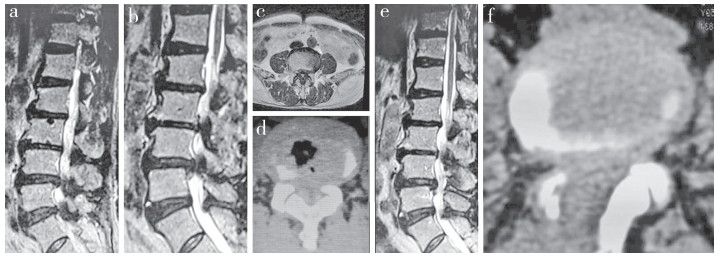
男, 72岁, 腰痛伴双侧下肢疼痛3年, 加重伴间歇性跛行3个月a ~ d:术前MRI及CT示L3 ~ S1椎管狭窄, 椎间盘突出, 神经受压明显e, f:术后3个月MRI及CT示神经减压彻底 Male, 72 years old, back pain and bilateral lower extremity pain for 3 years, with intermittent claudication for 3 months a-d:Preoperative MRIs and CT show L3-S1 spinal stenosis, disc herniation and obvious nerve compression e, f:MRI and CT at postoperative 3 months show that nerve decompression is complete 图 1 典型病例影像学资料 Figure 1 Imaging data of a typical case |
退行性腰椎椎管狭窄症的病理特点是脊柱关节突关节增生内聚, 黄韧带肥厚, 椎间盘突出、钙化, 椎体后缘骨质增生, 椎间隙狭窄等, 以上变化导致椎管变窄、马尾神经受压, 引起腰腿痛等症状[5]。文献表明, 脊柱退行性变的起始因素是椎间盘髓核脱水、椎间隙高度下降, 导致脊柱稳定性丢失, 进而引起周围结构增生肥厚, 治疗的目的是重新稳定脊柱、保持椎体正常序列, 但过度的增生、肥厚可导致椎管狭窄, 压迫神经结构[6-7]。腰椎退行性变可同时发生在多个节段, 导致影像学上表现为多节段椎管狭窄。Sigmundsson等[8]发现50%腰椎椎管狭窄症患者有≥2个节段的椎管狭窄, 横截面积 < 70 mm2。研究表明, 影像学上的椎管狭窄与患者症状无显著相关性, 大多数多节段腰椎椎管狭窄症患者症状可能仅由单个狭窄节段引起[9-10]。Takahasi等[9]指出, 多节段椎管狭窄对神经根血流的影响较单节段更为显著, 患者更容易出现间歇性跛行。Sato等[10]的研究表明, 尽管多节段椎管狭窄更容易导致患者出现马尾神经症状, 但患者症状往往是由单节段狭窄引起, 该节段被称为责任节段。术前精准定位、明确责任节段可避免大范围减压, 达到彻底减压并尽可能减少正常结构破坏, 对于高龄患者尤其重要。
传统手术由于减压范围大, 椎板及关节突切除较多, 术后腰椎稳定性受到严重破坏, 为重建腰椎稳定性, 避免术后发生医源性腰椎不稳, 多节段减压结合长节段融合是治疗多节段腰椎椎管狭窄症较为常用的治疗方法。但术中大范围剥离肌肉, 破坏脊神经内侧支, 患者术后远期可能会遗留腰背部慢性疼痛、僵硬、邻近节段退行性变等问题, 甚至部分患者需再次手术治疗[11-12]。对于多节段腰椎椎管狭窄症的减压范围尚存在争议, Yukawa等[13]比较责任节段减压和全部狭窄节段减压治疗多节段腰椎椎管狭窄症, 结果显示, 2组疗效无明显差异。Ulrich等[14]通过多中心前瞻性研究表明, 责任节段减压治疗多节段腰椎椎管狭窄症术后疗效优于全部狭窄节段减压。本研究结果也显示, 责任节段减压治疗多节段腰椎椎管狭窄症术后疗效满意, 肌肉软组织破坏少, 手术时间短。
精准减压的关键在于判定责任节段, 目前尚无一种简洁而精准的判定方法。临床上常联合多种方法判定责任节段, 包括病史、查体、影像学检查、步行负荷试验、神经根管封闭试验等。神经根管封闭试验是最常用的介入方法, 从神经根管口向内注射局部麻醉药物, 将神经根封闭, 阻断神经信号传导, 与原有症状对比, 如患者临床症状减轻或消失则判定为责任节段, 症状的改善程度可用来评估手术减压后的效果。操作中需要注意:①穿刺过程中C形臂X线机与身体成45°角, 确保穿刺针对准椎弓根“6点钟”位置, 或感觉麻木时略退出为宜; ②局部麻醉药用量 < 1 mL, 药量过大可能会使其他神经根同时封闭, 影响定位诊断效果。如果封闭发现症状来源于多个节段, 则需更改手术方案。
经皮显微内窥镜辅助下手术治疗腰椎椎管狭窄症是近年来逐渐开展的微创手术, 具有疗效好、创伤小、恢复快、不破坏脊柱稳定性等优点[15-16]。手术入路的选择对于能否顺利完成手术至关重要。退行性腰椎椎管狭窄症患者通常伴侧凸畸形, 凹侧的椎管狭窄程度较凸侧严重, 患者症状往往来自凹侧; 同时, 该类患者椎体往往同时伴旋转, 棘突偏向凹侧, 故凹侧的手术入路空间较小, 暴露需要切除大量的关节突关节, 影响脊柱的稳定性[17-18]; 笔者建议对于此类患者选择凸侧作为手术入路侧, 然后向对侧倾斜工作通道, 切除对侧肥厚的黄韧带及增生的骨赘, 潜行扩大侧隐窝, 解除神经根及硬膜囊的压迫。如患者不伴脊柱侧凸畸形, 则首选症状侧入路。
据文献报道, 椎间盘突出合并椎管狭窄的发生率为5% ~ 25%, 术中需根据突出情况决定是否切除椎间盘[19]。如椎间盘巨大突出或脱出可予以切除, 以减轻神经根张力; 如为包容性椎间盘突出, 可根据神经根紧张程度及受压因素予以部分切除, 保持局部完整性有利于维持脊柱前柱高度, 避免术后发生医源性脊柱不稳[20]。
多节段腰椎椎管狭窄症患者往往同时伴有椎体不稳甚至滑脱, 这类患者是否需行融合手术, 要根据患者的临床表现及影像学上的不稳或滑脱程度来判断:影像学上Ⅱ度及以上的中重度滑脱或同时伴有顽固性腰痛, 需行融合手术; Ⅱ度以下的滑脱、不稳, 或患者动力位X线片显示滑脱处于“稳定状态”, 则不需行融合手术, 仅精准减压, 尽可能保留脊柱的稳定系统[21-22]。
综上所述, 经皮显微内窥镜下责任节段减压治疗多节段腰椎椎管狭窄症是一种微创、并发症少、快速康复的治疗方案。该术式可有效解除神经压迫, 不影响脊柱稳定性。但本研究未设立对照组, 且样本量较小、随访时间较短, 尚需更大样本量及长时间随访的对照研究以进一步探讨该术式的远期临床疗效。
| [1] |
El-Abed K, Barakat M, Ainscow D. Multilevel lumbar spinal stenosis decompressio:midterm outcome using a modified hinge osteotomy technique[J]. J Spinal Disord Tech, 2011, 24(6): 376-380. DOI:10.1097/BSD.0b013e3182014aa1 |
| [2] |
Iguchi T, Wakami T, Kurihara A, et al. Lumbar multilevel degenerative spondylolisthesis:radiological evaluation and factors related to anterolisthesis and retrolisthesis[J]. J Spinal Disord Tech, 2002, 15(2): 93-99. DOI:10.1097/00024720-200204000-00001 |
| [3] |
Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127-1131. |
| [4] |
Fukui M, Chiba K, Kawakami M, et al. Japanese Orthopaedic Association back pain evaluation questionnaire. Part 2. Verification of its reliability:the subcommittee on low back pain and cervical myelopathy evaluation of the Clinical Outcome Committee of the Japanese Orthopaedic Association[J]. J Orthop Sci, 2007, 12(6): 526-532. DOI:10.1007/s00776-007-1168-4 |
| [5] |
Benoist M. The natural history of lumbar degenerative spinal stenosis[J]. Joint Bone Spine, 2002, 69(5): 450-457. DOI:10.1016/S1297-319X(02)00429-3 |
| [6] |
Erkintalo MO, Salminen JJ, Alanen AM, et al. Development of degenerative changes in the lumbar in tervertebral disk:results of a prospective MR imaging study in adolescents with and without low-back pain[J]. Radiology, 1995, 196(2): 529-533. DOI:10.1148/radiology.196.2.7617872 |
| [7] |
Modic MT, Ross JS. Lumbar degenerative disk disease[J]. Radiology, 2007, 245(1): 43-61. |
| [8] |
Sigmundsson FG, Kang XP, Jönsson B, et al. Correlation between disability and MRI findings in lumbar spinal stenosis:a prospective study of 109 patients operated on by decompression[J]. Acta Orthop, 2011, 82(2): 204-210. DOI:10.3109/17453674.2011.566150 |
| [9] |
Takahashi K, Olmarker K, Holm S, et al. Double-level cauda equina compression:an experimental study with continuous monitoring of intraneural blood flow in the porcine cauda equina[J]. J Orthop Res, 1993, 11(1): 104-109. DOI:10.1002/jor.1100110112 |
| [10] |
Sato K, Kikuchi S. Clinical analysis of two-level compression of the cauda equina and the nerve roots in lumbar spinal canal stenosis[J]. Spine, 1997, 22(16): 1898-1903. DOI:10.1097/00007632-199708150-00018 |
| [11] |
Sihvonen T, Herno A, Paljärvi L, et al. Local denervation atrophy of paraspinal muscles in postoperative failed back syndrome[J]. Spine(Phila Pa 1976), 1993, 18(5): 575-581. DOI:10.1097/00007632-199304000-00009 |
| [12] |
管俊杰, 石志才. 后路腰椎椎间融合术对邻近节段退变的影响[J]. 脊柱外科杂志, 2011, 9(2): 83-87. DOI:10.3969/j.issn.1672-2957.2011.02.005 |
| [13] |
Yukawa Y, Lenke LG, Tenhula J, et al. A comprehensive study of patients with surgically treated lumbar spinal stenosis with neurogenic claudication[J]. J Bone Joint Surg Am, 2002, 84-A(11): 1954-1959. |
| [14] |
Ulrich NH, Burgstaller JM, Held U, et al. The influence of single-level versus multilevel decompression on the outcome in multisegmental lumbar spinal stenosis:analysis of the lumbar spinal outcome study(LSOS) data[J]. Clin Spine Surg, 2017, 30(10): E1367-E1375. DOI:10.1097/BSD.0000000000000469 |
| [15] |
Smith JS, Ogden AT, Shafizadeh S, et al. Clinical outcomes after microendoscopic discectomy for recurrent lumbar disc herniation[J]. J Spinal Disord Tech, 2010, 23(1): 30-34. DOI:10.1097/BSD.0b013e318193c16c |
| [16] |
叶晓健. 脊柱内窥镜及脊柱微创技术:快速发展又任重道远[J]. 脊柱外科杂志, 2015, 13(6): 321. DOI:10.3969/j.issn.1672-2957.2015.06.001 |
| [17] |
Schöller K, Steingrüber T, Stein M, et al. Microsurgical unilateral laminotomy for decompression of lumbar spinal stenosis:long-term results and predictive factors[J]. Acta Neurochir(Wien), 2016, 158(6): 1103-1113. DOI:10.1007/s00701-016-2804-6 |
| [18] |
Khoo LT. Microendoscopic decompressive laminotomy for the treatment of lumbar stenosis[J]. Neurosurgery, 2002, 51(5 Suppl): S146-S154. |
| [19] |
Siepe CJ, Heider F, Beisse R, et al. Treatment of dynamic spinal canal stenosis with an interspinous spacer[J]. Oper Orthop Traumatol, 2010, 22(5-6): 524-535. DOI:10.1007/s00064-010-9042-5 |
| [20] |
Dall BE, Rowe DE. Degenerative spondylolisthesis. Its surgical management[J]. Spine(Phila Pa 1976), 1985, 10(7): 668-672. DOI:10.1097/00007632-198509000-00013 |
| [21] |
马远征, 李大伟. 腰椎滑脱与腰椎不稳的诊疗[J]. 中国骨伤, 2014, 27(9): 709-711. DOI:10.3969/j.issn.1003-0034.2014.09.001 |
| [22] |
唐天驷, 钱忠来. 腰椎崩裂和滑脱症[J]. 中华骨科杂志, 1997, 17(1): 5-7. DOI:10.3760/j.issn:0253-2352.1997.01.002 |
 2019, Vol.17
2019, Vol.17  Issue(4): 244-247
Issue(4): 244-247


