2. 上海开元骨科医院骨科, 上海 201200
2. Department of Orthopaedics, Shanghai Kaiyuan Orthopaedics Hospital, Shanghai 201200, China
腰椎椎间融合术是治疗腰椎退行性疾病、畸形、肿瘤、感染等多种腰椎疾病的重要手术方式。近年来,腰椎椎间融合术后邻近节段退行性变(ASD)的发生逐渐增多,越来越受到学者重视[1]。ASD表现为手术治疗节段的相邻节段出现椎间盘退行性变等影像学改变,并可能继发神经根压迫、椎管狭窄及脊柱不稳等,从而引发相关临床症状[2]。一般认为,腰椎相应节段融合后,可能增加邻近节段活动度,加重邻近节段负担;手术可能破坏相应部位解剖结构,引发脊柱不稳;加之该部分患者年龄相对偏大,邻近节段椎间盘可能已发生退行性变。上述因素的共同作用导致ASD发生并产生症状[3]。症状性ASD的治疗是目前临床上较为棘手的问题。本研究回顾性分析2017年4月—2018年3月上海健康医学院附属浦东新区人民医院在后路腰椎椎间融合术(PLIF)中采用延长链接固定治疗的25例腰椎椎间融合术后ASD患者临床资料,评估该术式的安全性及有效性,现报告如下。
1 资料与方法 1.1 一般资料纳入标准:①PLIF中采用椎弓根螺钉内固定术后;②随访时腰椎正侧位X线、CT、MRI等影像学检查诊断为ASD,临床症状与病变节段相符;③规范的非手术治疗无效。根据以上标准纳入患者25例,其中男10例、女15例,年龄68 ~ 71(70.1±1.8)岁。入院诊断:腰椎椎管狭窄症8例、椎间不稳9例、腰椎后凸3例、腰椎侧凸5例。初次手术节段:L4 ~ S1 9例、L3 ~ S1 13例、L4,5 3例。初次手术至发生ASD再手术的时间为8.5 ~ 14.7(10.08±1.56)年。ASD节段:L3,4 9例,L2~4 11例,L1~3 3例,L1以上节段2例;单节段ASD 9例,多节段ASD 16例。
1.2 手术方法及术后处理患者全身麻醉后取俯卧位,以原手术节段椎弓根螺钉平面下方为切口起点,做正中切口,向上延长与拟行手术节段相当,依次切开皮肤、皮下组织,分离椎旁肌肉等组织,骨膜下剥离,显露手术野,范围包括手术节段原有椎弓根螺钉及其上下部分连接棒。根据术前腰椎正侧位X线及CT检查判断原椎弓根螺钉钉尾及连接棒位置。进手术节段椎弓根置钉时,先预估钉尾棒槽位置,选择进钉点、内外倾角和头尾侧倾角,以确保顺利安装链接块及连接棒,通过链接块装置将原有内固定连接棒与再次手术使用的连接棒相连接,并通过链接块中的4枚螺帽锁紧相连(图 1)。经调整后仍无法确保连接2根棒时,可贴近相邻椎体椎弓根螺钉原手术侧剪去原有连接棒,再次调整该椎弓根螺钉方向重新置钉。透视确认置钉无误后预弯连接棒,做椎间撑开,采用经椎间孔腰椎椎间融合术减压,椎间Cage融合。留置引流管1根,逐层缝合切口。术后24 h拔除引流管,术后3 ~ 7 d佩戴腰围下床进行功能锻炼,期间避免过度弯腰和重体力活动。

|
注:a,原内固定连接棒 b,螺帽 c,链接块 d,新内固定连接棒 Note:a, Original internal fixation connecting rod b, Nut c, Extended-link block d, New internal fixation connecting rod 图 1 链接块装置示意图 Fig. 1 Diagram of extended-link block |
记录手术时间、术中出血量及并发症情况。临床疗效评估采用疼痛视觉模拟量表(VAS)评分[4]和Oswestry功能障碍指数(ODI)[5]。拍摄手术前后腰椎正侧位X线片及CT,测量腰椎前凸角(L1上终板与L5下终板延长线间的夹角)、椎间隙高度等影像学参数。椎间隙高度(mm)=(椎间隙前缘高度+椎间隙后缘高度)/2。
1.4 统计学处理应用SPSS 13.0软件对数据进行统计学分析,计量资料以x±s表示,手术前后资料比较采用配对t检验;以P < 0.05为差异有统计学意义。
2 结果所有手术顺利完成,术后随访3 ~ 15个月,平均7.9个月;手术时间90 ~ 180 min,平均120 min;术中出血量200 ~ 800 mL,平均500 mL;所有患者未出现手术相关并发症。所有患者术后VAS评分及ODI均较术前明显改善,差异均有统计学意义(P < 0.05,表 1)。影像学测量结果显示,手术节段术前腰椎前凸角、椎间隙高度分别由术前26.96°±5.03°、(6.80±0.87)mm改善至末次随访时37.58°±1.50°、(11.04±0.68)mm,差异均有统计学意义(P < 0.05,表 1)。末次随访时椎间植骨均达到骨性融合。典型病例影像学资料见图 2。
|
|
表 1 疗效评定指标 Tab. 1 Efficacy evaluation index |
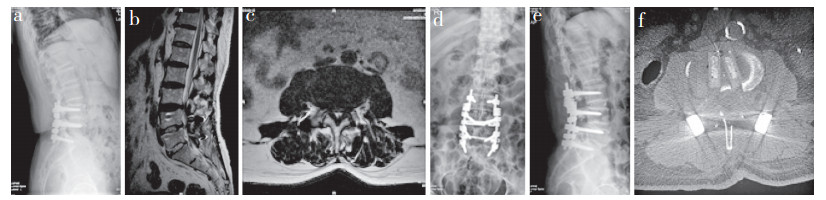
|
男,69岁,L4 ~ S1椎弓根螺钉内固定并椎间自体髂骨块植入术后11年 a ~ c:术前腰椎X线片及MRI示L3,4腰椎不稳,硬膜囊受压 d,e:术后1个月腰椎正侧位X线片示腰椎生理曲度恢复 f:术后3个月腰椎CT示双侧减压彻底,Cage无明显沉降,椎间骨性融合 Male, 69 years old, 11 years after first operation of PLIF with pedicle screw internal fixation and iliac bone autograft at L4 -S1 a-c:Preoperative roentgenograph and MRIs show instability of L3, 4 and compression of dural sac d, e:Anteroposterior and lateral roentgenographs at postoperative 1 month show recovery of lumbar physiological curvature f:CT at postoperative 3 months shows bilateral complete decompression, no subsidence of Cages, and intervertebral bony fusion 图 2 典型病例影像学资料 Fig. 2 Imaging data of a typical case |
ASD是PLIF术后常见并发症,既往报道1.04% ~ 30.3%接受腰椎固定融合的患者因ASD出现临床症状需再次手术治疗[6-9];无临床症状但已有影像学表现的ASD发生率高达100%[10]。对于无症状ASD患者可采取非手术治疗,而伴有临床症状者往往需要接受再次手术[11]。相关研究表明,多种因素与腰椎术后ASD发生相关,主要包括患者自身因素,如骨质疏松程度、术前ASD情况以及手术因素等[11-12]。Harrop等[13]进行系统综述比较了腰椎关节固定术和关节成形术后ASD发生率,发现固定术后ASD发生率达34%,高于接受关节成形术的患者。上述结果显示,腰椎椎间融合术后可能增加邻近节段的关节负荷和活动度,加速邻近节段发生退行性变。Min等[14]发现前路腰椎椎间融合术(ALIF)后ASD发生率为44%,PLIF术后为82.6%。相较于ALIF,PLIF对周围解剖结构损伤较大,邻近结构的破坏可能是ASD的危险因素[15]。ASD表现形式多样,本研究病例表现为椎管狭窄、椎间不稳、后凸及侧凸畸形等,增加了ASD诊断和治疗的困难。
关于腰椎ASD再次手术治疗方式目前尚无统一标准,由于涉及到初次手术节段,处理较为复杂,多种术式均有报道,主要包括邻近节段的非固定融合术和固定融合术[16-17]。非固定融合术式,如单纯椎管减压术或单纯椎间盘切除术,主要适用于单纯椎间盘突出或单侧神经根管狭窄的患者[10]。Phillips等[18]报道了采用单纯减压术治疗26例腰椎椎间融合术后邻近节段椎管狭窄患者,57.7%的患者手术效果满意。Zhu等[19]报道采用髓核消融成形术治疗ASD取得良好疗效。但是,对于伴有严重椎管狭窄、椎间不稳、后凸畸形及侧凸畸形的患者,该术式治疗效果有限。采用固定融合手术可选择拆除原内固定,新单节段椎弓根螺钉内固定结合椎间植骨融合,该术式适用于单节段ASD患者,且要求原手术节段已融合;或拆除原有内固定后延长(包括原有节段或部分原有节段)固定融合,但手术创伤较大,治疗费用昂贵。Chen等[20]采用后路椎板切除自体骨融合并椎弓根螺钉固定节段延长治疗39例腰椎椎间融合术后ASD患者,治疗有效率为76.9%,骨性融合率为94.9%。此外,皮质骨螺钉技术[21]、微创经椎间孔入路腰椎椎间融合术、侧方入路腰椎椎间融合术等[22]均可应用于腰椎退行性疾病的治疗,手术操作简便、创伤较小。但是,对于腰椎术后ASD,已有椎弓根螺钉可能影响再次置入皮质骨螺钉或椎弓根螺钉,手术操作范围多局限于1 ~ 2个节段,尤其是多节段或伴有后凸、侧凸畸形的患者,处理较为困难,不能进行彻底的减压。
本研究采用延长链接固定技术治疗腰椎椎间融合术后ASD,相较于上述手术方式具有以下优势。①手术创伤小,操作简便,不干扰或很少干扰原有内固定。②适用于多节段ASD,如合并严重椎管狭窄、滑脱、后凸畸形及侧凸畸形的患者,可进行彻底单侧减压、单侧椎间植骨融合,或进行双侧减压、双侧椎间植骨融合,还可对椎体进行复位,对后凸及侧凸畸形进行矫正。③手术时间较短,出血量可控制,患者术后恢复快,可早期进行活动及康复训练。④所用链接块采用每根棒2枚锁定螺母固定,链接固定牢固、可靠。⑤切口设计略超过相邻椎体椎弓根螺钉平面即可,创伤较小。术前应拍摄标准腰椎正侧位X线片、CT及MRI,对比原椎弓根螺钉位置、钉尾位置、原有连接棒位置。2根棒之间需预留间距,间距略小于链接块上2棒孔间的距离,绝对不可大于后者;略小于后者时链接块允许少许倾斜而不影响安装,反之,则无法安装链接块。置钉时首先要预估钉尾棒槽的位置,选择进钉点,调整进钉内外倾角和头尾侧倾角。仍然无法确保连接2根棒时,可以贴近相邻椎体椎弓根螺钉原手术侧剪去原有连接棒,再次调整该椎弓根螺钉的方向。原棒在需要连接一端过短、无法进行链接块安装时,也可用以上方法进行剪棒连接。对于长节段ASD合并骨质疏松的患者,同时需要进行后/侧凸畸形矫正时,需要对钉道进行骨水泥强化。
综上,PLIF中采用延长链接固定治疗腰椎椎间融合术后ASD具有操作简便、时间短、出血量少、术后并发症少、恢复快等特点。该技术对多节段ASD患者亦可取得良好疗效,为腰椎椎间融合术后ASD提供了一种安全、有效的治疗方式,近期随访临床效果良好。但本研究存在样本量小、随访时间短、缺乏对照研究等不足,后期尚需大样本量病例的中、长期对照研究进一步证实。
| [1] |
Di Martino A, Quattrocchi CC, Scarciolla L, et al. Estimating the risk for symptomatic adjacent segment degeneration after lumbar fusion:analysis from a cohort of patients undergoing revision surgery[J]. Eer Spine J, 2014(Suppl 6): 693-698. |
| [2] |
Helgeson MD, Bevevino AJ, Hilibrand AS. Update on the evidence for adjacent segment degeneration and disease[J]. Spine J, 2013, 13(3): 342-351. DOI:10.1016/j.spinee.2012.12.009 |
| [3] |
Heo Y, Park JH, Seong HY, et al. Symptomatic adjacent segment degeneration at the L3-4 level after fusion surgery at the L4-5 level:evaluation of the risk factors and 10-year incidence[J]. Eur Spine J, 2015, 24(11): 2474-2480. DOI:10.1007/s00586-015-4188-3 |
| [4] |
Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127-1131. |
| [5] |
Fairbank JC, Couper J, Davies JB, et al. The Oswestry low back pain disability questionnaire[J]. Physiotherapy, 1980, 66(8): 271-273. |
| [6] |
Cheh G, Bridwell KH, Lenke LG, et al. Adjacent segment disease following lumbar/thoracolumbar fusion with pedicle screw instrumentation:a minimum 5-year follow-up[J]. Spine (Phila Pa 1976), 2007, 32(20): 2253-2257. DOI:10.1097/BRS.0b013e31814b2d8e |
| [7] |
Ghasemi AA. Adjacent segment degeneration after posterior lumbar fusion:an analysis of possible risk factors[J]. Clin Neurol Neurosurg, 2016, 143: 15-18. DOI:10.1016/j.clineuro.2016.02.004 |
| [8] |
Ishihara H, Osada R, Kanamori M, et al. Minimum 10-year follow-up study of anterior lumbar interbody fusion for isthmic spondylolisthesis[J]. J Spinal Disord, 2001, 14(2): 91-99. DOI:10.1097/00002517-200104000-00001 |
| [9] |
李超, 阮狄克, 何勍, 等. 腰椎后外侧融合术对已存在退变的相邻节段的中远期影响[J]. 脊柱外科杂志, 2017, 15(3): 150-155. DOI:10.3969/j.issn.1672-2957.2017.03.005 |
| [10] |
Cho KS, Kang SG, Yoo DS, et al. Risk factors and surgical treatment for symptomatic adjacent segment degeneration after lumbar spine fusion[J]. J Korean Neurosurg Soc, 2009, 46(5): 425-430. DOI:10.3340/jkns.2009.46.5.425 |
| [11] |
孙浩林, 李淳德, 刘宪义, 等. 腰椎融合术后症状性邻近节段退变的临床特点和再手术治疗[J]. 北京大学学报(医学版), 2012, 44(6): 855-859. DOI:10.3969/j.issn.1671-167X.2012.06.010 |
| [12] |
Okuda S, Iwasaki M, Miyauchi A, et al. Risk factors for adjacent segment degeneration after PLIF[J]. Spine (Phila Pa 1976), 2004, 29(14): 1535-1540. DOI:10.1097/01.BRS.0000131417.93637.9D |
| [13] |
Harrop JS, Youssef JA, Maltenfort M, et al. Lumbar adjacent segment degeneration and disease after arthrodesis and total disc arthroplasty[J]. Spine (Phila Pa 1976), 2008, 33(15): 1701-1707. DOI:10.1097/BRS.0b013e31817bb956 |
| [14] |
Min JH, Jang JS, Lee SH. Comparison of anterior-and posterior-approach instrumented lumbar interbody fusion for spondylolisthesis[J]. J Neurosurg Spine, 2007, 7(1): 21-26. DOI:10.3171/SPI-07/07/021 |
| [15] |
Miyagi M, Ikeda O, Ohtori S, et al. Additional decompression at adjacent segments leads to adjcent segment degeneration after PLIF[J]. Eur Spine J, 2013, 22(8): 1877-1883. DOI:10.1007/s00586-013-2694-8 |
| [16] |
Kim SI, Ha KY, Suh DW, et al. Risk factors for adjacent segment degeneration after iliac screw fixation in lumbar degenerative kyphoscoliosis[J]. J Orthop Surg(Hong Kong), 2017, 25(1): 2309499016684727. |
| [17] |
Kim TH, Lee BH, Moon SH, et al. Comparison of adjacent segment degeneration after successful posterolateral fusion with unilateral or bilateral pedicle screw instrumentation:a minimum 10-year follow-up[J]. Spine J, 2013, 13(10): 1208-1216. DOI:10.1016/j.spinee.2013.07.431 |
| [18] |
Phillips FM, Carlson GD, Bohlman HH, et al. Results of surgery for spinal stenosis adjacent to previous lumbar fusion[J]. J Spinal Disord, 2000, 13(5): 432-437. DOI:10.1097/00002517-200010000-00011 |
| [19] |
Zhu H, Zhou XZ, Cheng MH, et al. Coblation nucleoplasty for adjacent segment degeneration after posterolateral fusion surgery:a case report[J]. J Back Musculoskelet Rehabil, 2012, 25(4): 235-238. DOI:10.3233/BMR-2012-0341 |
| [20] |
Chen WJ, Lai PL, Niu CC, et al. Surgical treatment of adjacent instability after lumbar spine fusion[J]. Spine (Phila Pa 1976), 2001, 26(22): E519-E524. DOI:10.1097/00007632-200111150-00024 |
| [21] |
Keorochana G, Pairuchvej S, Trathitephun W, et al. Comparative outcomes of cortical screw trajectory fixation and pedicle screw fixation in lumbar spinal fusion:systematic review and meta-analysis[J]. World Neurosurg, 2017, 102: 340-349. DOI:10.1016/j.wneu.2017.03.010 |
| [22] |
Khechen B, Haws BE, Patel DV, et al. Comparison of postoperative outcomes between primary Mis TLIF and Mis TLIF as a revision procedure to primary decompression[J]. Spine(Phila Pa 1976), 2018, 10. |
 2019, Vol.17
2019, Vol.17  Issue(5): 314-318
Issue(5): 314-318

