经椎间孔腰椎椎间融合术(TLIF)广泛应用于腰椎退行性疾病的治疗,且术后可获得满意的影像学和临床疗效[1-3]。融合器沉降是TLIF术后常见并发症之一,既往文献报道其发生率为13% ~ 50%[4-6]。融合器沉降常伴随椎间隙高度的丢失,甚至再次诱发腰腿痛,显著影响手术效果和患者生活质量[7-8]。融合器沉降的常见危险因素包括年龄、骨密度、融合器大小和型号等[8-10]。终板位于融合器与椎体交界区,其形态学特征及相关生物力学因素对术后融合器沉降的影响逐渐被重视。本研究通过回顾性分析接受TLIF治疗的单节段腰椎退行性疾病患者的临床和影像学资料,评估不同椎体终板形态对术后融合器沉降发生率的影响,报告如下。
1 资料与方法 1.1 一般资料纳入标准:①单节段腰椎退行性疾病并接受TLIF治疗;②术后随访≥ 2年;③影像学资料完整,包括术前、术后1周和末次随访时腰椎正侧位X线片及术前腰椎MRI。排除标准:①腰椎手术史;②既往脊柱骨折、肿瘤及其他脊柱疾患;③合并退行性腰椎侧凸(Cobb角 > 10°);④腰椎滑脱Meyerding分型[11] > Ⅱ度;⑤术后即刻CT检查示骨性终板损伤及融合器沉降。根据上述标准,纳入2015年1月—2016年8月在本院接受TLIF治疗的单节段腰椎退行性疾病患者75例,其中男35例、女40例,年龄46 ~ 76(59.7±16.1)岁;其中腰椎椎间盘突出症(LDH)52例,崩裂性腰椎滑脱症(ILS)8例,退行性腰椎滑脱症(DLS)15例;手术节段为L4/L5 48例,L5/S1 27例。
1.2 影像学测量及分组采用Surgimap Spine软件测量术前、术后1周及末次随访时腰椎侧位X线片相关参数。①椎间隙高度:手术节段上位椎体下终板与下位椎体上终板前缘、中间、后缘间的距离。椎间隙高度(mm)=(前缘高度+中间高度+后缘高度)/3。②椎间孔高度:上位椎体椎弓根下缘与下位椎体椎弓根上缘间的距离。③腰椎前凸角:L1和S1上终板间的夹角。④腰椎局部前凸角:手术节段上位椎体下终板与下位椎体上终板间的夹角。术后矫正率(%)=(术后参数测量值-术前参数测量值)/术前参数测量值;末次随访矫正率(%)=(末次随访参数测量值-术前参数测量值)/术前参数测量值;矫正丢失率(%)=术后矫正率-末次随访矫正率。
根据Pappou等[12]的方法,在腰椎矢状位MRI T1加权像沿终板前后缘划1条直线,终板曲线光滑或与直线重合者纳入终板规则组(A组);终板曲线不光滑,有突起或赘生物超出直线者纳入终板不规则组(B组)。当同一节段椎间盘上下终板形态不同时,按就重原则(如上终板规则,下终板不规则,则定义该节段终板形态为不规则)。根据上述标准,54例患者纳入A组,21例患者纳入B组。2组患者一般资料差异无统计学意义(P > 0.05,表 1),具有可比性。
|
|
表 1 一般资料 Tab. 1 General data |
参照Kim等[13]的研究,根据末次随访时融合节段上/下终板塌陷距离将融合器沉降分为轻度沉降(≥2 mm且 < 4 mm)和重度沉降(≥4 mm)。采用Oswestry功能障碍指数(ODI)[14]评估患者腰椎功能,采用腰痛和下肢痛视觉模拟量表(VAS)评分[15]评估患者生活质量。
1.4 统计学处理采用SPSS 17.0软件对数据进行统计学分析。计量资料采用x±s表示,2组患者影像学及临床评价指标采用独立样本t检验,组间比较采用配对t检验,运用χ2检验及Fisher精确检验比较2组患者末次随访时融合器沉降发生率;以P < 0.05为差异有统计学意义。
2 结果所有手术顺利完成。所有患者随访2.0 ~ 3.9(2.7±0.7)年。末次随访时,B组椎间隙高度及腰椎局部前凸角矫正丢失率均高于A组,差异有统计学意义(P < 0.05,表 2);2组椎间孔高度和腰椎前凸角矫正率无明显丢失(表 2)。2组患者末次随访时ODI及腰痛、下肢痛VAS评分较术前显著改善,且末次随访时B组腰痛VAS评分显著高于A组,差异均有统计学意义(P < 0.05,表 2)。末次随访时,16例(21.3%)患者发生融合器沉降,A组7例(13.0%),B组9例(42.9%);其中重度沉降3例,A组1例,B组2例。典型病例影像学资料见图 1,2。
|
|
表 2 统计数据 Tab. 2 Statistical data |
|
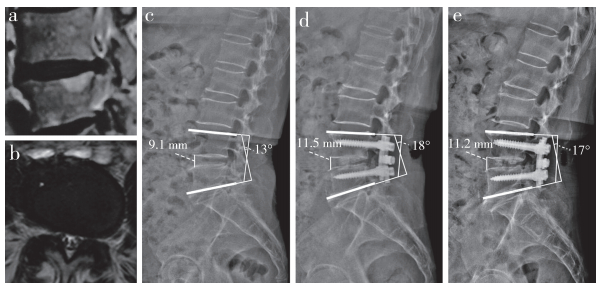
男,63岁,L4终板规则 a ~ c:术前MRI示L4/L5椎管狭窄,椎间隙高度9.1 mm,腰椎局部前凸角13° d:术后椎间隙高度升至11.5 mm,腰椎局部前凸角增至18° e:末次随访时椎间隙高度(11.2 mm)及腰椎局部前凸角(17°)无明显丢失 Male, 63 years old, with a regular L4 endplate a-c:Preoperative MRIs show L4/L5 spinal canal stenosis, intervertebral height is 9.1 mm and local lumbar lordosis angle 13° d:Postoperative intervertebral height increases to 11.5 mm and local lumbar lordosis angle to 18° e:Intervertebral height(11.2 mm) and local lumbar lordosis angle(17°) without significant loss at final follow-up 图 1 A组典型病例影像学资料 Fig. 1 Imaging data of a typical case in group A |

|
女,58岁,L4终板不规则a ~ c:术前MRI示L4/L5椎管狭窄,椎间隙高度5.8 mm,腰椎局部前凸角10° d:术后椎间隙高度升至10.3 mm,腰椎局部前凸角增至16° e:末次随访时融合器沉降,椎间隙高度降至7.9 mm,腰椎局部前凸角降至11° Famale, 58 years old, with a irregular L4 endplate a-c:Preoperative MRIs show L4/L5 spinal canal stenosis, intervertebral height is 5.8 mm and local lumbar lordosis angle 10° d:Postoperative intervertebral height increased to 10.3 mm and local lumbar lordosis angle to 16° e:Cage subsidence at final follow-up, and intervertebral height decreases to 7.9 mm and local lumbar lordosis angle to 11° 图 2 B组典型病例影像学资料 Fig. 2 Imaging data of a typical case in group B |
椎体终板作为椎间盘与椎体的交界区域,具有协助椎间盘缓冲躯干纵向应力的作用[16-17]。伴随椎间盘的退行性变,椎体终板常因承受更大的轴向负荷而出现不同程度的退行性变[12, 18]。Farshad-Amacker等[19]通过回顾性分析90例退行性腰椎疾病患者的影像学资料,发现随着椎间盘退行性变的逐渐加重,椎体终板形态从规则向不规则变化。然而,术前不同终板形态对TLIF术后融合器沉降的发生率及腰椎矢状面形态的影响尚未见报道。本研究末次随访时共16例(21.3%)发生融合器沉降,终板不规则者9例(42.9%),其发生率显著高于规则组(13.0%),提示椎体终板不规则是TLIF术后融合器沉降的危险因素。Lim等[20]的生物力学研究结果显示,椎体终板出现多个局部缺损时,其终板强度和载荷均降低,本研究与上述研究结果一致。
终板不规则患者术后易发生融合器沉降的原因可能与终板的生物力学性能改变有关。Pappou等[12]报道终板形态不规则患者术前即存在较严重的椎间盘退行性变和终板局部缺损。椎体终板因退行性变重塑,发生骨质增生,局部刚性增加而缓冲能力下降,置入融合器后,僵硬的终板会导致接触应力的集中点由终板椎体骨转移至终板表面。本研究采用的融合器形态均为肾形,上下均有1个椭圆形弧度,其目的是为了使融合器与终板有更好的贴合度。但是,对于终板形态不规则的患者而言,融合器与终板的接触面积反而减少,融合器置入后应力集中在交界面,故术后易发生融合器沉降。
末次随访时,终板不规则患者椎间隙高度及腰椎局部前凸角矫正率丢失明显,且显著高于终板规则患者,2组患者椎间孔高度无明显丢失,该结果与Massie等[21]和Lang等[22]的研究结果一致,分析其原因,可能与终板不规则患者术后即刻融合器的沉降有关,TLIF术中腰椎曲度的重建主要依靠椎间隙前高后低和前凸角的恢复,而融合器沉降者的椎间隙高度和局部前凸角丢失明显,从而导致腰椎前凸矫正丢失。TLIF术中应用的后路椎弓根螺钉内固定系统可提供强大支撑,避免因前柱椎间隙高度丢失引起中后柱椎间孔高度的下降[23-25]。上述研究结果表明,终板不规则患者TLIF术后更易发生融合器沉降,且常合并椎间隙高度的丢失,但对椎间孔高度无显著影响。
本研究2组患者末次随访时ODI及下肢痛VAS评分无显著差异,但终板不规则患者腰痛VAS评分显著高于终板规则患者。可能原因在于,椎弓根内固定系统强大的后路支撑作用可有效维持椎间孔高度,避免诱发下肢疼痛症状。但终板不规则患者腰椎局部前凸角丢失率(21.2%)显著高于终板规则患者(3.8%),Choi等[26]的研究结果显示,当术后腰椎前凸角丢失或重建不足、与骨盆入射角不匹配时,患者易产生下腰痛症状。因此,对椎体终板不规则且腰椎前凸角丢失明显的患者可采取前路椎间融合术、斜外侧椎间融合术或极外侧椎间融合术等以有效重建腰椎前凸。
针对终板形态不规则患者术后易发生融合器沉降的现象,在诊疗中应注意:①术前仔细识别椎体终板形态,终板形态不规则患者应常规完善骨密度检查,必要时行抗骨质疏松治疗;②选择合适型号的融合器,术中注意保护椎体终板,在融合器周围充分植骨,避免置入过大的融合器造成终板后份的损伤;③合理放置融合器,Hou等[27]通过尸体研究发现,相较于椎体终板中央部分骨质,终板外周骨质的皮质骨含量高、抗压性强,融合器置于终板前外侧或横跨终板中央区可有效降低术后融合器沉降的发生率。
本研究的局限性。①TLIF术后未能常规行腰椎CT检查,无法排除术中医源性终板损伤的可能。②CT检查是评估椎间隙及椎间孔高度的金标准,故本研究在X线片上测量患者椎间隙及椎间孔高度可能存在误差。③本研究仅回顾性分析患者术前、术后1周及末次随访时的资料,未详细统计术后发生融合器沉降的具体时间。
综上,终板不规则患者术前常存在严重的椎间盘退行性变,尽管术后可获得较好的椎间隙高度重建,但在随访过程中融合器沉降发生率显著高于终板规则患者。对于终板形态不规则患者,术前应完善骨密度检查,必要时给予抗骨质疏松治疗;术中注意仔细操作,保护终板,避免术后融合器沉降的发生。
| [1] |
Challier V, Boissiere L, Obeid I, et al. One-level lumbar degenerative spondylolisthesis and posterior approach:is transforaminal lateral interbody fusion mandatory?:a randomized controlled trial with 2-year follow-up[J]. Spine(Phila Pa 1976), 2017, 42(8): 531-539. DOI:10.1097/BRS.0000000000001857 |
| [2] |
Levin JM, Tanenbaum JE, Steinmetz MP, et al. Posterolateral fusion(PLF) versus transforaminal lumbar interbody fusion(TLIF) for spondylolisthesis:a systematic review and meta-analysis[J]. Spine J, 2018, 18(6): 1088-1098. DOI:10.1016/j.spinee.2018.01.028 |
| [3] |
卓祥龙, 胡建中, 李兵, 等. 经椎间孔腰椎间融合术治疗复发性腰椎间盘突出症的临床研究[J]. 中国矫形外科杂志, 2009, 17(21): 1667-1669. |
| [4] |
Kuang L, Wang B, Lü G. Transforaminal lumbar interbody fusion versus mini-open anterior lumbar interbody fusion with oblique self-anchored stand-alone cages for the treatment of lumbar disc herniation:a retrospective study with 2-year follow-up[J]. Spine(Phila Pa 1976), 2017, 42(21): E1259-E1265. DOI:10.1097/BRS.0000000000002145 |
| [5] |
Malham GM, Parker RM, Blecher CM, et al. Assessment and classification of subsidence after lateral interbody fusion using serial computed tomography[J]. J Neurosurg Spine, 2015, 23(5): 589-597. DOI:10.3171/2015.1.SPINE14566 |
| [6] |
Sonmez E, Coven I, Sahinturk F, et al. Unilateral percutaneous pedicle screw instrumentation with minimally invasive TLIF for the treatment of recurrent lumbar disk disease:2 years follow-up[J]. Turk Neurosurg, 2013, 23(3): 372-378. |
| [7] |
Lin GX, Quillo-Olvera J, Jo HJ, et al. Minimally invasive transforaminal lumbar interbody fusion:a comparison study based on end plate subsidence and cystic change in individuals older and younger than 65 years[J]. World Neurosurg, 2017, 106: 174-184. DOI:10.1016/j.wneu.2017.06.136 |
| [8] |
Oh KW, Lee JH, Lee JH, et al. The correlation between cage subsidence, bone mineral density, and clinical results in posterior lumbar interbody fusion[J]. Clin Spine Surg, 2017, 30(6): E683-E689. DOI:10.1097/BSD.0000000000000315 |
| [9] |
Gonzalez-Blohm SA, Doulgeris JJ, Aghayev K, et al. In vitro evaluation of a lateral expandable cage and its comparison with a static device for lumbar interbody fusion:a biomechanical investigation[J]. J Neurosurg Spine, 2014, 20(4): 387-395. DOI:10.3171/2013.12.SPINE13798 |
| [10] |
鲁世保, 孙文志, 海涌, 等. 腰椎后路椎间植骨融合器后移的危险因素[J]. 脊柱外科杂志, 2016, 14(1): 16-20. |
| [11] |
Meyerding HW. Low backache and sciatic pain associated with spondylolisthesis and protruded intervertebral disc:incidence, significance and treatment[J]. J Bone Joint Surg Am, 1941, 23(2): 461-470. |
| [12] |
Pappou IP, Cammisa FP Jr, Girarod P. Correlation of end plate shape on MRI and disc degeneration in surgically treated patients with degenerative disc disease and herniated nucleus pulposus[J]. Spine J, 2007, 7(1): 32-38. |
| [13] |
Kim MC, Chung HT, Cho JL, et al. Subsidence of polyetheretherketone cage after minimally invasive transforaminal lumbar interbody fusion[J]. J Spinal Disord Tech, 2013, 26(2): 87-92. DOI:10.1097/BSD.0b013e318237b9b1 |
| [14] |
Fairbank JC, Couper J, Davies JB, et al. The Oswestry low back pain disability questionnaire[J]. Physiotherapy, 1980, 66(8): 271-273. |
| [15] |
Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127-1131. |
| [16] |
Duran S, Cavsoglu M, Hatipoglu HG, et al. Association between measures of vertebral endplate morphology and lumbar intervertebral disc degeneration[J]. Can Assoc Radiol J, 2017, 68(2): 210-216. DOI:10.1016/j.carj.2016.11.002 |
| [17] |
Louie PK, Espinoza Orias AA, Fogg LF, et al. Changes in lumbar endplate area and concavity associated with disc degeneration[J]. Spine(Phila Pa 1976), 2018, 43(19): E1127-E1134. DOI:10.1097/BRS.0000000000002657 |
| [18] |
徐永立, 赵小华, 郝金华, 等. 腰椎终板形态变化与椎间盘退变相关性的影像学研究[J]. 中国医药导报, 2016, 13(34): 130-133. |
| [19] |
Farshad-Amacker NA, Hughes AP, Aichmair A, et al. Determinants of evolution of endplate and disc degeneration in the lumbar spine:a multifactorial perspective[J]. Eur Spine J, 2014, 23(9): 1863-1868. DOI:10.1007/s00586-014-3382-z |
| [20] |
Lim TH, Kwon H, Jeon CH, et al. Effect of endplate conditions and bone mineral density on the compressive strength of the graft-endplate interface in anterior cervical spine fusion[J]. Spine(Phila Pa 1976), 2001, 26(8): 951-956. DOI:10.1097/00007632-200104150-00021 |
| [21] |
Massie LW, Zakaria HM, Schultz LR, et al. Assessment of radiographic and clinical outcomes of an articulating expandable interbody cage in minimally invasive transforaminal lumbar interbody fusion for spondylolisthesis[J]. Neurosurg Focus, 2018, 44(1): E8. DOI:10.3171/2017.10.FOCUS17562 |
| [22] |
Lang G, Nacarro-Ramirez R, Gandevia L, et al. Elimination of subsidence with 26-mm-wide cages in extreme lateral interbody fusion[J]. World Neurosurg, 2017, 104: 644-652. DOI:10.1016/j.wneu.2017.05.035 |
| [23] |
Jiya TU, Smit T, Van Royen BJ, et al. Posterior lumbar interbody fusion using non resorbable poly-ether-ether-ketone versus resorbable poly-L-lactide-co-D, L-lactide fusion devices. Clinical outcome at a minimum of 2-year follow-up[J]. Eur Spine J, 2011, 20(4): 618-622. DOI:10.1007/s00586-010-1568-6 |
| [24] |
Chen Y, Chen D, Guo Y, et al. Subsidence of titanium mesh cage:a study based on 300 cases[J]. J Spinal Disord Tech, 2008, 21(7): 489-492. DOI:10.1097/BSD.0b013e318158de22 |
| [25] |
邓乾兴.经椎间孔单节段腰椎椎间融合术后融合器下沉的危险因素分析[D].重庆: 重庆医科大学, 2016. http://d.old.wanfangdata.com.cn/Periodical_zhgkzz98201803005.aspx
|
| [26] |
Choi JY, Sung KH. Subsidence after anterior lumbar interbody fusion using paired stand-alone rectangular cages[J]. Eur Spine J, 2006, 15(1): 16-22. DOI:10.1007/s00586-004-0817-y |
| [27] |
Hou Y, Luo Z. A study on the structural properties of the lumbar endplate:histological structure, the effect of bone density, and spinal level[J]. Spine(Phila Pa 1976), 2009, 34(12): E427-E433. DOI:10.1097/BRS.0b013e3181a2ea0a |
 2019, Vol.17
2019, Vol.17  Issue(6): 409-414
Issue(6): 409-414


