颈椎椎间盘突出症是中老年人常见疾病[1],对非手术治疗无效或有明显神经系统症状的患者,可采用颈椎前路椎间盘切除融合术(ACDF)治疗[2]。生物力学实验和临床研究表明,钉板系统(PCC)内固定可重建颈椎稳定性,防止融合器下沉,提高融合率[3-4]。尽管PCC的制造工艺不断进步,但吞咽困难仍然是PCC术后的常见并发症[5]。Lee等[6]报道,采用PCC术中需要显露病变节段的上、下椎体,增加对相邻椎间盘的刺激并加速其发生退行性变。为了克服上述弊端,零切迹椎间融合器(Zero-P)被应用于颈椎椎间盘突出症的治疗,且被证实其可减少术后吞咽困难和邻近节段疾病的发生[7-8]。然而,Nemoto等[9]发现,尽管Zero-P可获得满意的临床效果,但一些病例在随访中出现了椎间融合器沉降及颈椎曲度的丢失。
理论上,钢板的存在能为椎间隙提供更好的支撑,从而更好地维持颈椎曲度和椎间高度,但目前关于PCC与Zero-P在单节段颈椎椎间盘突出症术后颈椎曲度的维持方面的比较研究较少。本研究回顾性分析了2016年5月—2018年3月在ACDF术中采用Zero-P或PCC治疗的136例单节段颈椎椎间盘突出症患者临床资料,并对其临床和影像学结果进行比较,现报告如下。
1 资料与方法 1.1 一般资料2016年5月—2018年3月,在本院经影像学检查确诊为单节段颈椎椎间盘突出症,且病变节段与临床症状一致,非手术治疗时间超过6周,四肢放射痛、麻木或无力症状仍然存在的248例患者接受ACDF治疗。将年龄为25 ~ 75岁、随访时间超过24个月且资料完整者纳入本研究。排除合并颈椎骨折、后纵韧带骨化、肿瘤或神经系统疾病(肌萎缩性侧索硬化症)者,既往有颈椎手术史者,存在全身或局部感染、重度骨质疏松等影响手术因素者。共纳入患者136例,其中71例术中采用Zero-P(Zero-P组),65例采用PCC(PCC组)。2组患者术前一般资料差异无统计学意义(P > 0.05,表 1),具有可比性。本研究经医院机构审查委员会批准备案,所有患者签署知情同意书。
|
|
表 1 2组患者一般资料 Tab. 1 General data of 2 groups |
所有手术由同一位主任医师带领的手术组完成。患者全身麻醉成功后,取仰卧位,肩背部垫小枕,颈部自然后伸,颈部术区常规消毒铺巾。在颈前右侧做横切口,根据标准的Smith-Robinson路径[10]显露椎体及其两侧椎间盘前部。透视下明确定位无误后,采用Caspar撑开器撑开椎体,以尖刀切除病变节段椎间盘前部纤维环,以髓核钳取出发生退行性变的髓核组织,刮除终板软骨,以枪状咬骨钳咬除突入椎管的椎间盘组织、增生肥厚的后纵韧带及椎体后缘骨赘,以大量生理盐水冲洗术区,观察受压脊髓逐渐恢复正常形态。以三关节咬骨钳咬除椎体前缘骨赘。Zero-P组选择大小合适填压有碎骨的Zero-P(强生,美国)置入椎间隙,取出椎体撑开钉,骨腊封闭钉孔,拧入螺钉并锁定;PCC组选择大小合适的填压碎骨的椎间融合器(强生,美国)置入椎间隙,取出椎体撑开钉,骨蜡封闭钉孔,取合适长度的钛板(强生,美国)预弯后固定于椎体前壁上,拧入螺钉并锁定。透视下见钢板、螺钉、融合器位置良好后再次用大量生理盐水冲洗术区,检查确认无明显出血点,切口旁另切1个小口引入1根负压引流管。逐层缝合联合腱膜、颈阔肌、皮下组织,以可吸收线缝合皮肤。确认负压引流通畅后无菌包扎创口。
术后雾化吸入地塞米松磷酸钠注射液10 mg与10 mL氯化钠注射液混合液3 d,缓解气管和食管不适。引流管于术后24 ~ 48 h取出。术后1 d患者可在颈托保护下下床,术后颈托佩戴1周。
1.3 观察指标记录手术时间和术中出血量。术前及术后1、6、12和24个月,采用日本骨科学会(JOA)评分[11]评估患者神经功能;采用疼痛视觉模拟量表(VAS)评分[12]评估患者颈部和手臂疼痛情况;采用正侧位、过伸过屈位X线片测量C2~7颈椎曲度(C2下终板与C7下终板间的夹角)、手术节段Cobb角(手术节段上位椎体上终板与下位椎体下终板间的夹角)及邻近椎体高度(手术节段上位椎体上终板与下位椎体下终板间的垂直距离);根据Lin等[13]的方法评估椎间融合情况:在过伸过屈位X线片上测量融合节段及邻近节段棘突间隙差值(ISM),当邻近节段ISM > 4 mm(提示屈伸足够)且融合节段ISM < 1 mm定义为椎间融合,否则为不融合。所有影像学资料的测量均由未参加手术的同一位脊柱外科医师完成,并且由其他2位脊柱外科医师对结果进行审查和确认。
1.4 统计学处理使用SPSS 26.0软件对数据进行统计学分析。计量资料以x±s表示,组间比较采用方差分析,计数资料采用χ2检验;以P < 0.05为差异有统计学意义。
2 结果所有手术顺利完成,未发生食管、气管、主要血管或脊髓损伤等并发症。Zero-P组手术时间明显短于PCC组,差异有统计学意义(P < 0.05,表 2)。2组术中出血量相当,差异无统计学意义(P > 0.05,表 2)。2组患者术后JOA评分、VAS评分、C2~7颈椎曲度、手术节段Cobb角及邻近椎体高度均较术前显著改善,差异有统计学意义(P < 0.05,表 2)。术后24个月,Zero-P组C2~7颈椎曲度、手术节段Cobb角和邻近椎体高度较术后1个月降低,与PCC组相比差异亦有统计学意义(P < 0.05,表 2)。末次随访时所有患者均获得骨性融合。典型病例影像学资料见图 1、2。
|
|
表 2 2组患者统计数据 Tab. 2 Statistical data of 2 groups |
|
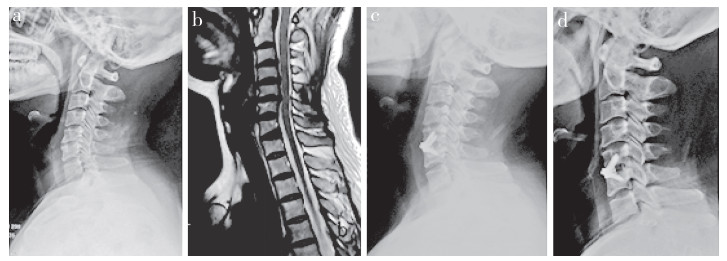
a:术前侧位X线片 b:术前MRI c:术后1个月侧位X线片示C2~7颈椎曲度、手术节段Cobb角及邻近椎体高度与术前相比均有所改善 d:术后24个月侧位X线片示C2~7颈椎曲度、手术节段Cobb角及邻近椎体高度与术后1个月相比有所丢失 a:Postoperative lateral roentgenograph b:Postoperative MRI c:Lateral roentgenograph at postoperative 1 month shows C2-7 cervical curvature, Cobb's angle of operative segment and adjacent vertebral height are improved compared with those before operation d:Lateral roentgenograph at postoperative 24 months shows C2-7 cervical curvature, Cobb's angle of operative segment and adjacent vertebral height are lost compared with those at postoperative 1 month 图 1 Zero-P组典型病例影像学资料 Fig. 1 Imaging data of a typical case in Zero-P group |
|
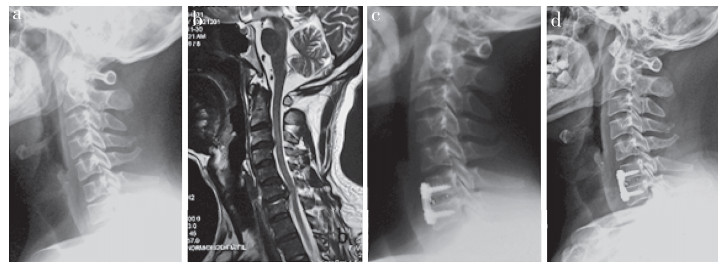
a:术前侧位X线片 b:术前MRI c:术后1个月侧位X线片示C2~7颈椎曲度、手术节段Cobb角及邻近椎体高度与术前相比均有所改善 d:术后24个月侧位X线片示C2~7颈椎曲度、手术节段Cobb角及邻近椎体高度无丢失 a:Postoperative lateral roentgenograph b:Postoperative MRI c:Roentgenograph at postoperative 1 month shows C2-7 cervical curvature, Cobb's angle of operative segment and adjacent vertebral height are improved compared with those before operation d:Roentgenograph at postoperative 24 months shows no loss of C2-7 cervical curvature, Cobb's angle of operative segment and adjacent vertebral height 图 2 PCC组典型病例影像学资料 Fig. 2 Imaging data of a typical case in PCC group |
彻底减压并有效重建颈椎稳定性和曲度是颈椎退行性疾病外科治疗的主要目标。在本研究中,尽管Zero-P组和PCC组临床结果相当,但PCC组的远期影像学结果优于Zero-P组。郭龙等[14]的研究发现,Zero-P提供强大稳定性的同时能有效控制手术创伤,并可以大大降低术后吞咽困难发生率,认为Zero-P组术后生活质量更好。Yang等[8]认为与PCC相比,Zero-P不仅可降低吞咽困难的发生率,也可降低邻近节段退行性变的发生率,术后内固定沉降和不融合的发生率也低。Vanek等[15]发现Zero-P组与PCC组术后6周颈椎Cobb角有一定变化。Lee等[16]对Zero-P、单椎间融合器和PCC 3组进行了12个月的随访观察,发现Zero-P组的临床疗效与PCC组相似,但Zero-P组在融合器沉降和椎体间融合方面逊于PCC组。
本研究结果显示,2组术中出血量无明显差异,但手术时间有显着差异。可能相关的因素:①Zero-P组无需显露上下椎体,只需显露椎间隙,减少对相邻椎间盘前纤维环干扰的同时缩短了手术操作的时间;②PCC组为了钢板能较好地与椎体前缘贴合,常规会使用高速磨钻进行骨赘打磨;③术中拧入螺钉时,Zero-P组钉道在一定范围内,以上、下40°的角度在套筒辅助下拧入螺钉,有较高的准确率,而PCC组则可能存在因钢板长短不合适或螺钉方向不佳而进行调整的可能。
本研究结果显示,2组术后JOA评分和VAS评分均较术前显著改善,临床症状改善满意。但Zero-P组术后24个月时C2~7颈椎曲度、手术节段Cobb角和邻近椎体高度与术后1个月相比均有所丢失。本研究组认为,症状缓解与减压程度相关,影像学改变是否会影响临床症状仍需进一步的随访研究。本研究组分析Zero-P组影像学结果不如PCC组有以下原因。①颈椎椎体上下终板解剖形态存在明显差异。上终板呈圆顶形,下终板呈凹形。而Zero-P上下表面是非解剖设计,在椎间隙测量和放置融合器的过程中,如果相邻上下终板未完全清理和重塑,与假体不匹配,可影响椎间融合速度;但过度清理或切除终板会导致骨骼板受伤,从而导致融合器的下沉。②颈椎退行性疾病常伴椎体前缘骨赘形成,为了尽可能重塑椎体外形及预防术后吞咽困难的发生及便于融合器置入,需要彻底清除骨赘,因此将不可避免地增加椎体前缘骨量的缺失。Barsa等[17]证实,去除椎体前的骨赘会影响椎体上、下终板对融合器的支撑,并增加术后融合器下沉的风险。Nemoto等[9]建议保留椎前骨赘为融合器提供重要的支撑。本研究PCC组术中用高速磨钻彻底清除骨赘,而Zero-P组则未清除椎前骨赘。③融合器的沉陷不仅受融合器大小及位置、终板接触面积和固定设计的影响,还与患者的骨质相关[8, 14-16]。Qi等[18]报道,在中期随访中,Zero-P组老年多节段颈椎病患者会出现颈椎曲度丢失、融合节段高度丢失,且有不同程度的融合器沉降发生。本研究患者平均年龄超过50岁,骨密度T值符合骨质减少诊断,因此,内固定对影像学结果的影响较明显。
本研究的主要局限性在于是单中心回顾性非随机性对照研究。且采用腰椎骨密度间接反映颈椎的骨密度,可能也是其局限性之一。此外,理论上当椎间隙融合后,融合器沉降和颈椎曲度的丢失将停止。但现有的影像学变化是否会影响远期临床结果尚不清楚,应在长期随访研究中予以证实。
综上,PCC可获得与Zero-P相同的临床效果,虽然PCC在控制手术时间方面不如Zero-P,但在术后24个月的随访中PCC可更好地维持颈椎曲度。
| [1] |
贾连顺. 颈椎病的诊断学基础[J]. 脊柱外科杂志, 2004, 2(3): 187-189. DOI:10.3969/j.issn.1672-2957.2004.03.021 |
| [2] |
杨有庚, 任宪盛, 杨晨, 等. 剖析颈椎病外科治疗的策略提高颈椎病前路手术的疗效[J]. 脊柱外科杂志, 2009, 7(5): 260-262. DOI:10.3969/j.issn.1672-2957.2009.05.002 |
| [3] |
Song KJ, Taghavi CE, Lee KB, et al. The efficacy of plate construct augmentation versus cage alone in anterior cervical fusion[J]. Spine(Phila Pa 1976), 2009, 34(26): 2886-2892. DOI:10.1097/BRS.0b013e3181b64f2c |
| [4] |
Pitzen TR, Chrobok J, Stulik J, et al. Implant complications, fusion, loss of lordosis, and outcome after anterior cervical plating with dynamic or rigid plates:two-year results of a multi-centric, randomized, controlled study[J]. Spine(Phila Pa 1976), 2009, 34(7): 641-646. DOI:10.1097/BRS.0b013e318198ce10 |
| [5] |
Riley LH 3rd, Skolasky RL, Albert TJ, et al. Dysphagia after anterior cervical decompression and fusion:prevalence and risk factors from a longitudinal cohort study[J]. Spine(Phila Pa 1976), 2005, 30(22): 2564-2569. DOI:10.1097/01.brs.0000186317.86379.02 |
| [6] |
Lee MJ, Bazaz R, Furey CG, et al. Influence of anterior cervical plate design on dysphagia:a 2-year prospective longitudinal follow-up study[J]. J Spinal Disord Tech, 2005, 18(5): 406-409. DOI:10.1097/01.bsd.0000177211.44960.71 |
| [7] |
Li Y, Hao D, He B, et al. The efficiency of zero-profile implant in anterior cervical discectomy fusion:a prospective controlled long-term follow-up study[J]. J Spinal Disord Tech, 2015, 28(10): 398-403. DOI:10.1097/BSD.0000000000000032 |
| [8] |
Yang HS, Chen DY, Wang XW, et al. Zero-profile integrated plate and spacer device reduces rate of adjacent-level ossification development and dysphagia compared to 11 ACDF with plating and cage system[J]. Arch Orthop Trauma Surg, 2015, 135(6): 781-787. DOI:10.1007/s00402-015-2212-z |
| [9] |
Nemoto O, Kitada A, Naitou S, et al. Stand-alone anchored cage versus cage with plating for single-level anterior cervical discectomy and fusion:a prospective, randomized, controlled study with a 2-year follow-up[J]. Eur J Orthop Surg Traumatol, 2015, 25(Suppl 1): S127-S134. |
| [10] |
Smith GW, Robinson RA. The treatment of certain cervical-spine disorders by anterior removal of the intervertebral disc and interbody fusion[J]. J Bone Joint Surg Am, 1958, 40-A(3): 607-624. |
| [11] |
Yonenobu K, Abumi K, Nagata K, et al. Interobserver and intraobserver reliability of the Japanese Orthopaedic Association scoring system for evaluation of cervical compression myelopathy[J]. Spine(Phila Pa 1976), 2001, 26(17): 1890-1895. DOI:10.1097/00007632-200109010-00014 |
| [12] |
Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127-1131. |
| [13] |
Lin W, Ha A, Boddapati V, et al. Diagnosing pseudoarthrosis after anterior cervical discectomy and fusion[J]. Neurospine, 2018, 15(3): 194-205. DOI:10.14245/ns.1836192.096 |
| [14] |
郭龙, 范顺武. 零切迹颈前路椎间融合系统与颈前路钢板椎间融合系统临床疗效比较[J]. 中国修复重建外科杂志, 2015, 29(7): 840-844. |
| [15] |
Vanek P, Bradac O, Delacy P, et al. Anterior interbody fusion of the cervical spine with Zero-P spacer:prospective comparative study-clinical and radiological results at a minimum 2 years after surgery[J]. Spine (Phila Pa 1976), 2013, 38(13): E792-E797. DOI:10.1097/BRS.0b013e3182913400 |
| [16] |
Lee YS, Kim YB, Park SW. Does a zero-profile anchored cage offer additional stabilization as anterior cervical plate?[J]. Spine(Phila Pa 1976), 2015, 40(10): E563-E570. DOI:10.1097/BRS.0000000000000864 |
| [17] |
Barsa P, Suchomel P. Factors affecting sagittal malalignment due to cage subsidence in standalone cage assisted anterior cervical fusion[J]. Eur Spine J, 2007, 16(9): 1395-1400. DOI:10.1007/s00586-006-0284-8 |
| [18] |
Qi M, Chen Y, Liu Y, et al. The use of a zero-profile device compared with an anterior plate and cage in the treatment of patients with symptomatic cervical spondylosis:a preliminary clinical investigation[J]. Bone Joint J, 2013, 95-B(4): 543-547. DOI:10.1302/0301-620X.95B4.30992 |
 2020, Vol.18
2020, Vol.18  Issue(4): 243-247, 252
Issue(4): 243-247, 252


