临床多采用颈椎前路椎间盘切除融合术(ACDF)治疗颈椎病,但多节段颈椎病患者采用该术式,因手术节段增多而显著增加假关节形成、植骨不融合及周围节段退行性变加速等风险[1]。非连续型多节段颈椎病的手术方案选择一直存在争议,重点集中于是否应保留中间正常的椎间盘。保留正常节段椎间盘的解决方案有应用人工椎间盘、零切迹融合固定或选择后路手术等[2]。有学者[3]提出,对于非连续型椎间盘突出压迫脊髓的患者,可保留相对正常的椎间盘,通过跳跃式手术完成植骨融合。但亦有研究[4]认为,此类术式可能引起中间被保留的椎间盘退行性变加速。本研究通过回顾性分析2013年1月—2018年12月收治的经非手术治疗无效的78例多节段颈椎病患者临床资料,探讨采用跳跃式和连续式ACDF治疗的疗效及安全性,现报告如下。
1 资料与方法 1.1 一般资料纳入标准:①年龄≥18岁;②颈脊髓及神经根受压症状持续6个月以上;③影像学检查证实2个及以上节段颈椎椎间盘突出[5];④非手术治疗无效。排除标准:①合并后纵韧带骨化症(OPLL);②既往有颈椎手术史;③颈椎外伤、颈椎急性损伤;④颈椎后凸畸形;⑤重度骨质疏松、代谢性骨病;⑥颈椎原发或转移性肿瘤。按照上述标准,纳入多节段颈椎病患者78例,其中36例采用跳跃式ACDF治疗(观察组),42例采用连续式ACDF治疗(对照组)。观察组男27例、女9例,年龄为(51.82±4.72)岁,病程为(11.03±3.30)个月;手术节段为C3/C4和C5/C6 18例,C4/C5和C6/C7 12例,C3/C4和C6/C7 6例。对照组男30例、女12例,年龄为(52.30±4.96)岁,病程为(10.78±3.17)个月;手术节段为C3~6 24例,C4~7 18例。2组患者一般资料差异无统计学意义(P>0.05),具有可比性。所有手术均由同一手术团队完成。
1.2 手术方法及术后处理患者全身麻醉后取仰卧位,做一颈前右侧横切口,依次经皮肤及颈阔肌完成颈阔肌瓣分离,经胸锁乳突肌前缘进入,剪开颈深筋膜,再沿血管鞘内侧钝性分离颈深筋膜至椎前,注意保护颈动脉鞘、食管及气管。X线透视辅助下确定病变椎间隙,撑开、固定椎体后有效切除病变椎间盘,并达椎体后缘,继续对双侧钩椎关节、椎体后缘骨赘及后纵韧带进行切除,暴露硬膜后沿椎体后壁潜行清除椎体后缘。将减压过程中切除的松质骨填塞入融合器,适当撑开椎间隙后置入融合器。2组采用相同操作处理病变节段,观察组采用跳跃式内固定,术中保留中间相对正常的椎间盘,对照组则进行连续内固定,同时,选择适宜钛板置于椎体前方固定。所有患者术后1 d佩戴颈托坐起进食,引流管拔除后下床活动,颈托制动3周,之后在无保护下适量完成功能锻炼。
1.3 观察指标记录2组手术时间、术中出血量、住院时间等临床指标及并发症发生情况。分别于术前、术后1周、术后12周及末次随访时采用改良日本骨科学会(JOA)评分[6]评估神经功能情况。JOA评分改善率(%)=(术后JOA评分-术前JOA评分)/(17-术前JOA评分)×100%,JOA评分改善率>50%判定为疗效优良。记录术前、术后12周及末次随访时2组C2~7活动度(C2~7 ROM,过伸、过屈位X线片上C2~7 Cobb角之和)、矢状位垂直距离(SVA,C2矢状位垂线与C7后上角垂线间的距离)、T1倾斜角(T1上缘连线与水平线间的夹角)、植骨融合率、邻近及中间节段椎间盘退行性变加重率等影像学指标。植骨融合判定标准为颈椎正侧位和屈伸动力位X线片或CT上可见椎间隙内连续骨小梁通过,屈伸动力位X线片上无相对运动发生。在MRI T2加权像上采用Pfirrmann分级[7]评估椎间盘退行性变情况,术后分级高于术前定义为退行性变加重。
1.4 统计学处理采用SPSS 24.0软件对数据进行统计分析,符合正态分布的计量资料以x±s表示,数据比较采用t检验和重复测量方差分析;计数资料以百分比(%)表示,数据比较采用χ2检验和Fisher确切概率法;以P < 0.05为差异有统计学意义。
2 结果所有手术顺利完成。所有患者随访8~19个月,中位随访时间为13个月。观察组手术时间和术中出血量明显少于对照组,差异有统计学意义(P < 0.05,表 1);2组住院时间差异无统计学意义(P>0.05,表 1)。2组术后各随访时间点JOA评分均较术前改善,差异有统计学意义(P < 0.05,表 1),组间差异无统计学意义(P>0.05,表 1);2组JOA评分改善率差异无统计学意义(P>0.05,表 1)。2组术后12周C2~7 ROM比术前降低,SVA及T1倾斜角较术前增加,差异有统计学意义(P < 0.05,表 1),组间差异无统计学意义(P>0.05,表 1);末次随访时C2~7 ROM、SVA及T1倾斜角均较术后12周有所改善,差异均有统计学意义(P < 0.05)。2组植骨融合率、邻近及中间节段椎间盘退行性变加重率差异无统计学意义(P>0.05,表 1)。观察组术后发生吞咽困难2例、声音嘶哑1例,并发症发生率为8.33%;对照组术后发生吞咽困难2例,并发症发生率为4.76%;组间差异无统计学意义(P>0.05)。典型病例影像学资料见图 1、2。
|
|
表 1 2组患者统计数据 Tab. 1 Statistical data of 2 groups |
|
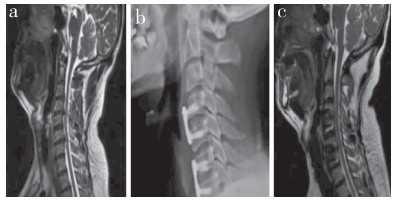
图 1 观察组典型病例影像学资料 Fig. 1 Imaging data of a typical case in observation group a:术前MRI示C4/C5和C6/C7椎间盘突出并压迫脊髓 b:术后3个月侧位X线片示内固定位置良好 c:术后12个月MRI示脊髓受压明显减轻,邻近节段和中间节段椎间盘退行性变未见加重 a: Preoperative MRI shows C4/C5 and C6/C7 intervertebral disc herniation and compression of spinal cord b: Lateral roentgenograph at postoperative 3 months shows that internal fixation is in good position c: MRI at postoperative 12 months shows a significant reduction in spinal cord compression and no exacerbation of intervertebral disc degeneration in adjacent and intermediate segments |
|
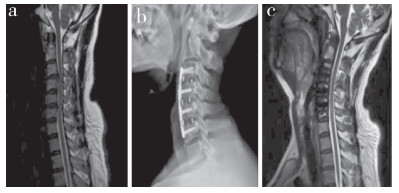
图 2 对照组典型病例影像学资料 Fig. 2 Imaging data of a typical case in control group a:术前MRI示C3/C4和C5/C6椎间盘突出并压迫脊髓 b:术后3个月侧位X线片示内固定位置良好 c:术后12个月MRI示脊髓受压明显减轻,邻近节段椎间盘退行性变未见加重 a: Preoperative MRI shows C3/C4 and C5/C6 intervertebral disc herniation and compression of spinal cord b: Lateral roentgenograph at postoperative 3 months shows that internal fixation is in good position c: MRI at postoperative 12 months shows a significant reduction in spinal cord compression and no exacerbation of intervertebral disc degeneration in adjacent segments |
ACDF已被广泛用于颈椎病的治疗,其能够直接清除脊髓前方压迫因素,包括发生退行性变的椎间盘、椎体后缘骨赘及异常的后纵韧带等,同时可通过椎间植骨有效促进椎间隙高度恢复,总体疗效及安全性令人满意[8]。既往治疗非连续型多节段颈椎病,因担心跳过正常节段使得椎间应力增加,出现退行性变加剧的问题,相当一部分临床医师倾向采用连续式ACDF进行治疗,但随之而来的假性关节形成、植骨融合率下降等并发症严重影响远期预后[9]。近年来,多项临床研究[10-11]采用跳跃式ACDF治疗非连续型多节段颈椎病,通过前路减压、分别融合完成手术,尽管具体减压融合效果存在差异,但在神经功能改善方面令人满意。如何有效维持术后颈椎正常生理曲度及ROM被认为是改善颈椎病患者脊柱稳定性、提高生活质量的关键。本研究结果显示,末次随访时2组C2~7 ROM均较术后12周时有所恢复,提示2种方式治疗多节段颈椎病,术后颈椎ROM均可逐渐恢复至术前水平。相关研究[12]显示,ACDF术后C2~7 ROM下降使得相邻节段ROM增大以保证颈椎整体ROM,会进一步导致相应椎间盘及关节突关节应力增加,最终导致椎间盘退行性变加速。但本研究纳入患者手术节段多位于低位颈椎,因胸廓、肩胛骨等遮挡导致邻近节段ROM无法测量。
术后颈椎矢状位失衡被认为是导致患者术后疼痛及功能障碍的原因[13]。有研究[14]证实,SVA与多节段颈椎病患者植骨融合术后邻近节段发生病变密切相关,SVA增大使得融合邻近节段应力增加;同时,T1倾斜角增大亦是导致颈椎失稳的独立危险因素之一,T1倾斜角增大可引起颈椎前倾,从而导致SVA进一步增大。本研究结果显示,末次随访时2组SVA和T1倾斜角较术后12周有所改善,接近术前水平,与既往研究[15]结果相似,说明2种术式均能够较好地维持颈椎术后矢状位曲度。
一项长期随访回顾性研究[16]显示,1~2个节段颈椎病患者ACDF术后与健康人群邻近节段退行性变情况比较,上下位邻近节段髓核、椎间盘突出及椎间隙狭窄信号改变率分别为45.71%、42.36%,61.35%、44.08%,12.74%、14.50%。而另一项针对1~4个节段颈椎病患者ACDF术后的长期随访研究[17]报道,上下位邻近节段髓核、椎间盘突出及椎间隙狭窄信号改变率分别为97%、97%,74%、48%,43%、30%。本研究采用Pfirrmann分级对相邻节段及中间保留节段的椎间盘退行性变情况进行评估,结果显示,2组邻近和中间节段椎间盘退行性变加重率差异无统计学意义,说明跳跃式ACDF术后邻近节段退行性变加重情况与连续式ACDF相近,同时跳跃式ACDF术后中间保留节段椎间盘并未出现退行性变加速的问题。国外学者[18]的相关报道指出,前路融合术后邻近节段退行性变发生风险每年增加3%,随访10年发生率达25%。本研究随访过程中未发现明显邻近节段退行性变,邻近节段和中间被保留椎间盘退行性变程度亦较以往文献报道轻,其可能原因:①随访时间短;②纳入患者年龄偏小;③C5/C6、C6/C7等高危节段术中被有效处理。
本研究的局限性:①纳入病例较少,为单中心、回顾性研究,结果存在偏倚;②术前、术后MRI参数并不完全一致,可能影响椎间盘退行性变评估结果;③随访时间最长仅为19个月,无法客观评估中长期手术效果及安全性;④2组手术节段分布难以完全匹配,可能影响研究结果。综上所述,跳跃式ACDF治疗经非手术治疗无效的多节段颈椎病患者可获得与连续式ACDF相近的疗效,并能够有效缩短手术时间,减少术中医源性创伤。
| [1] |
陈竞轩, 张志超, 石维, 等. 改良颈椎前路单椎体次全切除融合术并单节段颈椎前路椎间盘切除融合术治疗多节段脊髓型颈椎病[J]. 脊柱外科杂志, 2021, 19(2): 94-99. DOI:10.3969/j.issn.1672-2957.2021.02.005 |
| [2] |
关海山, 李承罡, 史洁, 等. 前路减压融合术与后路单开门椎管扩大成形术治疗多节段脊髓型颈椎病的中期随访研究[J]. 中华骨科杂志, 2019, 39(17): 1044-1052. DOI:10.3760/cma.j.issn.0253-2352.2019.17.002 |
| [3] |
Zhan Y, Yuan Z, Wang Q, et al. Treatment of multi-segmental cervical spondylotic myelopathy by posterior spatium intermusculare approach for spinal canal expansion and laminoplasty[J]. Minerva Chir, 2018, 73(2): 248-249. |
| [4] |
何俊波, 刘浩, 吴廷奎, 等. 颈椎前路椎间盘切除融合术与人工颈椎椎间盘置换术治疗跳跃型颈椎椎间盘突出症的生物力学效应有限元分析[J]. 脊柱外科杂志, 2021, 19(1): 38-45. DOI:10.3969/j.issn.1672-2957.2021.01.007 |
| [5] |
胡永成, 马信龙. 骨科疾病的分类与分型标准[M]. 第2版. 北京: 人民卫生出版, 2014: 112-113.
|
| [6] |
Yonenobu K, Wada E, Tanaka T, et al. Japanese Orthopaedic Association cervical myelopathy evaluation questionnaire(JOACMEQ): Part 2. Endorsement of the alternative item[J]. J Orthop Sci, 2007, 12(3): 241-248. DOI:10.1007/s00776-007-1119-0 |
| [7] |
Pfirrmann CW, Metzdorf A, Zanetti M, et al. Magnetic resonance classification of lumbar intervertebral disc degeneration[J]. Spine(Phila Pa 1976), 2001, 26(17): 1873-1878. DOI:10.1097/00007632-200109010-00011 |
| [8] |
史吉胜, 吕明波, 林斌, 等. 颈前路杂合与多节段融合术治疗多节段颈椎病的比较[J]. 中国矫形外科杂志, 2017, 25(21): 1927-1932. |
| [9] |
Qin R, Chen X, Zhou P, et al. Anterior cervical corpectomy and fusion versus posterior laminoplasty for the treatment of oppressive myelopathy owing to cervical ossification of posterior longitudinal ligament: a meta-analysis[J]. Eur Spine J, 2018, 27(6): 1375-1387. DOI:10.1007/s00586-017-5451-6 |
| [10] |
Koda M, Mochizuki M, Konishi H, et al. Comparison of clinical outcomes between laminoplasty, posterior decompression with instrumented fusion, and anterior decompression with fusion for K-line(-) cervical ossification of the posterior longitudinal ligament[J]. Eur Spine J, 2016, 25(7): 2294-2301. DOI:10.1007/s00586-016-4555-8 |
| [11] |
Phan K, Scherman DB, Xu J, et al. Laminectomy and fusion vs laminoplasty for multi-level cervical myelopathy: a systematic review and meta-analysis[J]. Eur Spine J, 2017, 26(1): 94-103. DOI:10.1007/s00586-016-4671-5 |
| [12] |
Miyakoshi N, Kudo D, Hongo M, et al. Intradural extramedullary tumor in the stenotic cervical spine resected through open-door laminoplasty with hydroxyapatite spacers: report of two cases[J]. BMC Surg, 2018, 18(1): 38. DOI:10.1186/s12893-018-0372-9 |
| [13] |
王震, 田纪伟. 颈椎后凸畸形的研究进展[J]. 中国矫形外科杂志, 2009, 17(18): 1393-1396. |
| [14] |
Lee GW, Cho CW, Shin JH, et al. Which technique is better option for C3 segment in multi-level open-door laminoplasty of the cervical spine? Laminectomy versus laminoplasty[J]. Spine(Phila Pa 1976), 2017, 42(14): E833-E840. DOI:10.1097/BRS.0000000000001974 |
| [15] |
Luo W, Li Y, Zhao J, et al. Open-versus French-door laminoplasty for the treatment of cervical multilevel compressive myelopathy: a meta-analysis[J]. World Neurosurg, 2018, 117: 129-136. DOI:10.1016/j.wneu.2018.06.026 |
| [16] |
Burkhardt BW, Simgen A, Wagenpfeil G, et al. Adjacent segment degeneration after anterior cervical discectomy and fusion with an autologous iliac crest graft: a magnetic resonance imaging study of 59 patients with a mean follow-up of 27 years[J]. Neurosurgery, 2018, 82(6): 799-807. DOI:10.1093/neuros/nyx304 |
| [17] |
Suh BG, Ahn MW, Kim HJ, et al. Wedge-shaped resection of the posterior bony arch during open door laminoplasty to prevent postoperative motion limitation[J]. Spine(Phila Pa 1976), 2017, 42(3): 143-150. DOI:10.1097/BRS.0000000000001689 |
| [18] |
Gillis CC, Kaszuba MC, Traynelis VC. Cervical radiographic parameters in 1- and 2-level anterior cervical discectomy and fusion[J]. J Neurosurg Spine, 2016, 25(4): 421-429. DOI:10.3171/2016.2.SPINE151056 |
 2022, Vol.20
2022, Vol.20  Issue(4): 230-234
Issue(4): 230-234


