腰椎退行性疾病是脊柱外科常见疾病,主要包括腰椎椎间盘突出、腰椎椎管狭窄及腰椎滑脱,非手术治疗无效时须手术干预。传统的开放式融合术能改善患者症状,但也存在术中椎旁肌肉剥离多、软组织损伤大、出血多等问题,术后腰背部僵硬、慢性下腰痛等问题也颇为常见[1-2]。近年来,脊柱内窥镜技术发展迅速,各种内窥镜下融合技术应运而生,经椎间孔入路术式报道较多,疗效肯定[3-4],而后路经椎板间入路报道较少。2017年,韩国学者Heo等[5]首次采用双通道内窥镜(一个观察通道,一个器械操作通道)对69例腰椎椎管狭窄症患者进行了经椎板间入路减压融合内固定的组合手术。本院从2019年开始采用全内窥镜下后方经椎板间入路腰椎椎间融合术(FE-PLIF)治疗单节段腰椎退行性疾病,临床效果肯定,现报告如下。
1 资料与方法 1.1 一般资料纳入标准:①病史、查体、CT和MRI等影像学检查确诊为单节段腰椎退行性疾病;②存在腰腿痛等典型症状;③非手术治疗3个月无效;④符合融合手术指征[6]。排除标准:①严重脊柱侧凸、后凸畸形;②腰椎椎间盘极外侧突出;③存在脊柱局部感染或凝血异常等手术禁忌证;④既往开放手术或椎管内注射治疗导致的硬膜外瘢痕。根据上述标准,纳入2019年3月—2021年3月采用FE-PLIF治疗单节段腰椎退行性疾病患者27例,其中男16例、女11例,年龄为(56.14±9.52)岁,病程3~10(6.1±2.8)年;腰椎椎间盘突出伴不稳10例,腰椎椎管狭窄11例,腰椎滑脱6例;手术节段L3/L4 5例,L4/L5 14例,L5/S1 8例。
1.2 手术方法患者全身麻醉后俯卧位于手术架上,保持腹部悬空,避免受压,同时保持正常腰椎曲度。手术床须允许正侧位X线透视,且X线透视机能在手术床下方完成正侧位透视切换,避免跨越无菌区。患者上肢置于托板上,上肢避免过度外展以避免臂丛神经牵拉损伤。手术采用德国Spinendos单通道全脊柱内窥镜系统,从椎板间隙入路进入。以腰椎椎管狭窄症手术为例,根据术前规划及术中X线透视图像确定手术切口,包括4枚经皮椎弓根螺钉的切口、内窥镜手术切口。常规消毒、铺单。置入经椎板间隙通道,透视确认位置正确。工作套管头部应位于手术节段相邻椎板间隙内,黄韧带背侧。内窥镜下切除同侧上位椎体下关节突及下位椎体上关节内侧大部分骨质,保留上关节突外侧骨壁以保护出口神经根免于损伤。然后在内窥镜下显露椎板间隙黄韧带,由中央向外侧切开黄韧带,显露椎管内硬膜囊、神经根等。根据脱出髓核与神经根的关系,选择肩路或腋路摘除突出的椎间盘。对于全椎管狭窄,可以采用单侧椎板间隙入路双侧减压切除双侧肥厚黄韧带及增生的关节突关节内侧部分。更换套管,依次使用圆形可旋转骨锉、环形刮匙、髓核钳等摘除椎间盘内髓核组织及剥脱软骨终板,再以终板刮匙及可扩张终板处理器刮除软骨终板,暴露骨性终板,准备椎间植骨床。经融合器通道放置植骨套管,将咬除的关节突去除软组织后咬碎填入椎体间隙。放入专门的神经根挡板,将融合器试模置入椎体间隙,确定融合器大小;然后将充填自体骨的融合器[全内窥镜下腰椎椎间融合系统(聚醚醚酮,博能华,中国)]置入椎间隙的中心。采用经皮椎弓根螺钉系统,在X线透视引导下或导航系统引导下置入。术毕缝合手术切口,无菌敷料覆盖。
1.3 观察指标记录术前和术后3 d、3个月、6个月、1年的腰腿痛视觉模拟量表(VAS)评分[7]、Oswestry功能障碍指数(ODI)[8]及并发症发生情况。术后1年复查CT和MRI,采用Brantigan等[9]的标准评估术后融合率。
1.4 统计学处理采用SPSS 21.0软件对数据进行统计分析。符合正态分布的计量资料以x±s表示,采用t检验;计数资料以例数或百分数表示,采用χ2检验;以P<0.05为差异有统计学意义。
2 结果所有手术顺利完成,手术时间为(243.62±46.73)min,出血量为(68.37±23.54)mL(镜下出血估算平均约15 mL,置钉出血量采用纱布估算,一块纱布湿透估算出血量约20 mL)。所有患者随访(16.8±3.1)个月。所有患者术后各时间点腰腿痛VAS评分和ODI较术前显著改善,术后3个月、6个月和1年时较术后3 d显著改善,差异均有统计学意义(P<0.05,表 1)。发生术后血肿1例,导致左侧拇长伸肌肌力下降至3级,再次内窥镜下清除血肿后肌力恢复正常;其余患者均未发生神经或血管损伤并发症。术后1年,27例患者中25例椎间骨性融合,融合率为92.6%(25/27);2例未达到融合标准,但患者的主观症状显著改善,主要包括腰背部疼痛及下肢神经根性疼痛症状明显缓解,分析这2例患者症状明显缓解的主要原因:①术中彻底减压,神经根压迫完全解除;②随访时间尚短,暂未出现内固定松动等情况。所有患者未发生融合器、内固定物移位等情况。典型病例影像学资料见图 1。
|
|
表 1 手术前后VAS评分和ODI Tab. 1 Preoperative and postoperative VAS score and ODI |
|
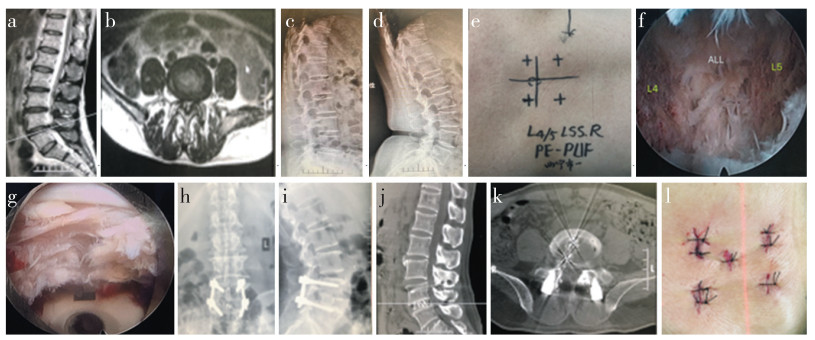
图 1 典型病例影像学资料 Fig. 1 Imaging data of a typical case a、b:术前MRI示L4/L5椎管狭窄伴椎间隙退行性变 c、d:术前动力位X线片示L4/L5节段不稳 e:术前G形臂X线机透视定位体表标记 f:内窥镜下减压并处理软骨终板 g:神经根与融合器的位置关系 h、i:术后3 d X线片示椎弓根螺钉及融合器位置良好 j、k:术后6个月CT示融合器及内置物位置良好,椎间骨性融合 l:术后手术切口 a, b: Preoperative MRIs show L4/L5 spinal stenosis with intervertebral space degeneration c, d: Preoperative dynamic roentgenographs show L4/L5 instability e: Preoperative G-arm X-ray machine fluoroscopic localization of body surface markers f: Decompression and remove of cartilaginous endplate under endoscope g: Location relationship between nerve root and fusion cage h, i: Roentgenographs at postoperative 3 d show good position of pedicle screws and fusion cage j, k: CTs at postoperative 6 months show that fusion cage and implants are in good position, and intervertebral bone fusion l: Postoperative surgical incision |
目前,经椎板间入路行内窥镜下腰椎椎间融合术的报道相对较少。Ruetten等[10]报道采用经椎板间入路FE-PLIF治疗331例腰椎椎间盘突出症患者并随访2年,结果显示,82%的患者不再感到腿部疼痛,13%的患者只是偶尔感到疼痛,减压效果与常规手术相当,椎旁肌和椎管内结构的创伤均较开放手术减轻,硬膜外瘢痕也明显减少,未观察到严重的手术并发症。Jiang等[11]采用经椎板间入路FE-PLIF治疗单节段腰椎退行性疾病患者24例,术后1年腰痛及腿痛VAS评分、ODI均较术前显著改善。以上结果与本研究结果一致,也再次肯定了经椎板间入路FE-PLIF治疗单节段腰椎退行性疾病的临床价值。
FE-PLIF与传统开放式PLIF相比有明显优势。①FE-PLIF对椎旁肌损伤相对较小。PLIF需要剥离椎旁肌肉,影响了腰椎的稳定及矢状面平衡。为了减少对椎旁肌的损伤,微创经椎间孔腰椎椎间融合术(MIS-TLIF)应运而生,但是MIS-TLIF的通道也存在对椎旁肌的牵拉、挤压。而FE-PLIF的所有操作均是在内窥镜下完成,对椎旁肌损伤极小,且不损伤后方复合体。②传统PLIF椎板切除范围大,采用骨刀或其他动力系统直接切除上位椎体下半部分椎板及下位椎体上半部分椎板,而FE-PLIF是从切除上下椎板间黄韧带开始向外侧减压,对椎板的切除有限,达到减压及通道置入目的即可。根据本研究组的临床经验,对椎板间隙大的病例,无须切除椎板即可完成减压及通道置入,仅对于椎板间隙狭窄的病例需切除部分上位椎体部分椎板,即便如此,与开放手术相比,术中创伤明显减小,出血量显著降低。
就手术入路而言,内窥镜下腰椎椎间融合主要包括经椎间孔入路和经椎板间入路,后者根据使用器械的不同又分为单通道系统(FE-PLIF技术)和单侧双通道系统(UBE技术)。文献报道较多的是经椎间孔入路内窥镜技术,其原因可能在于腰椎各节段Kambin三角的解剖尺寸允许安全置入椎间融合器[12-13]。Kambin三角的充分显露可通过切除上关节突大部分骨质来实现,但是切除位置应尽量靠近椎间孔下半部分,既能获得充分的安全空间,又可避免引起出口神经根刺激,甚至损伤[14]。不过,任何一种手术方式都有其适应证,目前多数研究[15-16]认为,经椎间孔入路内窥镜技术首选用于极外侧型、中央型及复发性的椎间盘突出;腋部及游离型椎间盘突出,髂嵴较高、横突较大及椎间孔狭窄的L5/S1节段椎间盘突出更宜采用经椎板间入路。本研究组也支持这一观点。
本研究中27例患者均未发生重大并发症,术后1年融合率为92.6%,这充分肯定了经椎板间入路FE-PLIF的安全性。理论上讲,内窥镜下置入椎间融合器损伤硬膜及神经根的风险较高,本研究术中置入融合器时,首先沿通道外缘放置神经挡板至椎间隙,这时内窥镜下可清楚观察到神经挡板将硬膜及神经根挡住,随后置入融合器,手术安全性得到了保证。Osman等[17]采用椎体间打压自体松质骨植骨结合经皮椎弓根螺钉内固定治疗合并椎管狭窄的腰椎节段不稳定、腰椎滑脱症患者60例,在平均12个月的随访期间,其椎间融合率为59.6%。随着脊柱内窥镜技术的进步,内窥镜下融合手术在临床疗效和安全性上都获得了长足的发展。Kim等[18]采用UBE技术治疗57例腰椎退行性疾病患者,在平均2年的随访中并发症发生率为5.3%,包括1例硬膜外血肿,1例融合器下沉,1例一过性瘫痪,最终融合率达100%。近期的一项荟萃分析[19]同样肯定了内窥镜下融合手术的安全性,该分析共纳入了12项研究,981例腰椎退行性变患者,系统对照了449例内窥镜下融合病例和532例MIS-TLIF或PLIF病例的临床结局,结果发现,二者并发症发生率、融合率无显著差异,而内窥镜下融合病例还有着明显更少的术中出血量、更短的住院时间、更佳的疼痛缓解,结果与本研究类似,一定程度上肯定了经椎板间入路FE-PLIF治疗腰椎退行性疾病的有效性与安全性。
本研究还存在一些局限性,首先样本量偏小、随访时间偏短,还需要大样本的长期随访研究来进一步验证其长期临床结局。其次,本研究属于回顾性分析,存在混杂因素控制不足等研究设计缺陷。
综上,经椎板间入路FE-PLIF可有效治疗单节段腰椎退行性疾病,术后融合率高,手术微创,且无重大并发症,为须行融合手术治疗的患者提供了另一种选择。
| [1] |
李毅嵩, 王庆敏, 吴志君, 等. 微创及传统开放手术治疗腰椎退行性疾病临床比较[J]. 外科研究与新技术, 2017, 6(4): 253-255. DOI:10.3969/j.issn.2095-378X.2017.04.007 |
| [2] |
王超兰. 腰椎术后骶髂关节源性下腰痛发病机制及临床治疗[J]. 外科研究与新技术, 2018, 7(1): 61-64. |
| [3] |
Zhang KH, Zhang WH, Xu BS, et al. CT-based morphometric analysis of approach of percutaneous transforaminal endoscopic lumbar interbody fusion[J]. Orthop Surg, 2019, 11(2): 212-220. DOI:10.1111/os.12434 |
| [4] |
严小林, 陈彦, 陈永华, 等. 经皮内窥镜下经椎间孔入路腰椎椎间融合术治疗腰椎椎管狭窄症[J]. 脊柱外科杂志, 2022, 20(6): 385-389. DOI:10.3969/j.issn.1672-2957.2022.06.005 |
| [5] |
Heo DH, Son SK, Eum JH, et al. Fully endoscopic lumbar interbody fusion using a percutaneous unilateral biportal endoscopic technique: technical note and preliminary clinical results[J]. Neurosurg Focus, 2017, 43(2): E8. DOI:10.3171/2017.5.FOCUS17146 |
| [6] |
中国康复医学会脊柱脊髓损伤专业委员会脊柱微创学组, 中国康复医学会脊柱脊髓专业委员会腰椎研究学组. 脊柱内镜辅助下腰椎椎体间融合术应用的中国专家共识[J]. 中华医学杂志, 2023, 103(5): 329-335. DOI:10.3760/cma.j.cn112137-20220817-01749 |
| [7] |
Huskisson EC. Measurement of pain[J]. Lancet, 1974, 2(7889): 1127-1131. |
| [8] |
Fairbank JC, Couper J, Davies JB, et al. The Oswestry low back pain disability questionnaire[J]. Physiotherapy, 1980, 66(8): 271-273. |
| [9] |
Brantigan JW, Steffee AD. A carbon fiber implant to aid interbody lumbar fusion. Two-year clinical results in the first 26 patients[J]. Spine(Phila Pa 1976), 1993, 18(14): 2106-2117. |
| [10] |
Ruetten S, Komp M, Godolias G. A new full-endoscopic technique for the interlaminar operation of lumbar disc herniations using 6-mm endoscopes: prospective 2-year results of 331 patients[J]. Minim Invasive Neurosurg, 2006, 49(2): 80-87. DOI:10.1055/s-2006-932172 |
| [11] |
Jiang C, Yin S, Wei J, et al. Full-endoscopic posterior lumbar interbody fusion with epidural anesthesia: technical note and initial clinical experience with one-year follow-up[J]. J Pain Res, 2021, 14: 3815-3826. DOI:10.2147/JPR.S338027 |
| [12] |
Hardenbrook M, Lombardo S, Wilson MC, et al. The anatomic rationale for transforaminal endoscopic interbody fusion: a cadaveric analysis[J]. Neurosurg Focus, 2016, 40(2): E12. DOI:10.3171/2015.10.FOCUS15389 |
| [13] |
陈政宇, 晏怡果, 尹健, 等. 不同入路腰椎椎间融合术的应用现状及进展[J]. 脊柱外科杂志, 2022, 20(1): 58-62. |
| [14] |
Li ZZ, Hou SX, Shang WL, et al. Modified percutaneous lumbar foraminoplasty and percutaneous endoscopic lumbar discectomy: instrument design, technique notes, and 5 years follow-up[J]. Pain Physician, 2017, 20(1): E85-E98. |
| [15] |
Youn MS, Shin JK, Goh TS, et al. Full endoscopic lumbar interbody fusion(FELIF): technical note[J]. Eur Spine J, 2018, 27(8): 1949-1955. DOI:10.1007/s00586-018-5521-4 |
| [16] |
杨晋才. 经皮内镜辅助腰椎融合技术面临的问题与挑战[J]. 中华医学杂志, 2019, 99(33): 2566-2568. |
| [17] |
Osman SG. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: a case series report[J]. Int J Spine Surg, 2012, 6: 157-166. |
| [18] |
Kim JE, Yoo HS, Choi DJ, et al. Learning curve and clinical outcome of biportal endoscopic-assisted lumbar interbody fusion[J]. BioMed Res Int, 2020, 2020: 8815432. |
| [19] |
Yang H, Cheng F, Hai Y, et al. Unilateral biportal endoscopic lumbar interbody fusion enhanced the recovery of patients with the lumbar degenerative disease compared with the conventional posterior procedures: a systematic review and meta-analysis[J]. Front Neurol, 2023, 13: 1089981. |
 2024, Vol.22
2024, Vol.22  Issue(1): 12-15, 31
Issue(1): 12-15, 31


